Perkutaaninen kolekystostomia akuutin kolekystiitin hoitona: Mitä on tapahtunut viimeisten viiden vuoden aikana? A literature review | Revista de Gastroenterología de México
Introduction
Sappirakon patologia on yksi yleisimpiä yleiskirurgin kohtaamia sairauksia. Tällä hetkellä laparoskooppista kolekystektomiaa (LC) pidetään kultaisena standardina akuutin kolekystiitin (AC) hoidossa. Toimenpiteeseen liittyvää sairastuvuutta ja kuolleisuutta on pyritty vähentämään korkean riskin kirurgisilla potilailla vähemmän invasiivisilla toimenpiteillä, kuten perkutaanisella kolekystostomialla (PC).
AC on sappirakon tulehduksellinen sairaus, jonka patofysiologia koostuu sappirakon tyhjennysreittien tukkeutumisesta tai sen seinämien dysmotiliteetista, mikä aiheuttaa sappirakon sisäisen paineen nousun, seinämän turvotuksen, muuttuneen verisuonituksen, johon liittyy iskemiaa tai nekroosia, bakteerien leviämistä tai sappirakon perforaatiota. PC:n tavoitteena AC:ssa on mahdollistaa sappitiehyen tyhjennys akuuttien oireiden poistamiseksi ja paikallisten ja systeemisten komplikaatioiden kehittymisen estämiseksi. PC on yleensä varattu AC-potilaille, jotka ovat korkean riskin leikkauspotilaita tai joilla on elimellinen vajaatoiminta. PC:llä on tässä yhteydessä hyödyllisiä etuja: yleisanestesiaa ei tarvita, se voidaan suorittaa potilaan vuodeosastolla, se on nopea toimenpide, sen onnistumisprosentti on yli 95 prosenttia, sen komplikaatioiden osuus on alhainen ja sitä voidaan käyttää siirtymähoitona ennen elektiivistä leikkausta.
Sappirakon tyhjennys on hoitovaihtoehto, joka sisältyy tärkeimpiin kansainvälisiin AC:n hoitoa koskeviin ohjeisiin, mutta sen tuloksista kriittisesti sairailla potilailla, tarkoista käyttöaiheista ja paremmuudesta verrattuna lopulliseen kirurgiseen hoitoon on edelleen kiistelty.
PC:n läpikäyneiden potilaiden seurannasta ja hoidosta on vain vähän näyttöä. Useimmissa tutkimuksissa keskitytään toimenpiteestä hyötyvien potilaiden valintaan, mutta vain harvat kuvaavat potilaan myöhempää hoitoa. Analysoimme tässä yhteydessä näyttöä PC:n hyödyllisyydestä AC:n hoidossa ja ehdotamme algoritmia PC-katetrin hoitoa varten.
Kriteerit akuutin kolekystiitin vaikeusasteen luokittelemiseksi
Akuuttia kolekystiittiä koskevissa Tokion vuoden 2018 ohjeissa (TG18) AC:n vaikeusaste luokitellaan lieväksi (luokka I), keskivaikeaksi (luokka II) ja vaikeaksi (luokka III).1 Mainitussa luokittelussa otetaan huomioon potilaan liitännäissairaudet, oireiden kesto, fyysiset löydökset sairaalaan tullessa, merkit systeemisestä tulehdusvasteesta, merkittävän paikallisen tulehduksen esiintyminen kuvantamistutkimuksissa ja elinten toimintahäiriöiden kehittyminen. TG-luokitus on hyödyllinen, koska taudin vaikeusaste korreloi kuolleisuuden, sairastuvuuden, sairaalassaoloajan pituuden ja laparoskooppisesta leikkauksesta avoleikkaukseen siirtymisen osuuden kanssa (taulukot 1 ja 2).
| Luokka I (lievä) | Luokka II (keskivaikea) | Luokka III (vaikea-asteinen) |
|---|---|---|
|
Mikä tahansa seuraavista tiloista:
|
Mikä tahansa seuraavista elinten toimintahäiriöistä:
|
Erilaisten vaikeusasteiden ominaispiirteet.
| Mortaliteetti 30 vuorokauden kuluttua2 | Morbiditeetti78 | Sairaalassaoloaika78,a | Muutosprosentti78,a | |
|---|---|---|---|---|
| Luokka I | 1.1 % | 2.9 % | 3 (1-16) | 7 % |
| Luokka II | 0.8 % | 3.1 % | 4 (1-33) | 25.6 % |
| Luokka III | 5.4 % | 11.1 % | 7 (1-60) | 34.6 % |
Keskiarvo±SD.
Varhainen LC (72 tunnin kuluessa) olisi mieluiten suoritettava I- ja II-asteen AC-tapauksissa, jos Charlsonin komorbiditeetti-indeksi (Charlson comorbidity index, CCI) ja toimintakyky amerikkalaisen anestesialääkäriyhdistyksen (American Society of Anesthesiologists, ASA) luokittelujärjestelmän mukaisesti viittaavat siihen, että potilas voi sietää leikkauksen. Päinvastoin, olisi aloitettava lääkehoito (antibiootit ja yleistuki) ja harkittava kirurgista hoitoa, kun olosuhteet paranevat. Asteen II AC:ssa suositellaan lisäksi perkutaanisen dreneerauksen suorittamista, kun potilas ei siedä kirurgista hoitoa.1
Vuoden 2013 Tokion ohjeissa (TG13) AC luokitellaan asteeseen III, kun on viitteitä elinten toimintahäiriöstä, ja se määritellään, kun kyseessä on sydän- ja verenkiertoelimistön, neurologinen, hengityselimistön, munuaisten, maksan tai hematologinen vajaatoiminta. TG13:n mukaan hätä-LC on vasta-aiheinen, jos kyseisissä elinjärjestelmissä on toimintahäiriöitä. Vuonna 2017 Yokoe ym.2 antoivat kuitenkin tietoa AC:n hoidosta japanilaisessa ja taiwanilaisessa populaatiossa (n=5 329), jossa LC tehtiin onnistuneesti suurimmalle osalle potilaista, joilla oli asteen III AC. Sama kohortti analysoitiin myöhemmin uudelleen painottaen niitä potilaita, joilla oli elimellinen toimintahäiriö ja joille voitiin turvallisesti tehdä kirurginen hoito. Potilailla, joilla oli CCI>6 pistettä, oli suurempi kuolleisuus. Tutkimuksen tärkein hyöty oli sen monimuuttujainen logistinen regressioanalyysi, joka osoitti, että keltaisuus, neurologinen toimintahäiriö ja hengitystoiminnan häiriö olivat riippumattomia kuolleisuutta ennustavia tekijöitä 30 päivän kuluttua potilailla, joilla oli asteen III AC. Kuitenkaan ei ollut näyttöä lisääntyneestä kuolleisuudesta III asteen AC-potilailla, joilla oli muun tyyppinen elinten vajaatoiminta ja joille tehtiin LC.3 Näin ollen TG18 määritteli neurologisen toimintahäiriön, hengityshäiriön tai keltaisuuden (kokonaisbilirubiinipitoisuus ≥ 2 mg/dl) kuolleisuutta ennustaviksi tekijöiksi III asteen AC:ssa. -9 Harvinaisempia indikaatioita ovat ne, joiden tavoitteena on sappiteiden ohjaaminen transkolekystisen pääsyn avulla, jota pidetään useimmissa tapauksissa suhteellisen toissijaisena, koska endoskooppisten tai transhepaattisten ohjausten suorittamista suositaan. Mainitut skenaariot on koottu taulukkoon 3.10-13
Indikaatiot perkutaanisen kolekystostomian asettamiseen.
Vaikea akuutti kolekystiitti vuoden 2018 Tokio-ohjeiden mukaan
Akuutti kolekystiitti ja ASA-luokitus >3 tai Charlsonin komorbiditeetti-indeksi >6
Toisen linjan pääsy sappitiehyeeseen:Pahanlaatuisen sappitievaurion silloitusSappitiestriktuuran laajentaminenSappitiefistelin ulostulon diversioSappitien dekompressio kolangiitissaMuut
Ei TG13:ssa vakiintunutta,14 TG18 korostaa, että kiireellinen sappirakon tyhjennys voidaan tehdä luokan II AC:n yhteydessä, kun laparoskopia ei ole käytettävissä ja lääkkeelliseen alkuhoitoon ei saada riittävää vastetta, pääasiassa potilailla, joiden yleistila on ”huono” (CCI>6 pistettä tai ASA-luokitus >3). Tätä ehdotusta tukee vuonna 2017 tehty monikeskuksinen retrospektiivinen tutkimus15 , johon osallistui 1 764 potilasta kahden vuoden aikana, mutta jossa vain 330 potilasta jaettiin vertailua varten kahteen ryhmään. Ryhmä 1 koostui 330 potilaasta, joille tehtiin transhepaattinen perkutaaninen dreeni ja transhepaattinen perkutaaninen aspiraatio, ja ryhmä 2 koostui 330 potilaasta, joille tehtiin endoskooppinen transpapillaarinen sappirakon dreeni. Tulokset analysoitiin toimenpiteen jälkeisinä päivinä 3 ja 7. Päivänä 3 hoidon onnistumisprosentti oli 62,5 % (kolekystostomia) ja 69,8 % (endoskooppinen hoito). Päivänä 7 hoidon onnistumisprosentti oli 87,6 % (kolekystostomia) ja 89,2 % (endoskooppinen hoito). Varhaisessa tai myöhäisessä onnistumisprosentissa ei havaittu merkittäviä eroja. Komplikaatioiden esiintyvyys oli 4,8 % kolekystostomiaryhmässä ja 8,2 % endoskooppisen tyhjennyshoidon ryhmässä, eikä tilastollisessa analyysissä ollut tilastollisia eroja. Kolekystostomiaryhmässä raportoituja komplikaatioita olivat 8 potilasta, joilla katetri oli siirtynyt, yksi potilas, jolla oli verenvuotoa, ja 3 potilasta, joilla oli sappitievuoto. Kyseinen tutkimus osoitti perkutaanisen tyhjennyksen olevan tehokasta, ja sen teho oli sama kuin endoskooppisen hoidon. Vaikka potilaita ei ollut stratifioitu AC:n vaikeusasteen mukaan, kirjoittajat totesivat keskusteluosuudessa, että tutkimuksessa esiintyi todennäköisesti harhaa, koska mukaan oli otettu paljon potilaita, joilla oli vaikea (aste III) ja keskivaikea (aste II) AC.
Hoitosuositukset asteen III AC-tapauksissa olivat TG18:n suurimpia muutoksia TG13:een nähden. Aiemmin ainoa suositus oli sappirakon hätätyhjennys (endoskooppinen tai transhepaattinen),13 mikä osoitti ei-yksiselitteistä taipumusta välttää kiireellistä kirurgista hoitoa, jotta sairastuvuus ja kuolleisuus eivät lisääntyisi. Vaikka TG18 toistaa tämän suosituksen, siihen lisättiin mahdollisuus varhaisen LC:n suorittamiseen sen jälkeen, kun antibioottihoito on aloitettu ja elintoiminnot ovat normalisoituneet.16 Näin ollen AC:n, erityisesti asteen III, diagnosoinnin yhteydessä on olennaisen tärkeää laskea CCI ja ASA-toimintakyky ja tunnistaa, onko potilaalla suotuisia ennustetekijöitä elintoimintojen vajaatoiminnalle (munuais- tai sydän- ja verisuonitauti). Nämä potilaat saattavat toipua nopeasti lääkehoidon aloittamisen jälkeen, jolloin heistä voi tulla ehdokkaita lopulliseen LC-hoitoon.
World Society for Emergency Surgery suosittelee sappirakon perkutaanisen tyhjennyksen suorittamista ”korkean riskin” potilaille, mutta siinä ei anneta tarkkaa määritelmää mainituille potilaille, mikä voi johtaa siihen, että akuutin sappirakon tulehduksen hoitoon osallistuvien eri ammattihenkilöiden päätökset voivat vaihdella toisistaan.17
Huolimatta siitä, että PC:n asettaminen on yleisesti hyväksytty potilaille, joilla on vaikea akuutti sappitulehdus,18,19 ja huolimatta raportoidusta näytöstä suhteellisen alhaisesta kuolleisuusluvusta (17 %),20 paras hoitovaihtoehto on edelleen keskustelun aihe, kun otetaan huomioon, että jotkin ryhmät raportoivat hätätilanteessa suoritetun LC:n hyväksyttävästä lopputuloksesta kriittisesti sairaiden potilaiden kohdalla.21-25
Riski konversiosta laparoskooppisesta kolekystektomiasta avoleikkaukseen
Laparoskooppisen koleksistektomian konversiossa avoimeksi leikkaukseksiOn myös kuvailtu erilaisia tekijöitä, joiden avulla voidaan ennakoida konversiosta LC:n konversiossa avokoleksistektomiassa tapahtuvan konversiossa tapahtuvan käänteisleikkaukseen johtanutta vaaraa.26,27 Jotkut kirjoittajat ehdottavat, että potilaita, joilla on suuri konversiovaara, tulisi pitää ehdokkaina PC:n alustavaan asettamiseen, ja tulehdusprosessin hävittyä heille tulisi tehdä myöhäinen LC (taulukko 4).28,29
Riskitekijät konversiolle avoimeen kolekystektomiaan.
| Lipman ym. (2007)26 | Miehinen sukupuoli (OR 4,06, 95 %:n CI: 2,42-6.82)Leukosytoosi 3.01 (OR 3.01, 95% CI: 1.77-5.13),Hypoalbuminemia (OR 2.90, 95% CI: 1.70-4.96),Perikolekystinen neste (OR 2.36, 95% CI: 1.25-4.47)Diabetes mellitus (OR 1.87, 95% CI: 1.03-3.42)Kohonnut kokonaisbilirubiini (OR 1.85, 95% CI: 1.01-3.39) |
| Kim ym. (2014)27 | Pitkälle edennyt ikä (OR 1.05, 95% CI: 1.008-1.10),Miehinen sukupuoli (OR 5.0, 95% CI: 1.31-19.05),Perikolekystinen neste (OR17.22, 95% CI: 4.36-67.94). |
| Masri ym. (2018)79 | Naissukupuoli (OR 0.09, 95 % CI: 0.03-0.25)Korkea ikä (OR 2.15, 95 % CI: 1.62-2.85)Vatsaontelon leikkaushistoria (OR 4.66, 95 % CI: 1.78-12.17)Historiaan kuuluva keuhkosairaus, esim, COPD (OR 6.03, 95% CI: 1.21-29.97)Seerumin hemoglobiini mg/dl (OR 36.57, 95% CI: 3.16-423.72) |
| Morales Maza ym. (2019)a | Miehinen sukupuoli (OR 1.64, 95 % CI: 0,48-5,58)Sappirakon seinämän halkaisija (OR 1,35, 95 % CI: 1,03-1,76)Pitkälle edennyt ikä (OR 1,02, 95 % CI: 1,00-1,04)Perikolekystinen neste (OR 2,84, 95 % CI: 1,04-7.69) |
Julkaisuvaiheessa.
Ensimmäisen konservatiivisen hoidon, ensin PC:n asettaminen ja sen jälkeen intervalli-LC:n suorittaminen, käyttökelpoisuutta potilailla, joilla on ollut AC:n aiheuttamat oireet, jotka ovat olleet pidempään kuin 72 tuntia jatkuneet, on myös tutkittu. Karakayali ym.30 analysoivat potilasryhmää, jolla AC oli kestänyt yli 72 tuntia ja oireiden eteneminen oli kestänyt 48 tuntia alkuperäisen lääkehoidon jälkeen. Potilaille (n=92) tehtiin ei-sattumanvaraisesti joko PC ja sen jälkeen intervalli-LC tai hätä-LC. Intervalli-LC:n läpikäyneiden ryhmässä oli alhaisempi konversioluku (40 % vs. 19 %; p=0,029), vähemmän intraoperatiivista verenhukkaa (33 % vs. 9 %; p=0,006), lyhyempi sairaalassaoloaika (5,3 vrk vs. 3,0 vrk; p=0,001) ja vähemmän komplikaatioita yleensä (35 % vs. 9 %; p=0,003).
El-Gendi ym. 31. satunnaistivat ryhmän potilaita (n=150), joilla AC:n eteneminen oli kestänyt yli 72 tuntia, hätä-LC:hen vs. PC:hen ja intervalli-LC:hen 6 viikkoa myöhemmin. Heidän analyysinsä osoitti, että PC- ja intervalli-kolekystektomiaryhmässä oli alhaisempi konversiotaajuus (24 % vs. 2,27 %; p
0,001), vähemmän intraoperatiivista verenhukkaa (keskimäärin 41,73 ml vs. 26,33 ml; p=0,008), lyhyempi leikkauksen kesto (87,8 min vs. 38,09 min; p0.001), pienempi osittaisen kolekystektomian osuus (17,3 % vs. 0,0 %; p0,001), lyhyempi sairaalassaoloaika (51,71 h vs. 10,76 h; p0,001) ja vähemmän postoperatiivisia komplikaatioita (26,7 % vs. 2,7 %; p0,001).
Potilaat, joilla on akalkuloottinen AC, ovat toinen mainitsemisen arvoinen ryhmä. He ovat usein kriittisesti sairaita potilaita, joilla on useiden elinten vajaatoiminta, ja heille voidaan antaa PC:tä akuuttien oireiden hoitoon. Potilaille, joilla on merkkejä sappirakon perforaatiosta, gangreenista tai oireiden etenemisestä PC:n asettamisen jälkeen, on kuitenkin tehtävä kiireellinen kolekystektomia.32
Perkutaanisen kolekystostomian asettamisen vasta-aiheet
PC:lle ei ole ehdottomia vasta-aiheita. Suhteellisia vasta-aiheita on vähän, ja niihin kuuluvat hyytymishäiriöt, jotka aiheuttavat vakavan verenvuodon riskin (verihiutaleet
×109/l tai INR>1.5), allergia jodioidulle kontrastiaineelle (käytetään katetrin asianmukaisen sijoittamisen varmistamiseen läpivalaisun avulla (vaikka se voitaisiin tehdä ultraäänellä),33 ja suolen segmenttien päällekkäisyys punktiokohdassa (erittäin harvinaista, koska maksa estää segmenttien päällekkäisyyden).34
Paracentesia suositellaan potilaille, joilla on askites, ennen PC:n asettamista. On korostettava, että PC-komplikaatioiden esiintymistiheys potilailla, joilla on askites, on alhainen eikä poikkea merkittävästi potilaista, joilla ei ole askitesia. Sappirakko, joka on tiiviisti täynnä sappikiviä, voi myös vaikeuttaa PC-katetrin turvallista asettamista.35
Väheneekö kuolleisuus perkutaanisen kolekystostomian asettamisen yhteydessä ”korkean riskin” potilailla?
Kerrottuaan olemassa olevasta todistusaineistosta, joka koskee kuolleisuuden vähenemistä korkean riskin potilailla, joilla on akuutti kolekystostomia ja joille on suoritettu PC:n asettaminen, eräässä vuonna 2014 tehdyssä tutkimuksessa analysoitiin Kalifornian terveydenhoitojärjestelmän tietokantaa. Sen ensisijaisena tavoitteena oli määrittää kuolleisuus ja sen ajallinen vaihtelu kolmessa AC-potilasryhmässä: niissä, joille tehtiin PC:n asettaminen, niissä, joille tehtiin LC, ja niissä, joille ei tehty kumpaakaan näistä kahdesta strategiasta tilan vakavuuden vuoksi.36 Yhteensä tutkittiin 43 341 potilasta, ja tulokseksi saatiin 61,7 prosentin kuolleisuus PC:llä hoidetuilla potilailla, 42 prosentin kuolleisuus potilailla, joille ei tehty invasiivista hoitoa, ja 23 prosentin kuolleisuus LC:llä hoidetuilla potilailla. Vakavaa sepsistä ja septistä sokkia sairastavien potilaiden eloonjäämisessä ei ollut eroa PC-ryhmää ja ei-interventioryhmää verrattaessa (p=0,256), ja LC:n läpikäyneiden potilaiden eloonjääminen oli parempi (p
0,001). Vaikka kuolleisuus oli suurempi PC:n läpikäyneillä potilailla, heillä oli korkeampi CCI (5 vs. 3,8) verrattuna LC:n läpikäyneisiin potilaisiin. Näin ollen nämä tutkimuksen rajoitukset on otettava huomioon tuloksia tulkittaessa ja johtopäätöksiä tehtäessä. Toisessa vuonna 2014 julkaistussa tutkimuksessa ei pystytty osoittamaan PC:llä hoidettujen potilaiden vähentynyttä sairastuvuutta ja kuolleisuutta37 , mutta on mainittava, että PC:n hoitoprotokolla oli heterogeeninen ja vaihteli eri keskusten välillä, mikä saattoi osaltaan vaikuttaa tulosten vaihtelevuuteen.
CHOCOLATE-protokolla julkaistiin vuonna 2012 tarkoituksenaan antaa vakuuttavampi vastaus PC-keskusteluun. Se oli monikeskuksinen, satunnaistettu, kontrolloitu tutkimus intervention paremmuudesta. Siinä pyrittiin vertailemaan LC:n suorittamisen ja PC:n asettamisen välistä tulosta AC-potilailla, joiden APACHE-pisteet olivat >7 pistettä. Tutkimukseen rekrytoitiin 284 potilasta kahden vuoden aikana 30 suuren volyymin keskuksessa. Ensisijaisena tavoitteena oli analysoida komplikaatioita kolmen ensimmäisen kuukauden aikana toimenpiteen jälkeen ja kuolleisuutta vuoden kuluttua (Netherlands Trial Register ; NTR2666).38 Tutkimusprotokollan tuloksia ei julkaistu, koska se keskeytettiin vuonna 2016 sen jälkeen, kun alustava analyysi osoitti suurempaa sairastuvuutta ja kuolleisuutta PC:llä hoidetuilla potilailla.
Nämä tutkimukset asettavat kyseenalaiseksi PC:n todellisen hyödyn vakavaa AC:tä sairastaville potilaille. Siihen liittyy kuitenkin paljon kiistanalaisuutta, koska satunnaistettuja tutkimuksia tarvitaan, jotta valintaharha voidaan eliminoida. Suurin osa tällä hetkellä saatavilla olevasta todistusaineistosta on retrospektiivistä ja sisältää suuren määrän potilaita, jotka ovat ”niin vaikeita”, että heidän kuolleisuutensa on korkea tarjotusta toimenpiteestä riippumatta.
On tärkeää korostaa, että potilaat, jotka eivät ole korkean riskin potilaita, joilla ei ole liitännäissairauksia ja jotka ovat LC-ehdokkaita, eivät hyödy PC:n asettamisesta lainkaan. Joidenkin tutkimusten mukaan lopputulos voi jopa huonontua kyseistä strategiaa käytettäessä.39,40 Kokemuksemme mukaan emme pidä suositeltavana laparoskooppisen kolekystostomian suorittamista pelastusmenetelmänä epäonnistuneen LC:n jälkeen, koska siinä skenaariossa on suositeltavampaa suorittaa subtotaalinen kolekystektomia, jos toimenpiteen aikana ilmenee teknisiä ongelmia. Tutkimuksissa, joissa on verrattu PC:tä avoimeen kolekystektomiaan kriittisesti sairailla potilailla, joilla on akalkulaarinen kolekystiitti, on havaittu vähemmän sairastuvuutta, vähemmän sairaalassaolopäiviä ja alhaisemmat liitännäiskustannukset potilailla, joille on tehty PC:n sijoittaminen.41
Ultraääniohjatun perkutaanisen kolekystostomian sijoittamistekniikan kuvaus
Kun PC:n tekemisestä on päätetty, on ensiksi määriteltävä lähestymistapa, jota käytetään tyhjennyksen sijoittamiseen, onko se sitten transmaksiaalinen vai transperitoneaalinen. Kustakin potilaasta ja kirurgista riippuen voidaan valita jompikumpi lähestymistapa, jolla kummallakin on etunsa ja haittansa.
Potilaille, joilla on suurempi verenvuotoriski, on perinteisesti kuvattu transperitoneaalinen lähestymistapa maksan puhkeamisen estämiseksi. Toisaalta transhepaattista lähestymistapaa suositaan potilailla, joiden sappirakko on hyvin laajentunut (> 10 cm pitkällä akselilla tai > 5 cm aksiaalisella akselilla), jotta voidaan pienentää perforaation ja sappitievuodon sekä sappiperitoniitin riskiä.
Toinen tärkeä huomioon otettava seikka on potilaan habitus ja liikuntakyky, koska se voi haitata jompaakumpaa lähestymistapaa sappirakon huonon näkyvyyden tai sappirakon tavoittamisen vaikeuden vuoksi monimutkaisen sappitien vuoksi. Kun kaikki edellä mainitut näkökohdat on analysoitu, voidaan valita sopivin lähestymistapa.
Kokemuksemme mukaan PC on yleensä toimenpide, joka tehdään potilaan vuodeosastolla trokari-tekniikalla, vaikka perinteisesti on kuvattu modifioitu Seldinger-tekniikka. Tekninen onnistumisprosenttimme on samankaltainen kuin kirjallisuudessa raportoitu onnistumisprosentti (tiedot julkaistaan myöhemmin).
Vaihe vaiheelta etenevä tekniikka, jota käytetään ultraääniohjattuun PC:n asettamiseen, on kuvattu alla (kuva 1).
- 1
Toteuta asianmukainen aseptiikka ja antiseptiikka oikean hypokondriumin alueella.
- 2
Tarkista sappirakko ultraäänellä AC-diagnoosin vahvistamiseksi.
- 3
Infiltroi iho ja ihonalainen solukudos 2 % lidokaiinilla.
- 4
Varmennetaan katetrin asettamiseen tarvittavan materiaalin läsnäolo valitulla tekniikalla.
- 5
Löydetään sappirakko ultraäänitutkimuksella. Suorita transperitoneaalinen tai transhepaattinen punktio. Vie sitten monikäyttökatetri (8,5 Fr) sappiteiden läpi metallisen ohjauslangan yli ja työnnä sitä eteenpäin, kunnes se on sijoitettu sappirakkoon (kuva 2).
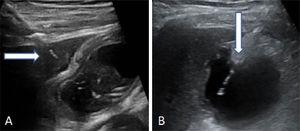 Kuva 2. Sappirakon punktio.
Kuva 2. Sappirakon punktio.Kaksi tapaa suorittaa sappirakon punktio. (A) Neulan transhepaattinen sisäänmeno. Nuoli osoittaa maksakupoliin. (B) Neulan transperitoneaalinen sisääntulo suoraan sappirakon fundukseen.
(0.25MB).- 6
Vetäkää metallinen ohjauslanka ulos, jolloin katetri jää sappirakon sisälle.
- 7
Kiinnittäkää katetri ihoon 3:lla.0 prolene-ompeleella.
- 8
Extraktoi sappineste, joka lähetetään mikrobiologian laboratorioon viljelyä varten.
- 9
Aseta keräyspussi katetrin distaaliseen päähän jättäen diversio.
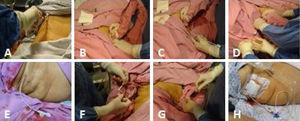 Kuva 1.
Kuva 1.(A) Oikean hypokondriumin aseptiikka. (B) Sappirakon tähystys. (C) Katetrin tuominen ultraääniohjatusti yhdessä metallisen ohjauslangan kanssa sappirakon suuntaan. (D) Metallinen ohjauslanka vedetään ulos siten, että katetri jätetään paikoilleen sappirakon luumeniin päin, ja sen asianmukainen sijainti sappirakon sisällä varmistetaan jälleen kerran ultraäänellä. (E) Paikallaan oleva kolekystostomiakatetri. (F) Katetri kiinnitetään yksinkertaisella ompeleella ihoon prolene 3-0:lla. (G) Sappineste imetään ja lähetetään viljelyä varten. (H) Diversion kolekystostomiakatetri keräyspussin kanssa.
(0.2MB).Perkutaanisen kolekystostomian komplikaatiot
PC:n asentamista pidetään yleisesti turvallisena ja tehokkaana toimenpiteenä. Yli 90 %:lla potilaista kivun ja systeemisen tulehdusvasteen odotetaan paranevan ensimmäisten 48 tunnin kuluessa PC:n asettamisesta.42 Komplikaatioita on kuitenkin kuvattu noin 3 %:ssa tapauksista. Yleisimpiä komplikaatioita ovat hemobilia, pneumothorax, sappitievuoto, sappitieperitoniitti, koledokolitiaasi ja abskessit.43,44 Katetrin ulostyöntyminen on aina riski, mikä voi vaikeuttaa sen uudelleen asettamista, kun sappirakko on dekompressioitu.45,46
AC:n uusiutumisriski PC:n poiston jälkeen vaihtelee 6-40 %:n välillä.47-49 AC:n uusiutumista on raportoitu jopa potilailla, joilla on toimiva ja läpäisevä katetri, ja se tapahtuu yleensä kahden ensimmäisen kuukauden aikana sen asettamisesta.50 Joissakin tapausselostuksissa on raportoitu PC:n saaneiden potilaiden pidemmästä sairaalassaoloajasta.51 Pidempi sairaalassaoloaika liittyy todennäköisesti PC:n saaneiden potilaiden vaikeusasteen kasvuun eikä ole suoranainen seuraus toimenpiteestä.52 PC:n oikea-aikainen asettaminen, mikä tarkoittaa sitä, että se tehdään ensimmäisten 24 tunnin kuluessa oireiden alkamisesta, lyhentää tehokkaasti sairaalassaoloaikaa. Tämä dokumentoitiin vuonna 2015 tehdyssä tutkimuksessa, jossa vain potilailla, joille PC asetettiin myöhään, oli pidempi sairaalassaoloaika.53
Milloin kolekystostomiakatetri poistetaan
Yleensä PC olisi poistettava, kun potilaan tila on vakaa ja akuutti oirekuva on laantunut. Ihanteellista poistoajankohtaa ei kuitenkaan ole tarkasti määritelty.54 PC:n kautta suoritettua kolangiografiaa on tehty kystisen kanavan läpäisevyyden arvioimiseksi. Potilailla, joilla on läpäisevä kystinen kanava, on raportoitu alhaisempi AC:n uusiutumisaste55 , mutta tiedot ovat ristiriitaisia. AC:n uusiutumista voi esiintyä joissakin tapauksissa, vaikka kolangiografia dokumentoisi sappiteiden läpäisevyyden.56
Vuonna 2017 julkaistussa retrospektiivisessä kohorttitutkimuksessa arvioitiin kahta ryhmää. Ryhmässä 1 (n=43) tehtiin rutiininomainen kolangiografia ennen kolekystostomian poistoa, ja ryhmässä 2 tehtiin vain tilauskolangiografia (n=41). Potilailla, joille tehtiin on-demand-kolangiografia, oli parempi lopputulos, koska heillä poistettiin tyhjennys aikaisemmin, kolekystektomian varhaisvaiheen osuus oli korkeampi ja resursseja käytettiin vähemmän.57
LK:n suorittamisen yhteydessä lopullisena hoitona on noudatettava erityistä varovaisuutta, koska vaikka sappirakon tulehdus on vähentynyt tai hävinnyt, potilaan liitännäissairaudet ovat yleensä edelleen olemassa, mikä tarkoittaa sitä, että leikkaus voi olla monimutkaisempi kuin alun perin harkittiin.58,59,59 Tässä tilanteessa avoleikkaukseen siirtymisen on raportoitu olevan 11-32 prosenttia.60-63 Intervallinen kolekystektomia tehdään yleensä ilman teknisiä ongelmia nuorille potilaille, joilla ei ole liitännäissairauksia.64,65,65
Päätehoito
Kolekystostomian asettaminen on ihanteellisesti siirtymähoito ennen lopullista hoitoa, joka suoritetaan, kun potilaan yleistila on parantunut.66,67 Yli 95 prosentilla potilaista kolekystektomia on lopullinen hoito,68 mutta kolekystostomian on raportoitu jäävän määrittelemättömäksi ajaksi 30-50 prosentilla potilaista.69-71 Jotkut kirjoittajat suosittelevat PC:n asettamista lopulliseksi ja pysyväksi hoidoksi iäkkäille potilaille ja potilaille, joilla on suuri kirurginen riski.72
Kuvailevassa tutkimuksessa, joka tehtiin vuosina 2000-2011 ja joka koski 36:aa potilasta, joille oli tehty PC:n asettaminen sen vuoksi, että heitä pidettiin ”suuririskisinä” potilaina, kirjoittajat raportoivat 100-prosenttisen oireiden häviämisen 3 päivän kuluttua PC:n asettamisesta kaikilla potilailla. PC oli lopullinen hoito 63 %:lla potilaista, ja lopullinen LC tehtiin vain 6 potilaalle (16 %).73 Toiset kirjoittajat kannattavat LC:n suorittamista saman sairaalahoidon aikana, koska LC:n viivästymiseen liittyy potilaiden menetys seurannassa.74 Toiset tutkimusryhmät ovat yhtä mieltä siitä, että katetriin liittyvien komplikaatioiden esiintymistiheys on suuri, ja suosittelevat PC:n poistamista heti, kun akuutti tulehdusreaktio on saatu hallintaan, jopa ensimmäisten 10 päivän aikana katetrin asettamisesta.75,76
Keskuksemme kokemuksen mukaan kolekystostomia poistetaan, kun potilas on ohjelmoitu kolekystektomiaan seuraavien 2 viikon aikana, ainoana tarkoituksena parantaa potilaan elämänlaatua ennen leikkausta. Katetri poistetaan vain, jos potilas on oireeton, hänellä ei ole merkkejä systeemisestä tulehdusreaktiosta eikä merkkejä läpäisevästä kystisesta kanavasta. Se poistetaan myös potilailta, joille tehdään lopullinen kolekystektomia. Jos nämä kriteerit eivät täyty, kantamme on jättää kolekystostomiakatetri paikoilleen toistaiseksi.
Ehdotamme kuvassa 3 esitettyä algoritmia kolekystostomiakatetrin poistamiseksi.
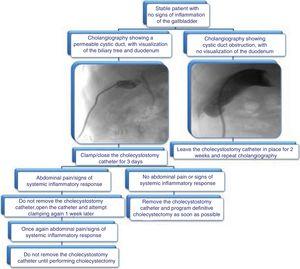 Kuvio 3. Katetrin poiston arviointi.
Kuvio 3. Katetrin poiston arviointi.Ehdotettu algoritmi kolekystostomian katetrien hoitoa varten: poiston arviointi kolangiografian ja kliinisten tietojen avulla.
(0.35MB).On tärkeää korostaa, että potilailla, joille tehdään kolekystostomian poisto ja sen jälkeen nestekiertoontelon poisto (LC), on raportoitu useammin leikkausalueen infektioita. Kyseinen infektio on kuvattu jopa 16 prosentissa tapauksista.77
Johtopäätökset
Sappirakon perkutaaninen dekompressio on laajalti tunnettu hoitomuoto, mutta kolekystostomian katetrin hoitoa varten ei vieläkään ole standardoitua strategiaa, mikä vaikeuttaa näiden potilaiden yhdenmukaista tutkimista tällä hetkellä saatavilla olevan kirjallisuuden avulla. Näytön vähäisyydestä huolimatta voidaan kuitenkin esittää joitakin näkökohtia:
- –
Korkean riskin kirurgiset potilaat, joilla on diagnosoitu AC ja joilla hätätilanteen LC on vasta-aiheinen, näyttävät olevan parhaita ehdokkaita PC:n asettamiseen.
- –
Ei ole näyttöä, joka tukisi PC:n asettamista vakaassa tilassa olevilla potilailla, joilla ei ole vasta-aihetta LC:n suorittamiselle.
- –
PC-katetrin poisto tulisi suorittaa vasta sen jälkeen, kun kystisen kanavan läpäisevyys on dokumentoitu kolangiografian avulla, jos katetri aiheuttaa potilaalle epämukavuutta ja jos potilas on ehdolla lopulliseen kirurgiseen hoitoon ”kohtuullisen” ja sopivan ajan kuluessa, jotta vähennetään mahdollisuutta, että potilaalle ilmaantuu toistuva akuutti kolekystiitti.
Perkutaanisten kolekystostomia-katetrien hoidosta on vain vähän näyttöä, ja tällä hetkellä tarvitaan satunnaistettuja tutkimuksia, joissa arvioidaan parasta strategiaa, jota tässä potilasryhmässä tulisi noudattaa.
Eettiset tiedonantovelvollisuudet
Ihmisten ja eläinten suojelu. Kirjoittajat ilmoittavat, että tätä artikkelia varten ei tehty ihmisillä tai eläimillä kokeita.
Tietojen luottamuksellisuus. Kirjoittajat ilmoittavat, että he ovat käsitelleet kaikkia potilastietoja luottamuksellisesti ja anonyymisti noudattaen työkeskuksensa protokollia.
Oikeus yksityisyyteen ja tietoon perustuva suostumus. Kirjoittajat ilmoittavat, että tässä artikkelissa ei esiinny potilastietoja, jotka vaarantaisivat heidän henkilöllisyytensä, joten heidän tietoon perustuvaa suostumustaan ei tarvinnut hankkia.
Rahoitustietojen ilmoittaminen
Tämän artikkelin laatimiseen ei ole saatu rahallista tukea.
Erityisintressien ristiriita
Kirjoittajat ilmoittavat, ettei eturistiriitoja ole.
Tekijät ilmoittavat, ettei eturistiriitoja ole.
- 6
Leave a Reply