Przezskórna cholecystostomia jako leczenie ostrego zapalenia pęcherzyka żółciowego: Co się wydarzyło w ciągu ostatnich pięciu lat? A literature review | Revista de Gastroenterología de México
Wprowadzenie
Patologia pęcherzyka żółciowego jest jedną z najczęstszych chorób, z którymi styka się chirurg ogólny. Obecnie cholecystektomia laparoskopowa (LC) jest uważana za złoty standard w leczeniu ostrego zapalenia pęcherzyka żółciowego (AC). Podjęto wysiłki w celu zmniejszenia zachorowalności i śmiertelności związanej z zabiegiem u chorych chirurgicznych wysokiego ryzyka poprzez zastosowanie mniej inwazyjnych interwencji, takich jak przezskórna cholecystostomia (PC).
Drenaż pęcherzyka żółciowego jest opcją leczenia uwzględnioną w głównych międzynarodowych wytycznych postępowania w AC, ale nadal istnieją pewne kontrowersje co do jego wyników u krytycznie chorych pacjentów, dokładnych wskazań i wyższości w porównaniu z ostatecznym leczeniem chirurgicznym.
Mało jest danych dotyczących nadzoru i opieki nad pacjentami poddanymi PCa. Większość badań koncentruje się na wyborze pacjentów, którzy odniosą korzyści z zabiegu, ale niewiele z nich opisuje dalsze postępowanie z pacjentem. W niniejszym opracowaniu przeanalizowano dowody dotyczące przydatności PC w AC i zaproponowano algorytm postępowania z cewnikiem PC.
Kryteria klasyfikacji ciężkości ostrego zapalenia pęcherzyka żółciowego
Wytyczne tokijskie z 2018 roku (TG18) dotyczące AC klasyfikują ciężkość choroby jako łagodną (stopień I), umiarkowaną (stopień II) i ciężką (stopień III).1 Klasyfikacja ta uwzględnia choroby współistniejące u pacjenta, czas trwania objawów, wyniki badań przedmiotowych przy przyjęciu do szpitala, objawy ogólnoustrojowej odpowiedzi zapalnej, obecność wyraźnego miejscowego stanu zapalnego w badaniach obrazowych oraz rozwój dysfunkcji narządów. Klasyfikacja TG jest przydatna, ponieważ ciężkość prezentacji choroby koreluje ze śmiertelnością, zachorowalnością, długością pobytu w szpitalu i wskaźnikiem konwersji z operacji laparoskopowej na operację otwartą (tabele 1 i 2).
Klasyfikacja ciężkości ostrego zapalenia pęcherzyka żółciowego według wytycznych tokijskich z 2018 r.1.
| Stopień I (łagodny) | Stopień II (umiarkowany) | Stopień III (ciężki) |
|---|---|---|
|
Każdy z następujących stanów:
|
Każde z następujących zaburzeń czynności narządów:
|
Charakterystyka poszczególnych stopni ciężkości.
| Śmiertelność w ciągu 30 dni2 | Zachorowalność78 | Pobyt w szpitalu78,a | Współczynnik konwersji78,a | |
|---|---|---|---|---|
| Stopień I | 1.1% | 2,9% | 3 (1-16) | 7% |
| Grad II | 0.8% | 3,1% | 4 (1-33) | 25,6% |
| Grad III | 5,4% | 11.1% | 7 (1-60) | 34,6% |
Mean±SD.
Wczesne LC (w ciągu 72 h) powinno być idealnie wykonane w przypadkach AC w stopniu I i II, jeśli wskaźnik współchorobowości Charlsona (CCI) i wydolność funkcjonalna zgodnie z systemem klasyfikacji Amerykańskiego Towarzystwa Anestezjologów (ASA) sugerują, że pacjent może tolerować operację. W przeciwnym razie należy ustalić wstępne leczenie farmakologiczne (antybiotyki i wsparcie ogólne) i rozważyć leczenie chirurgiczne po uzyskaniu poprawy stanu zdrowia. W II stopniu AC dodaje się zalecenie wykonania drenażu przezskórnego, gdy pacjent nie toleruje leczenia chirurgicznego.1
Wytyczne tokijskie z 2013 roku (TG13) klasyfikują AC jako stopień III, gdy istnieją dowody na dysfunkcję narządową, definiując ją w przypadku niewydolności sercowo-naczyniowej, neurologicznej, oddechowej, nerkowej, wątrobowej lub hematologicznej. Według TG13 w przypadku dysfunkcji tych układów narządowych przeciwwskazane jest wykonanie LC w trybie nagłym. W 2017 roku Yokoe i wsp.2 przedstawili jednak informacje na temat leczenia AC w populacji japońskiej i tajwańskiej (n=5 329), w której LC wykonano z powodzeniem u większości pacjentów z AC w stopniu III. Tę samą kohortę poddano później ponownej analizie, kładąc nacisk na tych chorych z dysfunkcją narządową, u których można bezpiecznie przeprowadzić leczenie chirurgiczne. Chorzy z CCI>6 punktów charakteryzowali się wyższym wskaźnikiem śmiertelności. Główną użytecznością tego badania była wieloczynnikowa analiza regresji logistycznej, która wykazała, że żółtaczka, dysfunkcja neurologiczna i dysfunkcja układu oddechowego były niezależnymi czynnikami predykcyjnymi śmiertelności w ciągu 30 dni u pacjentów z III stopniem AC. Nie było jednak dowodów na zwiększoną śmiertelność wśród pacjentów z AC w stopniu III, u których występowały inne rodzaje niewydolności narządowej i którzy byli poddani LC.3 Tak więc TG18 definiuje dysfunkcję neurologiczną, dysfunkcję układu oddechowego lub obecność żółtaczki (stężenie bilirubiny całkowitej ≥ 2mg/dl) jako czynniki predykcyjne śmiertelności w AC w stopniu III. Z drugiej strony, dysfunkcja nerek i dysfunkcja układu krążenia są uważane za korzystne rodzaje niewydolności narządowej, biorąc pod uwagę, że często mogą być odwrócone po wdrożeniu wstępnego leczenia medycznego, a w konsekwencji nie stanowią przeciwwskazania do leczenia chirurgicznego.1
Wskazania do przezskórnego założenia cholecystostomii
Ogólnie rzecz biorąc, najczęstszym wskazaniem do założenia PC jest ciężka AC.4-Mniej powszechne wskazania to te, których celem jest odwrócenie kierunku dróg żółciowych za pomocą dostępu przezcholecystycznego, który w większości przypadków jest uważany za względnie drugorzędowy ze względu na preferencje do wykonywania dywersji endoskopowych lub przezwątrobowych. Scenariusze te podsumowano w tabeli 3.10-13
Wskazania do przezskórnego założenia cholecystostomii.
Ciężkie ostre zapalenie pęcherzyka żółciowego wg Wytycznych Tokijskich 2018
Ostre zapalenie pęcherzyka żółciowego i klasyfikacja ASA >3 lub wskaźnik współchorobowości Charlsona >6
Dostęp drugiego rzutu do dróg żółciowych:Pomostowanie złośliwej zmiany w drogach żółciowychDoprowadzenie do zwężenia przewodu żółciowegoOdwrócenie wyjścia przetoki przewodu żółciowegoDekompresja dróg żółciowych w zapaleniu dróg żółciowychInne
W przeciwieństwie do tego, co ustalono w TG13,14 TG18 podkreślają fakt, że doraźny drenaż pęcherzyka żółciowego może być przeprowadzony w II stopniu AC, gdy laparoskopia nie jest dostępna i występuje nieodpowiednia odpowiedź na początkowe leczenie medyczne, głównie u pacjentów, którzy prezentują „zły” stan ogólny (CCI>6 punktów lub klasyfikacja ASA >3). Sugestię tę potwierdza wieloośrodkowe badanie retrospektywne15 z 2017 r., które objęło 1764 pacjentów w okresie 2 lat, ale dla porównania sparowano 330 pacjentów na dwie grupy. Grupa 1 składała się z 330 pacjentów, u których wykonano przezskórny drenaż przezwątrobowy i przezskórną aspirację, a grupa 2 składała się z 330 pacjentów, u których wykonano endoskopowy transpapilarny drenaż pęcherzyka żółciowego. Wyniki analizowano w 3 i 7 dobie po zabiegu. W 3. dobie odsetek powodzenia terapeutycznego wynosił 62,5% (cholecystostomia) i 69,8% (leczenie endoskopowe). W 7. dobie odsetek powodzeń terapeutycznych wynosił 87,6% (cholecystostomia) i 89,2% (leczenie endoskopowe). Nie stwierdzono istotnych różnic w zakresie wczesnych i późnych wskaźników powodzenia. Częstość powikłań wynosiła 4,8% w grupie cholecystostomii i 8,2% w grupie drenażu endoskopowego i nie było różnic w analizie statystycznej. Powikłania odnotowane w grupie cholecystostomii to 8 pacjentów z migracją cewnika, jeden pacjent z krwawieniem i 3 pacjentów z przeciekiem żółci. Badanie to wykazało, że drenaż przezskórny jest skuteczny i ma taką samą skuteczność jak postępowanie endoskopowe. Mimo że pacjenci nie byli stratyfikowani w zależności od stopnia zaawansowania AC, autorzy stwierdzili w części dyskusyjnej, że w badaniu najprawdopodobniej wystąpiła stronniczość ze względu na włączenie dużej liczby pacjentów z ciężkim (stopień III) i umiarkowanym (stopień II) AC.
Zalecenia dotyczące leczenia w przypadku AC stopnia III były jednymi z największych zmian w TG18 w stosunku do TG13. Poprzednio jedynym zaleceniem był doraźny drenaż pęcherzyka żółciowego (endoskopowy lub przezwątrobowy),13 co wskazywało na niewyraźną tendencję do unikania doraźnego leczenia chirurgicznego, aby nie zwiększać zachorowalności i śmiertelności. Mimo że TG18 powtórzyła to zalecenie, dodano możliwość wykonania wczesnej LC, po ustaleniu antybiotykoterapii i normalizacji funkcji narządów.16 Dlatego po rozpoznaniu AC, zwłaszcza stopnia III, istotne jest obliczenie wskaźnika CCI i wydolności czynnościowej wg ASA oraz ustalenie, czy u pacjenta występują korzystne czynniki prognostyczne niewydolności narządowej (uszkodzenie nerek lub układu sercowo-naczyniowego). Chorzy ci mogą szybko wracać do zdrowia po rozpoczęciu leczenia farmakologicznego, stając się kandydatami do ostatecznego leczenia za pomocą LC.
Światowe Towarzystwo Chirurgii Ratunkowej zaleca wykonywanie przezskórnego drenażu pęcherzyka żółciowego u chorych „wysokiego ryzyka”, ale nie podaje dokładnej definicji tych chorych, co może powodować podejmowanie różnych decyzji przez różnych specjalistów zajmujących się leczeniem ostrego zapalenia pęcherzyka żółciowego.17
Pomimo powszechnej akceptacji umieszczania PC u chorych z ciężkim AC,18,19 i przedstawionych dowodów na stosunkowo małą śmiertelność (17%),20 najlepsza opcja leczenia jest nadal przedmiotem debaty, biorąc pod uwagę, że niektóre grupy donoszą o akceptowalnych wynikach stosowania LC w trybie nagłym u krytycznie chorych pacjentów.21-25
Ryzyko konwersji z cholecystektomii laparoskopowej do operacji otwartej
Opisano również różne czynniki pozwalające przewidzieć ryzyko konwersji z LC do otwartej cholecystektomii.26,27 Niektórzy autorzy proponują, aby chorych z wysokim ryzykiem konwersji uznać za kandydatów do pierwotnego założenia PC, a po ustąpieniu procesu zapalnego poddać późnej LC (tab. 4).28,29
| Lipman i wsp. (2007)26 | Płeć męska (OR 4,06, 95% CI: 2,42-6.82)Leukocytoza 3,01 (OR 3,01, 95% CI: 1,77-5,13),Hipoalbuminemia (OR 2,90, 95% CI: 1,70-4,96),Płyn okołopęcherzykowy (OR 2,36, 95% CI: 1,25-4,47)Cukrzyca (OR 1,87, 95% CI: 1,03-3,42)Podwyższona bilirubina całkowita (OR 1.85, 95% CI: 1.01-3.39) |
| Kim i wsp. (2014)27 | Podwyższony wiek (OR 1.05, 95% CI: 1.008-1.10),Płeć męska (OR 5.0, 95% CI: 1.31-19.05),Płyn okołopęcherzykowy (OR17.22, 95% CI: 4.36-67.94). |
| Masri i wsp. (2018)79 | Płeć żeńska (OR 0,09, 95% CI: 0,03-0,25)Zaawansowany wiek (OR 2,15, 95% CI: 1,62-2,85)Historia operacji w obrębie jamy brzusznej (OR 4,66, 95% CI: 1,78-12,17)Historia choroby płuc, np, POChP (OR 6,03, 95% CI: 1,21-29,97)Hemoglobina w surowicy mg/dl (OR 36,57, 95% CI: 3,16-423,72) |
| Morales Maza i wsp. (2019)a | Płeć męska (OR 1.64, 95% CI: 0,48-5,58)Średnica ściany pęcherzyka żółciowego (OR 1,35, 95% CI: 1,03-1,76)Zaawansowany wiek (OR 1,02, 95% CI: 1,00-1,04)Płyn okołopęcherzykowy (OR 2,84, 95% CI: 1,04-7.69) |
W trakcie publikacji.
Badano również przydatność wstępnego leczenia zachowawczego, polegającego najpierw na założeniu PC, a następnie wykonaniu interwałowej LC u chorych z objawami AC o progresji powyżej 72 h. Karakayali i wsp.30 analizowali grupę chorych z AC trwającym ponad 72 h i progresją objawów do 48 h po wstępnym leczeniu zachowawczym. Pacjentów (n=92) przydzielono w sposób nielosowy do poddania się PC, a następnie interwałowej LC lub do poddania się LC w trybie nagłym. Grupa poddana interwencyjnej LC miała niższy odsetek konwersji (40% vs. 19%; p=0,029), mniejszą śródoperacyjną utratę krwi (33% vs. 9%; p=0,006), krótszy pobyt w szpitalu (5,3 dnia vs. 3,0; p=0,001) i ogólnie mniejszą częstość powikłań (35% vs. 9%; p=0,003).
El-Gendi i wsp.31 randomizowali grupę chorych (n=150) z AC o progresji powyżej 72 h do poddania się LC w trybie nagłym vs. PC i interwałowej LC 6 tygodni później. Ich analiza wykazała, że grupa PC i cholecystektomii interwałowej miała mniejszą częstość konwersji (24% vs. 2,27%; p
0,001), mniejszą śródoperacyjną utratę krwi (średnio 41,73ml vs. 26,33ml; p=0,008), krótszy czas trwania operacji (87,8min vs. 38,09min; p0.001), mniejszy odsetek cholecystektomii subtotalnej (17,3% vs. 0,0%; p0,001), krótszy czas pobytu w szpitalu (51,71h vs. 10,76h; p0,001) oraz mniejszą liczbę powikłań pooperacyjnych (odpowiednio 26,7% vs. 2,7% p0,001).
Kolejną grupą, o której warto wspomnieć są pacjenci z akalkulicznym AC. Często są to chorzy w stanie krytycznym, z niewydolnością wielonarządową i są kandydatami do PC jako wstępnego leczenia z wyboru w celu ustąpienia ostrych objawów. Jednak pacjenci z objawami perforacji pęcherzyka żółciowego, zgorzeli lub progresji objawów po założeniu PC powinni być poddani cholecystektomii w trybie nagłym.32
Przeciwwskazania do przezskórnego założenia cholecystostomii
Nie ma bezwzględnych przeciwwskazań do PC. Przeciwwskazania względne są nieliczne i należą do nich koagulopatia warunkująca ryzyko poważnego krwawienia (płytki krwi
×109/l lub INR>1.5), uczulenie na jodowany środek kontrastowy (konieczne jest potwierdzenie odpowiedniego położenia cewnika za pomocą fluoroskopii (choć można to zrobić za pomocą ultrasonografii),33 oraz nakładanie się segmentów jelita w miejscu wkłucia (niezwykle rzadkie, ponieważ wątroba utrudnia nakładanie się segmentów).34
Paracenteza jest sugerowana u chorych z wodobrzuszem, przed założeniem PC. Należy podkreślić, że częstość powikłań PC u chorych z wodobrzuszem jest mała i nie różni się istotnie w porównaniu z chorymi, u których nie występuje wodobrzusze. Pęcherzyk żółciowy ciasno wypełniony kamieniami żółciowymi może również utrudniać bezpieczne umieszczenie cewnika PC.35
Czy istnieje zmniejszenie śmiertelności przy przezskórnym założeniu cholecystostomii u pacjentów „wysokiego ryzyka”?
Dokładnie opisując istniejące dowody na zmniejszenie śmiertelności u pacjentów wysokiego ryzyka z AC poddawanych PC, w badaniu z 2014 roku przeanalizowano bazę danych California Health System. Jego głównym celem było określenie śmiertelności i jej czasowości w 3 grupach chorych z AC: tych, u których wykonano zabieg wszczepienia PC, tych, u których wykonano LC, oraz tych, u których nie zastosowano żadnej z tych dwóch strategii ze względu na ciężkość ich stanu.36 Łącznie przebadano 43 341 chorych, uzyskując śmiertelność 61,7% u chorych leczonych PC, 42% u chorych, u których nie zastosowano leczenia inwazyjnego, i 23% u chorych, u których wykonano LC. Nie stwierdzono różnicy w przeżywalności chorych z ciężką sepsą i wstrząsem septycznym podczas porównania grupy leczonej PC i grupy bez interwencji (p=0,256), natomiast większą przeżywalność odnotowano u chorych poddanych LC (p
0,001). Mimo że śmiertelność była większa u chorych poddanych PC, mieli oni wyższy wskaźnik CCI (5 versus 3,8) w porównaniu z chorymi poddanymi LC. Tak więc te ograniczenia badania muszą być brane pod uwagę przy interpretacji wyników i wyciąganiu wniosków. W innym badaniu opublikowanym w 2014 roku nie udało się wykazać zmniejszonej chorobowości i śmiertelności u chorych, u których zastosowano PC,37 ale należy wspomnieć, że protokół postępowania w przypadku PC był niejednorodny i różnił się między ośrodkami, co mogło częściowo przyczynić się do zmienności wyników.
Protokół CHOCOLATE opublikowano w 2012 roku z zamiarem udzielenia bardziej rozstrzygającej odpowiedzi na debatę dotyczącą PC. Było to wieloośrodkowe, randomizowane, kontrolowane badanie dotyczące wyższości interwencji. Podjęto w nim próbę porównania wyników pomiędzy wykonaniem LC i PC u pacjentów z AC, którzy mieli wynik w skali APACHE >7 punktów. Do badania zrekrutowano 284 pacjentów w ciągu 2 lat, w 30 ośrodkach o dużej liczbie pacjentów. Podstawowym celem była analiza powikłań w ciągu pierwszych 3 miesięcy po interwencji oraz śmiertelności w ciągu roku (Netherlands Trial Register ; NTR2666).38 Wyników protokołu nie opublikowano, biorąc pod uwagę, że został on zawieszony w 2016 roku, po tym jak wstępna analiza wykazała większą chorobowość i śmiertelność u chorych leczonych za pomocą PC.
Badania te stawiają pod znakiem zapytania rzeczywistą przydatność PC u chorych z ciężką AC. Istnieje jednak wiele kontrowersji wokół tego badania, biorąc pod uwagę, że potrzebne są badania z randomizacją, aby można było wyeliminować błąd selekcji. Większość obecnie dostępnych dowodów ma charakter retrospektywny i obejmuje dużą liczbę pacjentów, którzy są „tak poważni”, że mają wysoki wskaźnik śmiertelności, niezależnie od oferowanej interwencji.
Należy podkreślić, że pacjenci, którzy nie należą do grupy wysokiego ryzyka, nie mają chorób współistniejących i są kandydatami do LC, nie odnoszą żadnych korzyści z umieszczenia PC. Niektóre badania sugerują, że wynik leczenia może się nawet pogorszyć przy zastosowaniu tej strategii.39,40 Z naszego doświadczenia wynika, że nie uważamy za wskazane wykonywanie cholecystostomii laparoskopowej jako metody ratunkowej po nieudanej LC, ponieważ bardziej zalecane jest wykonanie cholecystektomii subtotalnej w takim scenariuszu, jeśli wystąpiły trudności techniczne podczas zabiegu. W badaniach, w których porównywano PC z otwartą cholecystektomią u krytycznie chorych pacjentów z akalkularnym zapaleniem pęcherzyka żółciowego, zaobserwowano mniejszą chorobowość, mniejszą liczbę dni pobytu w szpitalu i niższe koszty związane z zabiegiem u pacjentów, u których wykonano PC.41
Opis techniki ultrasonograficznego zakładania przezskórnej cholecystostomii
Po podjęciu decyzji o wykonaniu PC należy najpierw określić sposób umieszczenia drenu – przezwątrobowy lub przezotrzewnowy. W zależności od każdego pacjenta i każdego chirurga można wybrać jedno lub drugie podejście, każde z nich ma swoje zalety i wady.
W przypadku pacjentów z większym ryzykiem krwawienia tradycyjnie opisuje się podejście przezotrzewnowe, aby zapobiec nakłuciu wątroby. Z drugiej strony, podejście przezwątrobowe jest preferowane u pacjentów, których pęcherzyk żółciowy jest bardzo rozdęty (> 10 cm w osi długiej lub > 5 cm w osi osi osiowej), aby zmniejszyć ryzyko perforacji i wycieku żółci, a także żółciowego zapalenia otrzewnej.
Innym ważnym aspektem, który należy wziąć pod uwagę, jest postura pacjenta i jego zdolność do poruszania się, ponieważ może to utrudniać jedno lub drugie podejście z powodu złej wizualizacji pęcherzyka żółciowego lub trudności w dotarciu do niego z powodu skomplikowanego przebiegu. Po przeanalizowaniu wszystkich wyżej wymienionych aspektów można wybrać najbardziej odpowiednie podejście.
W naszym doświadczeniu PC jest zwykle zabiegiem wykonywanym przy łóżku chorego techniką trokarową, aczkolwiek tradycyjnie opisywana jest zmodyfikowana technika Seldingera. Nasz odsetek powodzeń technicznych jest podobny do opisywanego w piśmiennictwie (dane do opublikowania).
Poniżej opisano technikę zakładania PC krok po kroku pod kontrolą USG (ryc. 1).
- 1
Wykonaj odpowiednią jałowość i antyseptykę w okolicy prawego podżebrza.
- 2
Skanować pęcherzyk żółciowy za pomocą ultrasonografii w celu potwierdzenia rozpoznania AC.
- 3
Infiltrować skórę i podskórną tkankę komórkową 2% lidokainą.
- 4
Potwierdzić obecność materiału niezbędnego do założenia cewnika wybraną techniką.
- 5
Zlokalizować pęcherzyk żółciowy za pomocą badania ultrasonograficznego. Wykonać nakłucie przezotrzewnowe lub przezwątrobowe. Następnie wprowadzamy i przesuwamy cewnik wielozadaniowy przez drogi żółciowe (8,5 Fr) po metalowym prowadniku aż do umieszczenia go w pęcherzyku żółciowym (Ryc. 2).
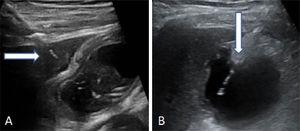 Ryc. 2.
Ryc. 2.Dwa sposoby wykonania nakłucia pęcherzyka żółciowego. (A) Przezwątrobowe wprowadzenie igły. Strzałka wskazuje na kopułę wątrobową. (B) Transperitonealne wprowadzenie igły bezpośrednio do dna pęcherzyka żółciowego.
(0.25MB).- 6
Wyciągnąć metalowy prowadnik, pozostawiając cewnik umieszczony wewnątrz pęcherzyka żółciowego.
- 7
Przymocować cewnik do skóry za pomocą szwu prolenowego 3.0 szwem prolenowym.
- 8
Wydzielić płyn żółciowy, który zostanie przesłany do laboratorium mikrobiologicznego w celu wykonania posiewu.
- 9
Założyć worek zbierający na dystalnym końcu cewnika, pozostawiając dywersję.
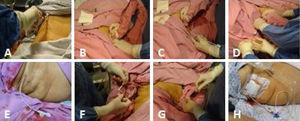 Ryc. 1.
Ryc. 1.(A) Jałowość prawego podżebrza. (B) Skanowanie pęcherzyka żółciowego. (C) Ultrasonograficzne wprowadzenie cewnika wraz z metalowym prowadnikiem w kierunku pęcherzyka żółciowego. (D) Wyciągnięto metalowy prowadnik, zwracając uwagę na pozostawienie cewnika na miejscu, skierowanego do światła pęcherzyka żółciowego i ponownie potwierdzając ultrasonograficznie jego właściwe położenie wewnątrz pęcherzyka. (E) Wprowadzony cewnik cholecystostomijny. (F) Cewnik jest mocowany prostym szwem do skóry przy użyciu prolenu 3-0. (G) Płyn żółciowy jest aspirowany i wysyłany na posiew. (H) Cewnik do cholecystostomii dywersyjnej z workiem do pobierania.
(0.2MB).Powikłania cholecystostomii przezskórnej
Założenie PC jest ogólnie uważane za bezpieczną i skuteczną procedurę. U ponad 90% pacjentów oczekuje się poprawy w zakresie dolegliwości bólowych i ogólnoustrojowej odpowiedzi zapalnej w ciągu pierwszych 48 godzin od założenia PCa.42 Powikłania opisywano jednak w około 3% przypadków. Do najczęstszych powikłań należą: hemobilia, odma opłucnowa, wyciek żółci, żółciowe zapalenie otrzewnej, kamica żółciowa i ropnie.43,44 Ryzykiem jest zawsze eksterioryzacja cewnika, co może utrudnić jego ponowne umieszczenie po odbarczeniu pęcherzyka żółciowego.45,46
Ryzyko nawrotu AC po usunięciu PC waha się od 6 do 40%.47-49 Odnotowano przypadki nawrotu AC, nawet u pacjentów ze sprawnym i drożnym cewnikiem, i zazwyczaj występują one w ciągu pierwszych 2 miesięcy od jego założenia.50 W niektórych seriach przypadków odnotowano dłuższy pobyt w szpitalu u pacjentów z PC.51 Ten dłuższy pobyt jest najprawdopodobniej związany z większym nasileniem objawów u pacjentów, którym zaoferowano PC, a nie jest bezpośrednią konsekwencją zabiegu.52 Odpowiednio wczesne umieszczenie PC, czyli w ciągu pierwszych 24 godzin od wystąpienia objawów, skutecznie skraca pobyt w szpitalu. Udokumentowano to w badaniu z 2015 r., w którym tylko pacjenci z późno założonym PC mieli dłuższy pobyt w szpitalu.53
Kiedy usunąć cewnik cholecystostomijny
Ogólnie rzecz biorąc, PC powinno się usunąć, gdy pacjent jest stabilny, a ostry obraz ustąpił. Idealny czas usunięcia cewnika nie został jednak dokładnie określony.54 Cholangiografia wykonywana przez PC była przeprowadzana w celu oceny drożności przewodu pęcherzykowego. Odnotowano mniejszą częstość nawrotów AC u pacjentów z przepuszczalnym przewodem torbielowatym,55 ale dane są sprzeczne. Nawrót AC może występować w niektórych przypadkach, nawet jeśli cholangiografia dokumentuje drożność dróg żółciowych.56
W retrospektywnym badaniu kohortowym opublikowanym w 2017 roku oceniano dwie grupy. Grupę 1 (n=43) poddano rutynowej cholangiografii przed usunięciem cholecystostomii, a grupę 2 poddano wyłącznie cholangiografii na żądanie (n=41). Chorzy, u których wykonywano cholangiografię na żądanie, mieli lepsze wyniki, ponieważ wcześniej usuwano u nich dren, częściej wykonywano wczesną cholecystektomię i rzadziej korzystano z zasobów.57
W czasie wykonywania LC jako leczenia ostatecznego należy zachować szczególną ostrożność, ponieważ nawet jeśli zapalenie pęcherzyka żółciowego zmniejszyło się lub ustąpiło, choroby współistniejące u pacjenta na ogół utrzymują się, co oznacza, że operacja może być bardziej skomplikowana niż początkowo rozważano.58,59 Częstość konwersji do operacji otwartej w takim przypadku wynosi od 11 do 32%.60-63 Cholecystektomia interwencyjna jest zwykle wykonywana bez problemów technicznych u młodych pacjentów bez chorób współistniejących.64,65
Leczenie definitywne
Założenie cholecystostomii jest w idealnym przypadku leczeniem pomostowym przed leczeniem definitywnym, które wykonuje się po uzyskaniu przez pacjenta poprawy stanu ogólnego.66,67 U ponad 95% pacjentów cholecystektomia jest leczeniem definitywnym,68 ale w seriach przypadków donoszono o pozostawaniu cholecystostomii na czas nieokreślony u 30 do 50% pacjentów.69-71 Niektórzy autorzy zalecają wszczepienie PC jako ostateczne i stałe leczenie u pacjentów w podeszłym wieku oraz u pacjentów z dużym ryzykiem operacyjnym.72
W badaniu opisowym przeprowadzonym w latach 2000-2011 na 36 pacjentach, u których wszczepiono PC, ponieważ uznano ich za pacjentów „wysokiego ryzyka”, autorzy odnotowali 100% ustąpienie objawów 3 dni po wszczepieniu PC u wszystkich pacjentów. PC było leczeniem ostatecznym u 63% chorych, a ostateczną LC wykonano tylko u 6 chorych (16%).73 Inni autorzy opowiadają się za wykonywaniem LC podczas tej samej hospitalizacji, ponieważ opóźnienie LC wiąże się z utratą pacjentów w obserwacji.74 Inne grupy badaczy zgadzają się, że częstość powikłań związanych z cewnikiem jest duża i sugerują usunięcie PC od razu po opanowaniu ostrej odpowiedzi zapalnej, nawet w ciągu pierwszych 10 dni od założenia cewnika.75,76
W doświadczeniach naszego ośrodka cewnik usuwa się w momencie, gdy chory jest planowany do cholecystektomii w ciągu następnych 2 tygodni, wyłącznie w celu poprawy jakości życia chorego przed operacją. Cewnik jest usuwany tylko wtedy, gdy pacjent jest bezobjawowy, nie ma objawów ogólnoustrojowej reakcji zapalnej i ma objawy przepuszczalnego przewodu pęcherzykowego. Jest on również usuwany u pacjentów, którzy będą poddawani definitywnej cholecystektomii. Jeśli te kryteria nie są spełnione, naszym zdaniem należy pozostawić cewnik cholecystostomijny na czas nieokreślony.
Proponujemy przedstawiony na rycinie 3 algorytm usuwania cewnika cholecystostomijnego.
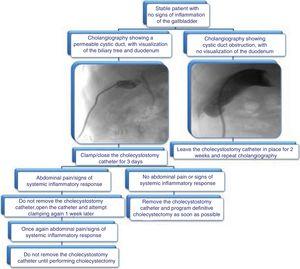 Ryc. 3.
Ryc. 3.Proposed algorithm for the management of cholecystostomy catheters: removal evaluation through cholangiography and clinical data.
(0.35MB).Należy podkreślić, że u pacjentów poddawanych zabiegowi usunięcia cholecystostomii, a następnie LC, odnotowano większą częstość zakażeń miejsca operowanego. Zakażenie to opisywano nawet w 16% przypadków.77
Wnioski
Przezskórna dekompresja pęcherzyka żółciowego jest powszechnie znaną metodą leczenia, ale nadal nie ma wystandaryzowanej strategii postępowania z cewnikiem cholecystostomijnym, co utrudnia jednolitą analizę tych chorych na podstawie dostępnego obecnie piśmiennictwa. Mimo niewielkiej liczby dowodów można jednak sformułować pewne wnioski:
- –
Chorzy operacyjni wysokiego ryzyka z rozpoznaniem AC, u których LC w trybie nagłym jest przeciwwskazana, wydają się być najlepszymi kandydatami do założenia PC.
- –
Nie ma dowodów przemawiających za założeniem PC u stabilnych chorych bez przeciwwskazań do LC.
- –
Usunięcie cewnika PC powinno być wykonane tylko po udokumentowaniu drożności przewodu pęcherzykowego za pomocą cholangiografii, jeśli cewnik powoduje dyskomfort u pacjenta i jeśli pacjent jest kandydatem do ostatecznego leczenia chirurgicznego w „rozsądnym” i odpowiednim czasie, aby zmniejszyć możliwość wystąpienia nawracającego ostrego zapalenia pęcherzyka żółciowego.
Mało jest dowodów dotyczących postępowania w przypadku przezskórnych cewników cholecystostomijnych i obecnie potrzebne są randomizowane badania oceniające najlepszą strategię postępowania w tej grupie chorych.
Ujawnienia etyczne
Ochrona ludzi i zwierząt. Autorzy oświadczają, że na potrzeby tego artykułu nie przeprowadzono żadnych eksperymentów na ludziach ani zwierzętach.
Poufność danych. Autorzy oświadczają, że traktowali wszystkie dane pacjentów z zachowaniem poufności i anonimowości, zgodnie z protokołami ich ośrodka pracy.
Prawo do prywatności i świadoma zgoda. Autorzy oświadczają, że w niniejszym artykule nie pojawiają się żadne dane pacjentów, które naruszają ich tożsamość, w związku z czym nie było konieczne uzyskanie ich świadomej zgody.
Ujawnienie informacji finansowych
Nie otrzymano żadnego wsparcia finansowego w związku z niniejszym artykułem.
Konflikt interesów
Autorzy oświadczają, że nie występuje konflikt interesów.
.
- 6
Leave a Reply