Atlas of plant and animal histology
1. Morfologi
2. Livscykel
3. Funktioner
– Matsmältning
– Skydd
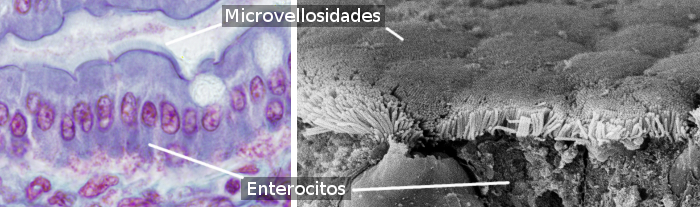
Enterocyter är kolonnformade celler som bildar större delen av tarmtarmens epitel (figur 1 och 2). De är rikligare i tunntarmen än i tjocktarmen och blindtarmen. I tunntarmen är mängden enterocyter cirka 80 % av den totala mängden tarmens enterocyter. Enterocyternas huvudsakliga funktion är att absorbera molekyler från tarmlumen och transportera dem till inre bindväv och blodkärl. Det är värt att notera att tarmepitelet är den större yta i kroppen som är i kontakt med den yttre miljön (tarmens lumen ligger utanför kroppens vävnader).


Morfologi
Enterocyter har mikrovilli i den apikala (fria) ytan (figur 3), många mitokondrier i den basala delen samt en välutvecklad Golgiapparat och endoplasmatiskt retikulum. Tarmepitelets mekaniska integritet, dvs. sammanhållningen mellan enterocyter och avsaknaden av intercelulära passager, beror på celladhesionskomplexen mellan intilliggande enterocyter. Det finns tighta korsningar och adherenta korsningar nära enterocytens apikala domän. Desmosomer finns i de latero-basala membranen. Gap junctions observeras också i de latero-basala membranen. Hemidesmosomer finns i enterocyternas basala membran och förankrar cellen till basalmembranet.
Enterocyter har två domäner: apikala och basolaterala. Det är därför de är polariserade celler. Polariseringen produceras av aktiviteten hos ett välordnat cytoskelett och en välutvecklad vesikulär trafik som distribuerar molekyler differentiellt mellan de båda domänerna. Täta junctions förhindrar lateral diffusion av molekyler mellan de båda domänerna, vilket bidrar till att upprätthålla polariteten. Enterocyter uppvisar en mycket packad mikrovillus i den apikala domänen, som ökar membranytan ungefär 100 gånger (figur 3). I de apikala membranen finns många transportörer som är portar för att molekyler från matsmältningen ska komma in i enterocyten. I de basolateala membranen finns andra transportörer för att dessa molekyler ska kunna lämna enterocyten och nå blodkärlen. Denna segregerade fördelning av receptorer skapas genom vesikulär trafikering.
Livscykel
Tarmlumen är full av molekyler som är potentiellt giftiga för enterocyter. Istället för att reparera varje kränkning dör skadade och gamla enterocyter genom apoptos,de utgår sedan ur epitelskiktet och ersätts kontinuerligt av nya. Tunntarmens slemhinna är starkt veckad och bildar många utväxter eller villi och invaginationer eller körtlar, så kallade Lieberkühn-kryptor. I tjocktarmen finns Lieberkühn-kryptor. Enterocyternas livscykel börjar i den nedre delen av Lieberkühn-körtlarna och slutar i spetsarna av småtarmens villi eller i tjocktarmens epitelyta. Livet för en enterocyt är ungefär 2 till 5 dagar långt. Hos människor förnyas tarmepitelet var fjärde till femte dag.
Enterocyter differentieras från vuxna stamceller som finns i botten av Lieberkühn-körtlarna (figur 4). Inledningsvis blir de vuxna stamcellerna till övergående amplifierande celler (progenitorceller), som ligger lite längre bort från den vuxna stamcellsnischen. Transient amplifierande celler delar sig 4-6 gånger för att öka progenitorpopulationen och differentierar sedan i de olika celltyper som finns i tarmepitelet. De flesta av dem blir enterocyter, men även globetceller, M-celler och de andra celltyperna. Nya enterocyter rör sig successivt mot spetsarna av villi eller mot den luminala epitelytan. När de når dessa positioner dör de och stöts ut från epitelet. Extrusionen inbegriper både mekaniskt tryck och förlust av adhesionsförbindelser med granncellerna. Vissa celler dör genom apoptos och stöts sedan ut från epitelet. Man vet inte vilken mekanism som förflyttar enterocyter från körtlarna till epitelytan. Molekylära komponenter i den basala lamina är olika längs enterocyternas väg och man tror att de kan bidra till rörelsen. Man har också trott att kosten är inblandad i dynamiken i enterocyternas liv.

Funktioner
Matsmältning
Enterociterna har som huvudfunktion att ta upp näringsämnen efter magens och den enzymatiska matsmältningen av maten. Enterocyter kan använda glutamat och glutamin samt fettsyror och glukos som energitillförsel. Detta är märkligt eftersom alla typer av näringsämnen går genom enterocyterna. De hjälper också till med matsmältningen genom att utsöndra enzymer som bryter ner peptider och disacarider. Glykokalyxet i enterocytens apikala domän bildar ett ca 400-500 nm tjockt lager, ibland till och med 1 µm tjockt. Vissa enzymer som deltar i matsmältningen är förankrade i detta glykokalyx. Enterocyterna väljer alltså inte bara ut och fångar upp ämnen från matsmältningen, utan bearbetar också en del av dem. Det sägs faktiskt att det finns två matsmältningsfaser, en som sker i tarmens lumen och som utförs av bukspottkörtelns enzymer, och en som sker på enterocyternas yta och som utförs av andra matsmältningsenzymer. Den största delen av näringsupptaget utförs av tunntarmens enterocyter, medan tjocktarmens enterocyter huvudsakligen absorberar vatten. Dessutom frigörs små vesiklar från mikrovilliernas spetsar som innehåller enzymer som fosfataser, vilka kan ha en försvarsfunktion mot patogener.
Substanser som uppstår vid matsmältningen måste passera tarmepitelet för att nå blodomloppet. Det kan ske genom flera vägar: transcellulär, endocytos/transcytos och paracellulär.
Transcellulärt. De flesta molekyler korsar tarmens epitelskikt och går genom enterocyter. Först korsar de det apikala membranet och sedan det basolaterala. Molekylerna kan förflyttas genom fri passiv diffusion, underlättad passiv diffusion eller aktiv transport. Vid fri passiv diffusion korsar molekylerna membranen utan någon hjälp, medan molekylerna vid underlättad och aktiv transport måste kännas igen av specifika transportörer som är infogade i membranen. Vatten, etanol och många lipider passerar genom enterocyter genom fri passiv diffusion. Glukos, vissa lipider och aminosyror kommer in i enterocyterna genom förenklad passiv transport eller aktiv transport.
Cellens apikala domän bär på en uppsättning proteiner för absorption av ämnen, medan de latero-basala membranen har andra transmembrantransportörer för att få ut molekyler ur enterocyten.
Absorptionsförmågan beror på enterocytens differentieringsstadium, vilket innebär ett antal natriummembranpumpar, som är rikligare när enterocyterna rör sig längre bort från kryptornas djup. Den största delen av absorptionen av socker och aminosyror sker således i den övre tredjedelen av tunntarmens villi och nära tjocktarmens yta. Hydrolasaktiviteten ökar till exempel när enterocyterna rör sig bort från stamcellsnischerna (de djupa delarna av kryptorna).
Absorptionen av glukos är ett exempel på en typisk absorptionsmekanism. Glukos passerar enterocytens apikala membran genom samtransport kopplad till en natriumgradient. Denna gradient genereras av natrium/kalium-pumpar och kan ta in glukos i enterocyten mot glukoskoncentrationsgradienten. Natriumglukostransportören (SGLT) möjliggör denna samtransport. Å andra sidan finns GLUT2-transportören i de laterobasala membranen, som translokaliserar glukos från cytoplasman till det intercellulära utrymmet. SGLT ökar alltså glukoskoncentrationen i enterocytens cytoplasma och GLUT2 låter glukos flyta ut mot blodkärlen. Den exakta placeringen av de två transportörerna ger upphov till ett flöde av glukos genom enterocyterna, från tarmlumen till blodkärlen.
Fett är bland de mest energirika ämnena, förutom att det är nödvändigt för cellmembranen. Majoriteten av det måltidsfett som införlivas från tarmen är i form av triacylglycerol, även om även andra typer kan absorberas, t.ex. kolesterol. Först bryter pankreasenzymer ner matfett i tarmlumen och triacylglyceroler omvandlas till fettsyror och monoacylglyceroler (figur 5). Dessa molekyler bildar tillsammans med kolesterol, fettlösliga vitaminer och fosfolipider micelas, som är små lipiddroppar som är lösliga i vatten tack vare gallsyrorna. Micellerna passerar fritt det apikala membranet i enterocyten. Transportörerna CD36 y FABP (fettsyrabindande protein) s 3 gör det möjligt för vissa fettämnen att korsa enterocytens apikala membran genom förenklad passiv transport. Huvuddelen av fetttransporten sker som miceller, medan membrantransportörerna ser ut som ett sensoriskt system för att upptäcka fettsyror s 3 med långa kedjor i tarmen. Kolesterol, som enskild molekyl, kan också transporteras av transportören NPC1L1 (Niemann-Pick C1-like 1), som överför kolesterol från tarmens lumen till enterocytens cytoplasma.

När de väl befinner sig i enterocyten förenas fetter med vissa proteiner och flyttas till det endoplasmatiska retikulumet, där triacylglyceroler syntetiseras på nytt. De förenas med vissa proteiner för att bilda pre-chylomikroner. ApoB-protein syntetiseras i det endoplasmatiska retikulumet. ApoB bildar tillsammans med MTP (microsome tranfer protein) och fettsyror den primära lipoproteinpartikeln. I det släta endoplasmatiska retikulumet ersätts ApoB av Apo A-IV-protein. Alla dessa komponenter utgör prechylomikroner, som ingår i vesiklar och flyttas till Golgiapparaten. Där förenas pre-chylomikroner till chylomikroner, som ingår i exocytiska vesiklar och släpps ut i den laterobasala delen av enterocyten. På detta sätt kan chylomikronerna nå blod- och lymfkärlen. Chylomikroner är lipoproteiner med en kropp som huvudsakligen består av triacylglyceroler och ett hölje av fosfolipider, kolesterol och apolipoproteiner. De spelar en viktig roll för transport av triacylglyceroler och fettlösliga vitaminer.
Utanför enterocyten kommer chylomikroner in i lymfkärlen i tarmvilli och sedan i de lymfatiska myenteriska plexus plexus från vilka de passerar till blodkärlen. Förutom chylomikroner packas fett också i lipoproteiner med mycket låg densitet (VLDL), som också exocytas från enterocyter. Fett kan också lagras i enterocyternas lipiddroppar.
Enterocyterna får också i sig järn efter matsmältningen. Järn är viktigt för många proteiner, till exempel hemoglobin, och det kan finnas i maten som en del av hemogrupper eller bundet till ferritin (i djurkött) (figur 6). Järn från matsmältningen kommer in i kroppen genom DMT1-transportören (divalent metal transporter 1) som finns i enterocyternas apikala membran. Transgena möss som saknar denna transportör utvecklar allvarlig anemi. DMT1 är en samtransportör som är kopplad till en protongradient. Protongradienten genereras av Na+/K+-pumpen, som också finns i enterocyternas apikala membran. DMT1 transporterar Fe2+ men det mesta järnet från måltid är Fe3+ form. Järnreduktion (Fe3+ till Fe2+) utförs av ett reduktasenzym som finns på enterocytens apikala yta. Det järn som är bundet till hemogrupper verkar införlivas genom receptormedierad endocytos. När de väl är inne i enterocyten bryts hemogruppen ner och järnet kan komma in i cytosolen.

Oavsett hur inflödesvägen ser ut verkar järnets rörelse mot de basolaterala membranen, när det väl befinner sig i cytosolen, medieras av metallokaperonproteiner. I de basolaterala membranen translokeras järn till det extracellulära rummet av ferroportintransportören. Ferroportin tar ut Fe2+ form. Ferritin är dock det protein som transporterar järn till portalveinsystemet och järn måste vara i Fe3+-form. Det finns ferrooxidaser i enterocytens basolaterala membran som möjliggör omvandlingen från Fe2+ till Fe3+. Järn kan lagras i enterocytens cytosol bundet till ferritin.
Endocytos/transcytos. Molekyler som immunglobuliner endocytas genom receptormedierad endocytos och transporteras till andra membranområden genom transcytos. Vesiklar bildas vid basen av mikrovilli, och de smälter senare samman med endosomer. Immunoglobuliner innesluts sedan i vesiklar som bildas i endosomerna och riktas till de basolaterala domänmembranen. På detta sätt undgår immunglobulinerna den lysosomala nedbrytningsvägen.
Paracellulär. Vatten och joner passerar epitelim genom den paracellulära vägen.
Beskydd
Enterocyter bildar en barriär som avvisar antigener, giftiga molekyler och mikroorganismer och samtidigt släpper igenom näringsämnen. Enterocyter är i kontakt med många mikroorganismer. De som är bofasta mikroorganismer i tarmen, men som kan vara farliga om de når de inre vävnaderna, och de icke bofasta patogener som följer med måltiden. Enterocyternas apikala yta är täckt av ett lager av slemämnen som frigörs av globetcellerna. Detta lager består av kolhydrater och har en tät viskositet som tillåter diffusion av molekyler, men stöter bort celler och de största molekylerna. Dessutom uppvisar enterocyternas mikrovilli en välutvecklad glykokalyx i de apikala spetsarna av varje mikrovillus, som fungerar som fysisk och elektrisk barriär eftersom den är full av negativa laddningar. Dessa mikrovilli försvårar en direkt fysisk kontakt mellan mikroorganismer och enterocytens membran. Även om mikroorganismerna passerar dessa två barriärer måste de dock övervinna mikrovilliernas transportmekanism.
Muciner är starkt glykosylerade proteiner som finns i enterocyternas apikala membran. De bidrar till det välutvecklade glykokalyxet. Muciner är transmembranproteiner som är kopplade till cytoskelettet genom sin cytosoliska domän. MUC3, MUC12 och MUC17 är de vanligaste mucinerna. De innehåller cirka 5 000 aminosyror och deras kolhydratkomponent kan sträcka sig upp till 1 µm från cellytan. Muciner bildar en fysisk barriär som är svår att passera för bakterier.
Enterocyter kan starta och reglera inflammatoriska processer genom att frisätta flera chimokiner och cytokiner. De har också receptorer för dessa molekyler. Enterocyter frigör proinflammatoriska molekyler som påverkar immunceller som finns i tarmslemhinnan.
En annan mindre känd skyddsmekanism är frisättningen av vesiklar från enterocyternas apikala yta. Actin och myosin, mikrovilliernas motoriska apparat, producerar mekaniska krafter som drar membranen mot spetsen av varje mikrovillus. Membranansamlingen slutar som vesiklar som släpps ut i tarmlumen. Dessa vesiklar innehåller en stor mängd alkaliskt fosfatas som är ett kraftfullt antipatogent medel genom att minska lipopolysacharidtoxicitet och tarminflammation. Det förhindrar också bakteriernas fastsättning på instegsepitelet och minskar bakteriespridningen. De vesiklar som släpps ut av enterocyten är ett sätt att skicka antimikrobiella molekyler till områden långt bort från epitelet.
Bibliografi
Barker N. 2014. Vuxna tarmstamceller: kritiska drivkrafter för epitelisk homeostas och regeneration. Nature. 15: 19-33.
Giammanco A, Cefalù AB, Noto D, Averna MR. 2015. Patofysiologin bakom produktionen av intestinala proteiner. Frontiers in physiology. 6: 61.
Knutson MD. 2014. Vuxna tarmstamceller: kritiska drivkrafter för epitelisk homeostas och regeneration. Nature review in molecular cell biology. 15:19-33.
Knutson MD. 2017. Järntransportproteiner: portar för cellulär och systemisk järnhomeostas. Journal of biological chemistry Nature review in molecular cell biology. 292: 12735-12743.
Shifrin DA, McConell RE, Nambiar R, Higginbotham JN, Coffey RJ, Tyska MJ. 2012. Vesiklar som härrör från enterocytens mikrovillus avgiftar bakterieprodukter och reglerar interaktioner mellan epitel och mikroorganismer. Aktuell biologi. 22: 627-631.
Snoeck V, Goddeeries B, Cox E. 2005. Enterocyternas roll i tarmens barriärfunktion och antigenupptag. Mikrober och infektioner. 7: 997-1004.
Leave a Reply