A növényi és állati szövettan atlasza
1. Morfológia
2. Életciklus
3. Funkciók
– Emésztés
– Védekezés
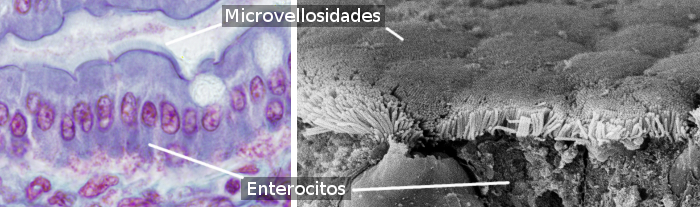
Az enterociták oszlopos sejtek, amelyek a bélbél hámjának nagy részét alkotják (1. és 2. ábra). A vékonybélben nagyobb mennyiségben fordulnak elő, mint a vastagbélben és a vakbélben. A vékonybélben az enterociták mennyisége a teljes bél enterociták mintegy 80%-át teszi ki. Az enterociták fő funkciója a molekulák felszívása a bél lumenéből, és azok szállítása a belső kötőszövetbe és a vérerekbe. Megjegyzendő, hogy a bélhám a testnek a külső környezettel érintkező nagyobb felülete (a bél lumenje a testszöveteken kívül van).


Morfológia
Az enterociták apikális (szabad) felszínén mikrovillák találhatók (3. ábra), a bazális részen sok mitokondrium, valamint jól fejlett Golgi-apparátus és endoplazmatikus retikulum. A bélhám mechanikai integritása, azaz az enterociták közötti kohézió és az intercelluláris átjárók hiánya a szomszédos enterociták közötti sejtadhéziós komplexektől függ. Az enterocita apikális tartományának közelében szoros kötések és adhéziós kötések vannak. A latero-bazális membránokban dezmoszómák találhatók. A latero-bazális membránokban is megfigyelhetők gap junctions. Az enterociták bazális membránjában hemidesmosomák találhatók, amelyek a sejtet a bazális membránhoz rögzítik.
Az enterocitáknak két tartománya van: apikális és basolaterális. Ezért polarizált sejtek. A polarizációt a jól rendezett citoszkeleton és a jól fejlett vezikuláris forgalom aktivitása hozza létre, amely differenciáltan osztja el a molekulákat a két domén között. A szoros kötések megakadályozzák a molekulák laterális diffúzióját a két domén között, így segítve a polaritás fenntartását. Az enterociták az apikális doménben nagymértékben csomagolt mikrovillákat mutatnak, amelyek mintegy 100-szorosára növelik a membránfelületet (3. ábra). Az apikális membránokban számos transzporter található, amelyek az emésztésből származó molekulák kapui, hogy bejussanak az enterocitába. A bazolateális membránokban más transzporterek találhatók, amelyek segítségével ezek a molekulák kiléphetnek az enterocitából, és elérhetik az ereket. A receptoroknak ezt a szegregált eloszlását a vezikuláris kereskedelem hozza létre.
Életciklus
A béllumen tele van az enterociták számára potenciálisan toxikus molekulákkal. Ahelyett, hogy minden sérülést kijavítanának, a sérült és öreg enterociták apoptózis útján elpusztulnak,majd kilökődnek a hámrétegből, és folyamatosan újakkal pótolják őket. A vékonybél nyálkahártyája erősen hajtogatott, és számos kitüremkedést vagy villi-t, illetve behúzódást vagy mirigyet alkot, amelyeket Lieberkühn-kripta néven ismerünk. A vastagbélben Lieberkühn-kripták találhatók. Az enterociták életciklusa a Lieberkühn-mirigyek alsó részén kezdődik, és a vékonybél villijeinek csúcsaiban vagy a vastagbél hámfelszínén végződik. Egy enterocita élete körülbelül 2-5 napig tart. Emberben a bélhám 4-5 naponta megújul.
Az enterociták felnőtt őssejtekből differenciálódnak, amelyek a Lieberkühn-mirigyek alján találhatók (4. ábra). Kezdetben a felnőtt őssejtek átmeneti felerősödő sejtekké (progenitorsejtekké) válnak, amelyek a felnőtt őssejt niche-től kissé távolabb helyezkednek el. A tranziens amplifikáló sejtek 4-6-szor osztódnak a progenitorpopuláció növelése érdekében, majd a bélhámban található különféle sejttípusokká differenciálódnak. Legtöbbjük enterocitákká válik, de globet-sejtekké, M-sejtekké és a többi sejttípussá is. Az új enterociták fokozatosan a villi csúcsok vagy a luminális hámfelszín felé mozognak. Amint elérik ezeket a pozíciókat, elhalnak és kilökődnek a hámból. Az extrudálás mechanikai nyomással és a szomszédos sejtekkel való adhéziós kapcsolat elvesztésével jár. Egyes sejtek apoptózis útján elpusztulnak, majd kilökődnek a hámból. Nem ismert, hogy mi az a mechanizmus, amely az enterocitákat a mirigyekből a hámfelszínre mozgatja. A bazális lamina molekuláris komponensei az enterociták útja mentén eltérőek, és úgy gondolják, hogy hozzájárulhatnak a mozgáshoz. Úgy gondolják, hogy a táplálkozásnak is szerepe van az enterociták életének dinamikájában.

Funkciók
Emésztés
Az enterociták fő funkciója a tápanyagok felszívása a táplálék gyomor- és enzimatikus emésztése után. Az enterociták energiaforrásként glutamátot és glutamint, valamint zsírsavakat és glükózt használhatnak. Ez azért különös, mert az enterocitákon mindenféle tápanyag áthalad. Az emésztést is segítik azáltal, hogy peptideket és diszakararidokat lebontó enzimeket választanak ki. Az enterociták apikális tartományának glikokalyxa körülbelül 400-500 nm vastagságú, néha 1 µm vastagságú réteget alkot. Néhány, az emésztésben részt vevő enzim ehhez a glikokalyxhoz rögzül. Így az enterociták nemcsak kiválasztják és felfogják az emésztésből származó anyagokat, hanem néhányat közülük fel is dolgoznak. Tulajdonképpen azt mondják, hogy két emésztési fázis van, az egyik a bél lumenében történik, amelyet a hasnyálmirigy enzimek végeznek, a másik pedig az enterociták felszínén, amelyet más emésztőenzimek végeznek. A tápanyagok felszívódásának nagy részét a vékonybél enterocitái végzik, míg a vastagbél enterocitái elsősorban vizet szívnak fel. Ezenkívül a mikrovillák csúcsaiból kis vezikulák szabadulnak fel, amelyek enzimeket, például foszfatázokat tartalmaznak, és amelyeknek védekező funkciójuk lehet a kórokozókkal szemben.
Az emésztésből származó anyagoknak át kell haladniuk a bélhámon, hogy a véráramba jussanak. Ez többféle úton történhet: transzcellulárisan, endocitózissal/transzcitózissal és paracellulárisan.
Transzcelluláris. A legtöbb molekula a bél hámrétegén áthaladva enterocitákon keresztül halad át. Először az apikális, majd a bazolaterális membránon haladnak át. A molekulák szabad passzív diffúzióval, facilitált passzív diffúzióval vagy aktív transzporttal mozoghatnak. A szabad passzív diffúzióban a molekulák segítség nélkül haladnak át a membránokon, míg a facilitált és az aktív transzportban a molekulákat a membránokba épített specifikus transzportereknek kell felismerniük. A víz, az etanol és számos lipid szabad passzív diffúzióval jut át az enterocitákon. A glükóz, néhány lipid és aminosav az enterocitákba könnyített passzív transzporttal vagy aktív transzporttal jut be.
A sejt apikális tartománya egy sor fehérjét hordoz az anyagok felszívódására, míg a latero-bazális membránok más transzmembrán transzportereket tartalmaznak a molekuláknak az enterocitából való kijuttatására.
Az abszorpciós képesség az enterocita differenciálódási stádiumától függ, ami számos nátrium membránszivattyút jelent, amelyek annál gyakoribbak, minél távolabb kerülnek az enterociták a kripták mélyétől. Így a cukrok és aminosavak felszívódásának nagy része a vékonybél cimpáinak felső harmadában és a vastagbél felszínéhez közel történik. Például a hidroláz aktivitás nő, ahogy az enterociták távolodnak az őssejtes niche-ektől (a kripták mély részei).
A glükóz felszívódása egy példa a tipikus felszívódási mechanizmusra. A glükóz az enterocita apikális membránján nátriumgradienshez kapcsolt ko-transzport révén halad át. Ezt a gradienst nátrium/káliumpumpák hozzák létre, és a glükóz a glükóz koncentrációs gradiens ellenében juthat be az enterocitába. A nátrium-glükóztranszporter (SGLT) teszi lehetővé ezt a ko-transzportot. Másrészt a GLUT2 transzporter a laterobazális membránokban található, amely a glükózt a citoplazmából a sejtközti térbe transzlokálja. Így az SGLT növeli a glükózkoncentrációt az enterocita citoplazmájában, a GLUT2 pedig lehetővé teszi a glükóz távozását az erek felé. A két transzporter pontos elhelyezkedése glükózáramlást eredményez az enterocitákon keresztül, a bél lumenéből a vérerekbe.
A zsír a legenergetikusabb anyagok közé tartozik, amellett, hogy szükséges a sejtmembránokhoz. A bélből beépülő étkezési zsír nagy része triacilglicerin formában van, bár más típusok is felszívódhatnak, például a koleszterin. Először a hasnyálmirigy enzimek lebontják az étkezési zsírt a bél lumenében, és a triacilglicerineket zsírsavakká és monoacilglicerinokká alakítják (5. ábra). Ezek a molekulák a koleszterinnel, a zsírban oldódó vitaminokkal és a foszfolipidekkel együtt micéliumokat alkotnak, amelyek az epesavaknak köszönhetően vízben oldódó kis lipidcseppek. A micellák szabadon áthaladnak az enterocita apikális membránján. A CD36 y FABP (fatty acid binding protein) s 3 transzporterek lehetővé teszik, hogy egyes zsíros anyagok könnyített passzív transzport révén áthaladjanak az enterocita apikális membránján. A zsírszállítás nagy része micellák formájában történik, míg a membrántranszporterek érzékelő rendszerként érzékelik a hosszú láncú s 3 zsírsavakat a bélben. A koleszterint, mint egyedi molekulát, az NPC1L1 (Niemann-Pick C1-like 1) transzporter is képes szállítani, amely a koleszterint a bél lumenéből az enterocita citoplazmájába juttatja.

Az enterocitában a zsírok egyes fehérjékhez kapcsolódnak, és az endoplazmatikus retikulumba kerülnek, ahol a triacilglicerineket újra szintetizálják. Ezek egyesülnek néhány fehérjével, hogy pre-kilomikronokat képezzenek. Az ApoB fehérje az endoplazmatikus retikulumban szintetizálódik. Az ApoB az MTP-vel (microsome tranfer protein) és a zsírsavakkal együtt alkotja a lipoprotein primordiális részecskét. A sima endoplazmatikus retikulumban az ApoB-t Apo A-IV fehérje helyettesíti. Mindezek a komponensek prekilomikronokat alkotnak, amelyek vezikulákba kerülnek, és a Golgi-apparátusba kerülnek. Itt a pre-kilomikronok összekapcsolódnak, és kilomikronokat alkotnak, amelyek exocitikus vezikulákba kerülnek, és az enterocita laterobazális tartományában szabadulnak fel. Ily módon a chilomikronok eljuthatnak a vérbe és a nyirokerekbe. A chilomikronok olyan lipoproteinek, amelyek teste főként triacilglicerinből, bevonata pedig foszfolipidekből, koleszterinből és apolipoproteinekből áll. Fontos szerepet játszanak a triacilglicerinok és a zsírban oldódó vitaminok szállításában.
Az enterocitán kívül a chilomikronok a bélnyálkahártyák nyirokerébe, majd a nyirokerekbe, a myentericus plexusokba kerülnek, ahonnan a vérerekbe jutnak. A chilomikronok mellett a zsír nagyon alacsony sűrűségű lipoproteinekbe (VLDL) is csomagolódik, amelyek szintén az enterocitákból exocitálódnak. A zsír az enterociták lipidcseppjeiben is tárolódhat.
Az enterociták emésztés után vasat is kapnak. A vas számos fehérje, például a hemoglobin számára fontos, és a táplálékban hemocsoportok részeként vagy ferritinhez kötve (állati húsban) megtalálható (6. ábra). Az emésztésből származó vas az enterociták apikális membránjában található DMT1 transzporteren (kétértékű fémtranszporter 1) keresztül jut a szervezetbe. Az e transzgénikus egereknél, amelyekből hiányzik ez a transzporter, súlyos vérszegénység alakul ki. A DMT1 egy protongradienshez kapcsolt ko-transzporter. A protongradienst a Na+/K+ pumpa hozza létre, amely szintén az enterociták apikális membránjában található. A DMT1 Fe2+-t szállít, de az étkezésből származó vasak többsége Fe3+ formában van jelen. A vas redukcióját (Fe3+ Fe2+ -ra) az enterocita apikális felszínén található reduktáz enzim végzi. Úgy tűnik, hogy a hemocsoportokhoz kötött vas receptor közvetítette endocitózissal épül be. Az enterocita belsejében a hemocsoport lebomlik, és a vas a citoszolba kerülhet.

A bejutási útvonaltól függetlenül, amint a citoszolban van, úgy tűnik, hogy a vas mozgását a bazolaterális membránok felé a metallochaperon fehérjék közvetítik. A bazolaterális membránokban a vasat a ferroportin transzporter transzlokálja az extracelluláris térbe. A ferroportin a Fe2+ formát veszi ki. A ferritin azonban az a fehérje, amely a portális vénarendszerbe szállítja a vasat, és a vasnak Fe3+ formában kell lennie. Az enterocita bazolaterális membránjaiban ferro-oxidázok vannak, amelyek lehetővé teszik a Fe2+-ról Fe3+-ra történő átalakulást. A vas az enterocita citoszoljában ferritinhez kötődve tárolható.
Endocitózis/transzcitózis. Az olyan molekulák, mint az immunglobulinok, receptor közvetítette endocitózissal endocitálódnak, és transzcitózissal más membrándoménekbe szállítódnak. A vezikulák a mikrovillák tövében képződnek, és később összeolvadnak az endoszómákkal. Az immunglobulinok ezután az endoszómákban keletkező vezikulákba záródnak, és a bazolaterális domének membránjaira irányulnak. Ily módon az immunglobulinok megmenekülnek a lizoszomális lebontási útvonaltól.
Paracelluláris. A víz és az ionok paracelluláris úton haladnak át a hámszöveten.
Védelem
Az enterociták olyan gátat képeznek, amely elutasítja az antigéneket, toxikus molekulákat és mikroorganizmusokat, ugyanakkor átengedi a tápláló anyagokat. Az enterociták számos mikroorganizmussal kerülnek kapcsolatba. Azokkal, amelyek a bélben rezidens mikroorganizmusok, de veszélyesek lehetnek, ha a belső szövetekbe jutnak, és azokkal a nem rezidens kórokozókkal, amelyek az étkezéssel érkeznek. Az enterociták apikális felszínét a globet sejtek által kibocsátott nyálkás anyagok rétege borítja. Ez a réteg szénhidrátokból áll, és sűrű viszkozitású, ami lehetővé teszi a molekulák diffúzióját, de visszautasítja a sejteket és a legnagyobb molekulákat. Ezenkívül az enterocita mikrovillák apikális csúcsain jól fejlett glikokalyx található, amely fizikai és elektromos gátként működik, mivel tele van negatív töltésekkel. Ezek a mikrovillák megnehezítik a mikroorganizmusok és az enterocita membránja közötti közvetlen fizikai kapcsolatot. Azonban még ha át is jutnak e két akadályon, a mikroorganizmusoknak le kell győzniük a mikrovillák transzportmechanizmusát.
A mucinek erősen glikozilált fehérjék, amelyek az enterociták apikális membránjában találhatók. Hozzájárulnak a jól fejlett glikokalyxhoz. A mucinek transzmembrán fehérjék, amelyek citoszolikus doménjükkel kapcsolódnak a citoszkeletonhoz. A MUC3, a MUC12 és a MUC17 a legnagyobb mennyiségben előforduló mucinek. Körülbelül 5000 aminosavat tartalmaznak, és szénhidrátkomponensük akár 1 µm-re is kiterjedhet a sejtfelszíntől. A mucinek olyan fizikai gátat képeznek, amelyet a baktériumok nehezen tudnak átlépni.
Az enterociták számos kimocin és citokin felszabadításával képesek gyulladásos folyamatokat elindítani és szabályozni. Ezen molekulák számára receptorokkal is rendelkeznek. Az enterociták olyan pro-inflammatorikus molekulákat szabadítanak fel, amelyek befolyásolják a bélnyálkahártyán található immunsejteket.
Egy másik, kevésbé ismert védelmi mechanizmus az enterociták apikális felszínéről történő vezikulák felszabadulása. A mikrovillák motoros apparátusa, az aktin és a miozin mechanikus erőket termel, amelyek a membránokat az egyes mikrovillák csúcsa felé húzzák. A membránfelhalmozódás végül vezikulák formájában végződik, amelyek a béllumenbe szabadulnak. Ezek a vezikulák nagy mennyiségű alkalikus foszfatázt tartalmaznak, amely a lipopoliszacharid toxicitását és a bélgyulladást csökkentve erős patogénellenes szer. Emellett akadályozza a baktériumok kötődését a bélhámhoz, és csökkenti a baktériumok szaporodását. Az enterociták által kibocsátott vezikulák a mikrobaellenes molekuláknak a hámtól távolabbi területekre történő elküldését szolgálják.
Bibliográfia
Barker N. 2014. Felnőtt bélrendszeri őssejtek: a hám homeosztázisának és regenerációjának kritikus mozgatórugói. Nature. 15: 19-33.
Giammanco A, Cefalù AB, Noto D, Averna MR. 2015. Az intestinalis lipoprotein termelés patofiziológiája. Frontiers in physiology. 6: 61.
Knutson MD. 2014. Felnőtt bélrendszeri őssejtek: a hám homeosztázisának és regenerációjának kritikus mozgatórugói. Nature review in molecular cell biology. 15:19-33.
Knutson MD. 2017. Vastranszportfehérjék: a celluláris és szisztémás vashomeosztázis kapui. Journal of biological chemistry Nature review in molecular cell biology. 292: 12735-12743.
Shifrin DA, McConell RE, Nambiar R, Higginbotham JN, Coffey RJ, Tyska MJ. 2012. Az enterocita microvillus-ból származó vezikulák detoxikálják a bakteriális termékeket és szabályozzák a hám-mikrobiális kölcsönhatásokat. Current biology. 22: 627-631.
Snoeck V, Goddeeries B, Cox E. 2005. Az enterociták szerepe a bélbarrier funkcióban és az antigénfelvételben. Mikrobák és fertőzés. 7: 997-1004.
Leave a Reply