Atlas of plant and animal histology
1. Morfologie
2. Životní cyklus
3. Funkce
– trávení
– ochrana
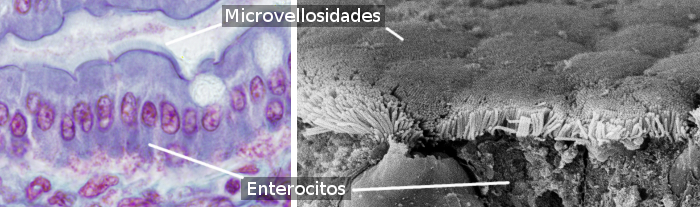
Enterocyty jsou sloupcovité buňky, které tvoří většinu epitelu střeva (obrázky 1 a 2). V tenkém střevě jsou hojnější než v tlustém střevě a slepém střevě. V tenkém střevě tvoří enterocyty asi 80 % všech střevních enterocytů. Hlavní funkcí enterocytů je vstřebávání molekul ze střevního lumen a jejich transport do vnitřní pojivové tkáně a krevních cév. Za povšimnutí stojí, že střevní epitel je větším povrchem těla, který je v kontaktu s vnějším prostředím (lumen střeva je vůči tělesným tkáním vnější).


Morfologie
Enterocyty mají na apikálním (volném) povrchu mikroklky (obrázek 3), v bazální části mnoho mitochondrií a dobře vyvinutý Golgiho aparát a endoplazmatické retikulum. Mechanická integrita střevního epitelu, tj. soudržnost mezi enterocyty a absence mezibuněčných chodeb, závisí na adhezních komplexech mezi sousedními enterocyty. V blízkosti apikální oblasti enterocytu se nacházejí těsné spoje a adherentní spoje. Desmosomy se nacházejí v laterobazálních membránách. V laterobazálních membránách jsou rovněž pozorovány gap junctions. Hemidesmosomy se nacházejí v bazální membráně enterocytů a ukotvují buňku k bazální membráně.
Enterocyty mají dvě domény: apikální a bazolaterální. Proto jsou to polarizované buňky. Polarizace vzniká činností dobře uspořádaného cytoskeletu a dobře vyvinutým vezikulárním provozem, který rozděluje molekuly diferencovaně mezi obě domény. Těsné spoje brání laterální difuzi molekul mezi oběma doménami, a pomáhají tak udržovat polaritu. Enterocyty vykazují v apikální doméně vysoce zabalené mikroviry, které zvětšují povrch membrány asi 100krát (obr. 3). V apikálních membránách se nachází mnoho transportérů, které jsou branami, jimiž se molekuly vzniklé trávením dostávají do enterocytu. V bazálních membránách jsou další přenašeče, kterými tyto molekuly opouštějí enterocyt a dostávají se do cév. Tato segregovaná distribuce receptorů vzniká vezikulárním přenosem.
Životní cyklus
Střevní lumen je plné molekul potenciálně toxických pro enterocyty. Místo toho, aby se každý inzult opravil, poškozené a staré enterocyty odumírají apoptózou,poté jsou vytlačeny z epitelové vrstvy a průběžně nahrazovány novými. Sliznice tenkého střeva je vysoce skládaná a tvoří mnoho evaginací neboli klků a invaginací neboli žlázek, známých jako Lieberkühnovy krypty. V tlustém střevě jsou Lieberkühnovy krypty. Životní cyklus enterocytů začíná ve spodní části Lieberkühnových žlázek a končí v koncích klků tenkého střeva nebo na povrchu epitelu tlustého střeva. Život enterocytu trvá asi 2 až 5 dní. U člověka se střevní epitel obnovuje každých 4 až 5 dní.
Enterocyty se diferencují z dospělých kmenových buněk, které se nacházejí na dně Lieberkühnových žláz (obrázek 4). Zpočátku se z dospělých kmenových buněk stávají přechodné zesilující buňky (progenitorové buňky), které se nacházejí o něco dále od niky dospělých kmenových buněk. Přechodné amplifikující buňky se dělí 4 až 6krát, aby zvýšily progenitorovou populaci, a poté se diferencují v různé typy buněk, které se nacházejí ve střevním epitelu. Většina z nich se stává enterocyty, ale také globetovými buňkami, M buňkami a dalšími typy buněk. Nové enterocyty se postupně přesouvají směrem ke špičkám klků nebo k luminálnímu povrchu epitelu. Jakmile dosáhnou těchto pozic, odumírají a jsou z epitelu vytlačeny. Vytlačování zahrnuje jak mechanický tlak, tak ztrátu adhezního spojení se sousedními buňkami. Některé buňky odumírají apoptózou a poté jsou vytlačeny z epitelu. Není známo, jaký je mechanismus přesunu enterocytů ze žlázek na povrch epitelu. Molekulární složky bazální lamely se podél cesty enterocytů liší a předpokládá se, že mohou přispívat k pohybu. Předpokládá se, že na dynamice života enterocytů se podílí také strava.

Funkce
Trávení
Hlavní funkcí enterocytů je vstřebávání živin po žaludečním a enzymatickém trávení potravy. Enterocyty mohou jako zdroj energie využívat glutamát a glutamin, stejně jako mastné kyseliny a glukózu. To je zvláštní, protože všechny typy živin procházejí enterocyty. Pomáhají také při trávení tím, že vylučují enzymy, které rozkládají peptidy a disakaridy. Glykokalyx apikální domény enterocytů tvoří vrstvu silnou asi 400 až 500 nm, někdy i 1 µm. Některé enzymy, které se podílejí na trávení, jsou ukotveny v tomto glykokalyxu. Enterocyty tedy nejen vybírají a zachycují látky z tráveniny, ale některé z nich také zpracovávají. Ve skutečnosti se říká, že existují dvě fáze trávení, jedna probíhá v lumen střeva, kterou provádějí enzymy slinivky břišní, a druhá na povrchu enterocytů, kterou provádějí jiné trávicí enzymy. Většinu vstřebávání živin provádějí enterocyty tenkého střeva, zatímco enterocyty tlustého střeva vstřebávají především vodu. Kromě toho se z konců mikrovilů uvolňují malé vezikuly obsahující enzymy, jako jsou fosfatázy, které mohou mít obrannou funkci proti patogenům.
Látky vznikající při trávení musí projít střevním epitelem, aby se dostaly do krevního oběhu. Může se tak dít několika cestami: transcelulární, endocytózou/transcytózou a paracelulární.
Transcelulární. Většina molekul prochází epitelovou vrstvou střeva a prochází enterocyty. Nejprve překračují apikální membránu a poté bazolaterální. Molekuly se mohou přesouvat volnou pasivní difuzí, usnadněnou pasivní difuzí nebo aktivním transportem. Při volné pasivní difúzi molekuly překračují membrány bez jakékoliv pomoci, zatímco při usnadněném a aktivním transportu musí být molekuly rozpoznány specifickými přenašeči vloženými do membrán. Voda, ethanol a mnohé lipidy procházejí enterocyty volnou pasivní difuzí. Glukosa, některé lipidy a aminokyseliny vstupují do enterocytů facilitovaným pasivním transportem nebo aktivním transportem.
Apikální doména buňky nese soubor proteinů pro absorpci látek, zatímco laterobazální membrány mají další transmembránové přenašeče pro získání molekul z enterocytu.
Vstřebávací schopnost závisí na stupni diferenciace enterocytu, což znamená řadu sodíkových membránových pump, které jsou hojnější, čím více se enterocyty vzdalují od hloubky krypt. Většina vstřebávání cukrů a aminokyselin se tedy uskutečňuje v horní třetině klků tenkého střeva a při povrchu tlustého střeva. Například aktivita hydrolázy se zvyšuje s tím, jak se enterocyty vzdalují od niky kmenových buněk (hluboké části krypt).
Vstřebávání glukózy je příkladem typického mechanismu vstřebávání. Glukosa přechází přes apikální membránu enterocytu ko-transportem spojeným se sodíkovým gradientem. Tento gradient vytvářejí sodíkové/draslíkové pumpy a glukóza může vstupovat do enterocytu proti koncentračnímu gradientu glukózy. Tento ko-transport umožňuje sodíkový glukózový transportér (SGLT). Na druhé straně se v laterobazálních membránách nachází transportér GLUT2, který přenáší glukózu z cytoplazmy do mezibuněčného prostoru. SGLT tedy zvyšuje koncentraci glukózy v cytoplazmě enterocytů a GLUT2 umožňuje únik glukózy směrem k cévám. Přesné umístění obou transportérů vytváří tok glukózy enterocyty z lumen střeva do cév.
Tuk patří mezi nejvíce energetické látky, kromě toho je nezbytný pro buněčné membrány. Většina tuků z jídla, které se začleňují ze střeva, je ve formě triacylglycerolů, i když se mohou vstřebávat i jiné typy, například cholesterol. Nejprve pankreatické enzymy rozkládají tuk ve střevě a triacylglyceroly se přeměňují na mastné kyseliny a monoacylglyceroly (obrázek 5). Tyto molekuly spolu s cholesterolem, vitaminy rozpustnými v tucích a fosfolipidy tvoří micely, což jsou malé lipidové kapičky, které jsou díky žlučovým kyselinám rozpustné ve vodě. Micely volně procházejí apikální membránou enterocytů. Přenašeče CD36 y FABP (fatty acid binding protein) s 3umožňují některým tukovým látkám přecházet přes apikální membránu enterocytů usnadněným pasivním transportem. Většina transportu tuků probíhá ve formě micel, zatímco membránové přenašeče vypadají jako senzorický systém pro detekci mastných kyselin s 3s dlouhými řetězci ve střevě. Cholesterol jako jednotlivá molekula může být také transportován transportérem NPC1L1 (Niemann-Pick C1-like 1), který přenáší cholesterol z lumen střeva do cytoplazmy enterocytů.

Po vstupu do enterocytu se tuky spojí s některými bílkovinami a přesunou se do endoplazmatického retikula, kde se opět syntetizují triacylglyceroly. Ty se spojují s některými bílkovinami a vytvářejí prechylomikrony. Protein ApoB je syntetizován v endoplazmatickém retikulu. ApoB spolu s MTP (microsome tranfer protein) a mastnými kyselinami tvoří lipoproteinové pračástice. V hladkém endoplazmatickém retikulu je ApoB nahrazen proteinem Apo A-IV. Všechny tyto složky tvoří prechylomikrony, které jsou zahrnuty do vezikul a přesunuty do Golgiho aparátu. Zde se pre-chylomikrony spojují a vytvářejí chylomikrony, které jsou součástí exocytických vezikul a uvolňují se v laterobazální oblasti enterocytu. Tímto způsobem se chylomikrony mohou dostat do krve a lymfatických cév. Chylomikrony jsou lipoproteiny s tělem složeným převážně z triacylglycerolů a obalem z fosfolipdů, cholesterolu a apolipoproteinů. Hrají hlavní roli při transportu triacylglycerolů a vitamínů rozpustných v tucích.
Mimo enterocyt se chylomikrony dostávají do lymfatických cév střevních klků a poté do lymfatických myenterických plexů, z nichž přecházejí do krevních cév. Kromě chylomikronů jsou tuky baleny také do lipoproteinů o velmi nízké hustotě (VLDL), které jsou rovněž exocytovány z enterocytů. Tuk může být uložen také v lipidových kapénkách enterocytů.
Enterocyty také získávají železo po trávení. Železo je důležité pro mnoho bílkovin, např. hemoglobin, a může se nacházet v potravinách jako součást hemo skupin nebo vázané na feritin (v mase zvířat) (obr. 6). Železo se z tráveniny dostává do těla prostřednictvím transportéru DMT1 (transportér dvojmocných kovů 1), který se nachází v apikálních membránách enterocytů. U transgenních myší, kterým tento transportér chybí, dochází k těžké anémii. DMT1 je ko-transportér spojený s protonovým gradientem. Protonový gradient je vytvářen Na+/K+ pumpou, která se rovněž nachází v apikální membráně enterocytů. DMT1 transportuje Fe2+, ale většina železa z jídla je ve formě Fe3+. Redukci železa (Fe3+ na Fe2+) provádí enzym reduktáza nacházející se na apikálním povrchu enterocytu. Zdá se, že železo navázané na hemo skupiny je inkorporováno receptorem zprostředkovanou endocytózou. Po vstupu do enterocytu je hemo skupina rozložena a železo se může dostat do cytosolu.

Ať už je cesta vstupu jakákoli, po vstupu do cytosolu je pohyb železa směrem k bazolaterálním membránám zřejmě zprostředkován proteiny metalochaperony. V bazolaterálních membránách je železo translokováno do extracelulárního prostoru pomocí ferroportinového transportéru. Ferroportin odebírá formu Fe2+ . Feritin je však protein, který přenáší železo do systému portální žíly, a železo musí být ve formě Fe3+. V bazolaterálních membránách enterocytů se nacházejí ferrooxidázy, které umožňují přeměnu Fe2+ na Fe3+. Železo může být uloženo v cytosolu enterocytu vázané na feritin.
Endocytóza/transcytóza. Molekuly jako imunoglobuliny jsou endocytovány receptorem zprostředkovanou endocytózou a transportovány do jiných membránových domén transcytózou. Vezikuly se tvoří na bázi mikrovilů a později se spojují s endozomy. Imunoglobuliny jsou pak uzavřeny ve vezikulách vytvořených v endozomech a zaměřeny na membrány bazolaterálních domén. Tímto způsobem se imunoglobuliny vyhnou lysozomální degradační cestě.
Paracelulární. Voda a ionty procházejí epitelií paracelulární cestou.
Ochrana
Enterocyty vytvářejí bariéru odmítající antigeny, toxické molekuly a mikroorganismy a zároveň propouštějí výživné látky. Enterocyty jsou v kontaktu s mnoha mikroorganismy. Těmi, které jsou rezidentními mikroorganismy ve střevě, ale mohou být nebezpečné, pokud se dostanou do vnitřních tkání, a těmi nerezidentními patogeny, které přicházejí s potravou. Apikální povrch enterocytů je pokryt vrstvou slizových látek uvolňovaných buňkami globet. Tato vrstva se skládá ze sacharidů a má hustou viskozitu, která umožňuje difuzi molekul, ale odmítá buňky a největší molekuly. Mikrovily enterocytů navíc vykazují dobře vyvinutý glykokalyx v apikálních koncích každého mikrovilu, který působí jako fyzikální a elektrická bariéra, protože je plný záporných nábojů. Tyto mikrovily ztěžují přímý fyzický kontakt mezi mikroorganismy a membránou enterocytů. I když však mikroorganismy projdou těmito dvěma bariérami, měly by překonat transportní mechanismus mikrovilů.
Muciny jsou vysoce glykosylované proteiny, které se nacházejí v apikální membráně enterocytů. Přispívají k dobře vyvinutému glykokalyxu. Muciny jsou transmembránové proteiny spojené s cytoskeletem svou cytosolickou doménou. MUC3, MUC12 a MUC17 jsou nejhojněji zastoupené muciny. Obsahují asi 5000 aminokyselin a jejich sacharidová složka může sahat až 1 µm od povrchu buňky. Muciny tvoří fyzikální bariéru, kterou bakterie těžko překonávají.
Enterocyty jsou schopny spouštět a regulovat zánětlivé procesy uvolňováním několika chimocinů a cytokinů. Mají také receptory pro tyto molekuly. Enterocyty uvolňují prozánětlivé molekuly, které ovlivňují imunitní buňky nacházející se ve střevní sliznici.
Dalším méně známým ochranným mechanismem je uvolňování vezikul z apikálního povrchu enterocytů. Aktin a myozin, motorický aparát mikrovilů, vytvářejí mechanické síly, které táhnou membrány směrem ke špičce každého mikrovilu. Akumulace membrán končí ve formě vezikul, které se uvolňují do střevního lumen. Tyto vezikuly obsahují vysoké množství alkalické fosfatázy, která je silným antipatogenním činitelem tím, že snižuje toxicitu lipopolysacharidu a střevní zánět. Brání také přichycení bakterií k instestinálnímu epitelu a snižuje proliferaci bakterií. Vezikuly uvolňované enterocyty jsou způsobem, jak poslat molekuly proti mikrobům do oblastí vzdálených od epitelu.
Bibliografie
Barker N. 2014. Dospělé střevní kmenové buňky: kritické faktory homeostázy a regenerace epitelu. Nature. 15: 19-33.
Giammanco A, Cefalù AB, Noto D, Averna MR. 2015. Patofyziologie produkce střevníchlipoproteinů. Frontiers in physiology. 6: 61.
Knutson MD. 2014. Dospělé střevní kmenové buňky: kritické faktory homeostázy a regenerace epitelu. Nature review in molecular cell biology. 15:19-33.
Knutson MD. 2017. Transportní proteiny železa: brány buněčné a systémové homeostázy železa. Journal of biological chemistry Nature review in molecular cell biology. 292: 12735-12743.
Shifrin DA, McConell RE, Nambiar R, Higginbotham JN, Coffey RJ, Tyska MJ. 2012. Vezikuly odvozené z mikroprostředí enterocytů detoxikují bakteriální produkty a regulují interakce mezi epitelem a mikroby. Current biology. 22: 627-631.
Snoeck V, Goddeeries B, Cox E. 2005. Úloha enterocytů ve funkci střevní bariéry a vychytávání antigenů. Mikroby a infekce. 7: 997-1004.
Leave a Reply