Endocrinopatías: El nuevo precio del tratamiento del cáncer
Los inhibidores del punto de control inmunitario (ICI) son anticuerpos monoclonales que bloquean los puntos de control -en concreto, el antígeno 4 de los linfocitos T citotóxicos (CTLA-4), la proteína de muerte celular programada 1 (PD-1) y el ligando de la proteína de muerte celular programada 1 (PD-L1)-, lo que conduce a la desrepresión de la función de las células T citotóxicas y a la mejora de la respuesta inmunitaria antitumoral (figura 1).

Figura 1. Mecanismos de los inhibidores de puntos de control inmunitarios.
En 2011, la Administración de Alimentos y Medicamentos de Estados Unidos aprobó el primer ICI, el ipilimumab, para su uso en el melanoma. Desde entonces, se han aprobado cinco ICI para la práctica clínica, incluidos los inhibidores de PD-1 (pembrolizumab y nivolumab) y los inhibidores de PD-L1 (atezolizumab, avelumab y durvalumab).
Los ICI han surgido como una nueva causa de acontecimientos adversos endocrinos relacionados con la inmunidad (IRAE) que afectan a la hipófisis, la tiroides, el páncreas endocrino y (raramente) las glándulas suprarrenales y paratiroides. El mecanismo subyacente de estas endocrinopatías parece estar mediado por el sistema inmunitario, principalmente por las células T; sin embargo, los mecanismos específicos aún no se han dilucidado y son objeto de estudios recientes y en curso.
El aumento del uso de los ICI, que son muy eficaces contra diversas neoplasias, probablemente aumentará la carga poblacional de estas endocrinopatías. Por lo tanto, es esencial que los clínicos sean capaces de identificarlas e iniciar su tratamiento.
Monitoreo de las endocrinopatías
Antes de iniciar los ICI, los pacientes deben someterse a pruebas de laboratorio que incluyan TSH en suero, tiroxina libre en suero, cortisol 8 AM en suero, ACTH en suero y glucosa en plasma en ayunas. Si alguna de estas pruebas es anormal, se pueden realizar más pruebas y controles. También deben realizarse pruebas de laboratorio específicas cuando haya síntomas o signos de cualquier endocrinopatía, como se comentará más adelante.
El clínico debe tener un umbral bajo para realizar pruebas de endocrinopatía si el paciente tiene antecedentes personales o familiares de autoinmunidad o ha desarrollado otras EIR. Sobre la base de nuestra experiencia clínica y de las directrices de la National Comprehensive Cancer Network, puede ser necesario interrumpir temporalmente el ICI iniciador si un paciente presenta hipofisitis con efectos de masa, crisis suprarrenal, tirotoxicosis grave o cetoacidosis diabética.
Hipofisitis
La hipofisitis es la endocrinopatía más común asociada al inhibidor de CTLA-4 ipilimumab, y se presenta en el 8%-11% de los pacientes. Se observa con menos frecuencia con los inhibidores de PD-1 y PD-L1 (0%-5%). Aunque la hipofisitis suele producirse entre 6 y 12 semanas después del inicio de los ICI, se han notificado algunos casos tras una duración prolongada del tratamiento.
Presentación y manejo
La hipofisitis puede presentarse con efectos de masa debido al agrandamiento de la hipófisis, con dolor de cabeza, visión doble y defectos del campo visual. Tanto si hay efectos de masa como si no, todos los casos tienen deficiencias hormonales hipofisarias -más comúnmente insuficiencia suprarrenal secundaria, que puede presentarse como una emergencia de «crisis suprarrenal». También puede causar hipotiroidismo central y a veces hipogonadismo secundario.
Pueden aparecer síntomas como fatiga, debilidad, náuseas, confusión, pérdida de memoria, pérdida de libido, anorexia, alucinaciones, intolerancia a la temperatura y sensación subjetiva de fiebre y escalofríos. Estos síntomas son a menudo inespecíficos y pueden superponerse a los síntomas constitucionales relacionados con el cáncer.
Por lo tanto, el clínico debe tener una alta sospecha al evaluar la hipofisitis, especialmente porque la insuficiencia suprarrenal secundaria que la acompaña puede ser potencialmente mortal si no se reconoce y se trata con prontitud. La hipófisis posterior no suele estar implicada, por lo que la diabetes insípida central es infrecuente en el contexto del uso de ICI.
Las pruebas de diagnóstico deben incluir una IRM cerebral (Figura 2) y pruebas de las hormonas producidas por la hipófisis y las glándulas diana.
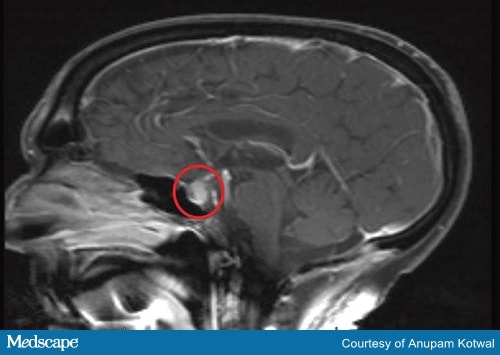
Figura 2a. Resonancia magnética de la cabeza, que demuestra el agrandamiento y el realce de la hipófisis, con engrosamiento del tallo.
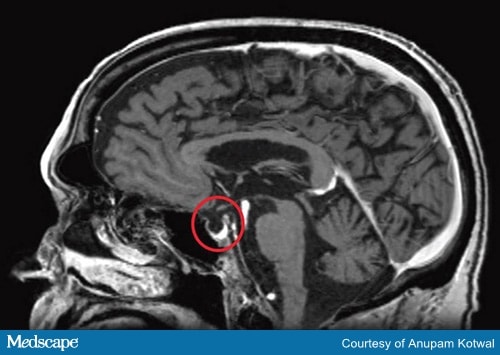
Figura 2b. Resonancia magnética de la cabeza, que demuestra la destrucción de la glándula pituitaria, con la apariencia de una silla turca vacía.
Además de las anomalías hormonales, pueden producirse anomalías electrolíticas como hiponatremia e hipoglucemia debido a una deficiencia de cortisol y tiroxina.
Cuando un paciente presenta efectos masivos como cefalea o anomalías de la visión, debe considerarse la hospitalización. Deben administrarse dosis altas de glucocorticoides (p. ej., prednisona/metilprednisolona 1 mg/kg/día o dexametasona 4 mg cada 6 horas) tan pronto como exista la preocupación de que se produzcan efectos de masa por la hipofisitis.
Los pacientes que presentan hipotensión, confusión e hipoglucemia pueden estar en crisis suprarrenal, que debe tratarse con una dosis de estrés de glucocorticoides y reanimación con líquidos. Una vez que la crisis suprarrenal y los efectos de masa se resuelven, o si el paciente presenta sólo síntomas leves o moderados de deficiencias hormonales, el reemplazo hormonal es el pilar del tratamiento. La mayoría de los pacientes que desarrollan hipopituitarismo requieren una sustitución hormonal de por vida.
Tiroiditis
La disfunción tiroidea es la endocrinopatía más común asociada a los inhibidores de PD-1 y PD-L1 (6%-21%). Ocurre con menos frecuencia con el inhibidor de CTLA-4 ipilimumab. El tratamiento combinado con ipilimumab y un inhibidor de PD-1 ha demostrado las tasas más elevadas de disfunción tiroidea, que suele producirse entre 8 y 10 semanas después del inicio de un ICI, pero puede retrasarse hasta 2 años.
Presentación y manejo
La tiroiditis puede presentarse con hipotiroidismo primario, a veces precedido por una fase tirotóxica durante la cual se liberan hormonas tiroideas. Los pacientes con tiroiditis de Hashimoto preexistente pueden presentar un empeoramiento del hipotiroidismo, sugerido por un aumento de la dosis de sustitución de hormonas tiroideas.
Parece haber un mayor riesgo de progresión a hipotiroidismo permanente en la tiroiditis inducida por ICI en comparación con la tiroiditis indolora, y esto es especialmente cierto cuando los anticuerpos contra la peroxidasa tiroidea (TPO) están elevados. El hipertiroidismo persistente, como la enfermedad de Graves, se ha notificado raramente con el uso de inhibidores de CTLA-4.
Muchos pacientes son asintomáticos debido a la naturaleza aguda o leve de la disfunción de la hormona tiroidea, lo que pone de relieve la importancia de controlar los niveles de la hormona tiroidea antes de cada infusión de ICI. La mayoría de los pacientes que presentan o evolucionan hacia un hipotiroidismo manifiesto requieren una sustitución de la hormona tiroidea a largo plazo.
El diagnóstico puede establecerse fácilmente mediante pruebas de función tiroidea. Los anticuerpos del receptor de la TSH sólo deben analizarse cuando el hipertiroidismo es persistente durante más de 8 semanas, en cuyo caso una prueba de anticuerpos del receptor de la TSH positiva sugeriría la existencia de la enfermedad de Graves.
El diagnóstico por imagen no suele ser necesario para establecer un diagnóstico de tiroiditis inducida por ICI. En algunos casos, la ecografía tiroidea puede ayudar a confirmar el diagnóstico de tiroiditis, ya que el tiroides aparece heterogéneo e hipovascular (Figura 3).
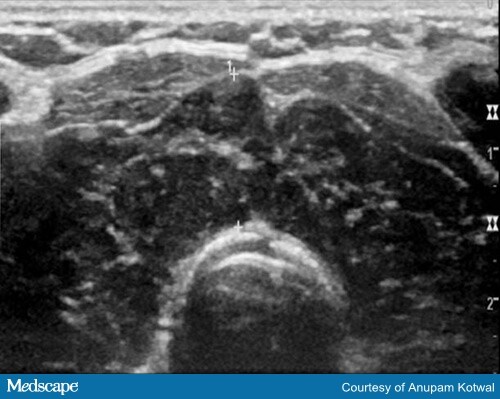
Figura 3. Imagen ecográfica que demuestra un parénquima de la glándula tiroidea heterogéneo e hipoecoico, que también es hipovascular.
Las exploraciones FDG-PET realizadas como parte de un estudio de malignidad o de seguimiento suelen demostrar un aumento difuso de la captación de FDG en la tiroides, consistente con la tiroiditis (Figura 4).

Figura 4. Gammagrafía FDG-PET que demuestra un aumento difuso de la captación de FDG en la tiroides.
El manejo depende de la fase de la tiroiditis durante la cual se hace el diagnóstico. La tirotoxicosis transitoria puede tratarse normalmente de forma sintomática con betabloqueantes. Si hay molestias significativas en el cuello, lo que es poco frecuente, se puede considerar el uso de glucocorticoides, pero normalmente no son necesarios.
Para el hipotiroidismo manifiesto o el hipotiroidismo subclínico sintomático, debe iniciarse la terapia de sustitución de T4 con levotiroxina y su dosis debe titularse en función de la TSH.
Diabetes mellitus dependiente de la insulina
No se ha notificado la aparición de diabetes mellitus en los ensayos clínicos de los inhibidores de CTLA-4 y se ha notificado en el < 1% de los pacientes en los estudios de los inhibidores de PD-1. Sin embargo, recientemente se han notificado tasas de hasta el 1,5% con el uso combinado de inhibidores de CTLA-4 y PD-1.
Se ha demostrado que los inhibidores de PD-L1 no sólo provocan una diabetes insulinodependiente de nueva aparición, sino que también empeoran la diabetes preexistente. Los títulos elevados de anticuerpos asociados a la diabetes tipo 1 que se observan con frecuencia están en consonancia con el proceso inmunitario.
La diabetes insulinodependiente de nueva aparición suele producirse 20 semanas después de iniciar el tratamiento con inhibidores de PD-1, pero se ha informado de casos tan tempranos como 2 semanas y tan tardíos como 3-4 años después del inicio del tratamiento.
Presentación y manejo
Dependiendo de la gravedad de la deficiencia de insulina, puede producirse una emergencia por cetoacidosis diabética y se ha notificado con bastante frecuencia.
Se recomienda que los pacientes con ICI que presenten hiperglucemia se sometan a pruebas de hemoglobina A1c (normalmente no muy elevadas debido a la naturaleza aguda de la hiperglucemia), péptido C (normalmente bajo) con glucosa plasmática concomitante y anticuerpos de diabetes tipo 1. Cuando hay alguna preocupación por la cetoacidosis diabética, se debe analizar el bicarbonato sérico, la brecha aniónica, el beta-hidroxibutirato y las cetonas en orina. Los médicos deben tener un umbral bajo para tratar a estos pacientes como si tuvieran diabetes deficiente de insulina en su presentación inicial.
Una vez que el episodio inicial de hiperglucemia se ha resuelto -y si los anticuerpos son negativos y los niveles de péptido C sugieren una producción adecuada de insulina, especialmente en ausencia de hiperglucemia preprandial- se puede considerar una desescalada cautelosa de la terapia, pero los pacientes deben ser vigilados muy de cerca porque pueden estar en la «fase de luna de miel» de la deficiencia de insulina.
La mayoría de los pacientes con diabetes inducida por ICI requieren una terapia intensiva de insulina con un régimen de bolos basales o una bomba de insulina en el seguimiento, lo que sugiere que la remisión es poco probable. Esto aumenta significativamente la morbilidad de los pacientes que ya están lidiando con el cáncer.
Endocrinopatías raras: Adrenalitis e Hipoparatiroidismo
En algunos informes de casos se ha descrito una presentación clínica sugestiva de insuficiencia suprarrenal primaria, pero suele ser difícil de diferenciar de la insuficiencia suprarrenal secundaria debida a hipofisitis o al uso crónico de glucocorticoides (para el cáncer o el manejo de otras ERI).
Recientemente, se han notificado dos casos de hipocalcemia y baja hormona paratiroidea sugestivos de hipoparatiroidismo inmunomediado con el uso de inhibidores de PD-1, uno de ellos mostrando anticuerpos contra el receptor sensor del calcio.
Siga Medscape en Facebook, Twitter, Instagram y YouTube
Leave a Reply