Frontiers in Immunology
Introduktion
I avsaknad av primärprevention genom immunisering och en specifik behandling för COVID-19 kan rationella behandlingsstrategier ändå vara tillgängliga. Förutom terapier för att direkt påverka virusreplikationen , har immunterapier föreslagits för att minska effekterna av den virusinducerade inflammationen (2). Dessa inkluderar kortikosteroidbehandling, som inte rekommenderas på grund av deras immunosuppressiva effekter, som kan leda till sämre resultat jämfört med obehandlade försökspersoner. Mer specifika metoder är inriktade på IL-6, TNFα, Januskinashämmare (JAK1/JAK2) och typ 1-inteferoner . Slutligen har komplementsystemet betraktats som en måltavla (3-5). Dessa parametrar kan vara av prognostisk betydelse, eftersom förhållandet mellan IL6/interferon IFɤ tycks förutsäga sjukdomens svårighetsgrad (6).
Den insikt att viruset utnyttjar det membranbundna angiotensinkonverterande enzymet 2 (ACE2) som ingångspunkt öppnar dessutom upp för potentiella strategier för att modifiera aktiviteten hos detta system. Det har föreslagits att användningen av angiotensinreceptorblockerare, som leder till ett uppreglerat uttryck av ACE2, kan vara skadlig (7). Den alternativa synen på en potentiellt gynnsam effekt av dessa föreningar har också uttryckts (8), baserad på de fysiologiskt antiinflammatoriska och skyddande effekterna av detta enzym. Denna kontrovers har nyligen beskrivits tydligt (9, 10). Utmaningen är att minska ACE2 som en ingångspunkt utan att förvärra den inflammatoriska reaktionen, när en infektion väl har inträffat.
ACE2-reduktion för att minska Covid-19 Entry?
Följande mekanistiska rön skulle en minskning av ACE2-uttrycket minska antalet ingångar för viruset till kroppen under den primära infektionen och potentiellt spridningen i kroppen. Båda bör leda till ett potentiellt mildare kliniskt förlopp. Celler som är mottagliga för infektion med SARS tycks i första hand vara typ II-pneumocyter, ileala absorptiva enterocyter och sekretoriska celler i nasala gobletceller (11). Därför kan det vara värt att identifiera en mekanism för att minska uttrycket av ACE2 i membranen i dessa celler (med eventuella negativa konsekvenser i åtanke). För att öka rimligheten i ett sådant tillvägagångssätt skulle det vara lämpligt att följa rapporterna om framgångsrik användning av traditionell kinesisk medicin (TCM). En av de mest använda föreningarna inom TCM innehåller ett extrakt från glycyrrhiza glabra, dvs. lakritsväxten (12) och interagerar med angiotensin-aldosteronsystemet: En av dess aktiva beståndsdelar är glycyrrhizin (GL), som metaboliseras i människans tarm till den systemiskt aktiva metaboliten glycyrrhetinsyra (GA). GL- och GA-administrering har ett antal relevanta effekter: GA hämmar främst ett enzym som kallas 11-beta-hydroxysteroiddehydrogenas (11bHSD), både typ 1 och 2 (13). Av betydelse här är typ 2 (11bHSD2). Dess hämning gör det möjligt för kortisol att få tillgång till mineralokortikoidreceptorer (MR) i aldosteronspecifik perifer vävnad, inklusive njurar, lungor, näs- och endotelceller, där det annars skulle vara förhindrat att göra det. Detta genom dess aktivitet att snabbt bryta ned kortisol intracellulärt för att ge aldosteron tillgång till receptorn. Med andra ord leder en hämning av detta enzym till en aldosteronliknande aktivering av MR via kortisol och kan likna effekterna av höga aldosteronnivåer i dessa organ. Av intresse i detta sammanhang är att höga aldosteronnivåer leder till en nedreglering av ACE2 i njuren (14), en vävnad som uttrycker 11bHSD2 liksom lungor och nasala epitelceller, dvs. huvudingångarna för COVID-19, medan MR-antagonism har motsatt effekt i flera vävnader (15). Detta stämmer överens med observationen att aldosteronreducerande föreningar, som enalapril, under vissa omständigheter kan leda till en ökning av ACE2-uttrycket (16, 17).
Direkt antiviral effekt av GA eller GL
Det är intressant att GL eller dess aktiva metabolit GA uttrycker antivirala effekter för det besläktade SARS-corona-viruset (18, 19) i cellkultur: En liknande effekt har beskrivits av Chen et al. i en Vero-E6-cellinje, men ingen effekt observerades i en fRhK4-cellinje (19). Viktigt är att GA, den systemiskt aktiva föreningen efter oral administrering, inte studerades, vilket gör dessa resultat potentiellt relevanta för lokal (inhalerad) eller intravenös administrering. I en studie med celler från de mänskliga luftvägarna visade GA, men inte GL, en effekt på infektionshastigheten med det mänskliga respiratoriska syncytialviruset (20). Dessa direkta antivirala effekter utanför MR pekar på en ytterligare, men okänd mekanism. I detta sammanhang kan det vara viktigt att notera att förutom ACE2 krävs serinproteaset TMPRSS2 för infektion av en cell (21). Hämning av detta enzym med en proteashämmare som ett terapeutiskt ingrepp har föreslagits av författarna. TMPRSS2 har varit involverad i både corona- och influensavirusinfektioner (22). Intressant nog regleras uttrycket av detta enzym av GA (23), vilket kan förklara de bredare antivirala effekterna av GL (24). Det regleras av androgener (23), vilket delvis kan förklara könsskillnaderna i det kliniska uttrycket av COVID-19-infektioner.
ACE2 Antiinflammation och glycyrrhizins antiinflammatoriska effekter
Den nedströmsrelaterade konsekvensen av minskat ACE2-uttryck är, som skisserats ovan, något kontroversiell (25). ACE2-aktivitet är generellt sett skyddande, även för lungvävnad (26). Det gör den genom att undertrycka konsekvenserna av aktiveringen av receptorn för endotoxin (LPS), dvs. toll-like receptor 4 (TLR4) och som en följd därav relaterad inflammation i lungan (endotoxin storm) (27): Övertryck av ACE2 hämmade den LPS-inducerade inflammationen i den här studien. Därför kan det minskade uttrycket av ACE2 betraktas som oroande. I detta sammanhang blir en annan egenskap hos glycyrrhizin viktig, nämligen dess immunmodulerande effekt. Den mest kända av dessa är dess antagonistiska effekt på TLR4-beroende mekanismer. En TLR4-antagonistisk effekt av GA minskar inflammation i flera vävnader, inklusive lungan (28). Dessutom leder GL till en minskning av TLR4-uttrycket i hjärtat och lungan i en LPS-modell av inflammation. Detta åtföljdes av en betydande minskning av cytokinfrisättning, dvs. frisättning av TNFα, IL6 och IL1ß (29). I enlighet med detta har GL skyddande effekter vid akut respiratoriskt nödsyndrom inducerat av TLR4-aktivatorn LPS hos möss (28). Den antiinflammatoriska potentialen inom lungan påvisades också i en musmodell av Streptococcus aureus-infektion, där intraperitoneal administrering av GL undertryckte inflammatoriska markörer på bred front (30). Dessa resultat ligger i linje med GL:s eller GA:s förmåga att hämma inflammatoriska vägar via TLR4 (31-34). GL:s mekanism mot lung- och hjärtinflammation kan delvis vara indirekt genom att förändra förhållandet mellan myeloida suppressorceller (MDSC) och CD11b+Gr1 myeloida celler (29). Sammantaget kan GL:s verkan för att hämma TLR4-aktiviteten inducera en antiinflammatorisk aktivitet nedströms den mindre aktiva ACE2 (35). Dessutom leder GA till ett undertryckande av den klassiska, men inte den alternativa komplementvägen (36). Slutligen har en påverkan på interferonutsöndringen beskrivits: glycyrrhizaextrakt leder till en ökad utsöndring av interferon 1ß i celler i de övre och nedre luftvägarna (20), vilket liknar effekten av GL och GA hos möss, vilket fastställs i serumprover (37); dessutom minskar GL dödsfallet hos möss som infekterats med en dödlig dos influensavirus på ett interferon ɤ- och T-cellsberoende sätt (38). Dessa antiinflammatoriska mekanismer kan också vara av betydelse i CNS (39, 40) och kan därför skydda mot neurologiska och psykiatriska konsekvenser av en COVID-19-infektion.
Från ett mer praktiskt perspektiv kan det också vara relevant att coronaviruset SARS Co-V, som har likheter med COVID-19, ofta ledde till arteriell hypotension (25), vilket inte är ovanligt vid inflammatoriska processer. Detta potentiellt kritiska symptom kan också övervinnas med glycyrrhizin, som leder till en ökning av blodtrycket (13). Se figur 1 för en schematisk översikt.
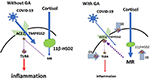
Figur 1. Schematisk modell av effekten av glycyrrhizin: COVID-19-tillträde till cellerna förmedlas via ACE2 med TMPRSS2 som kofaktor. Uttrycket av ACE2 regleras av mineralokortikoidreceptorer (MR): MR-aktivering leder till en minskning av ACE2-uttrycket; GA hämmar 11βHSD2, vilket gör det möjligt för kortisol att aktivera MR, följt av ACE2-nedreglering (pil 1). TMPRSS2 sensibiliserar ACE2 för uppdatering av viruset i cellen. GA leder till ett minskat uttryck av TMPRSS2 och kan därför utgöra ytterligare en mekanism för att begränsa virusets tillträde till cellen (pil 2). ACE2 har en antiinflammatorisk mekanism genom generering av angiotensin 1-7 och angiotensin 1-9. Via aktivering av MAS- eller angiotensin 2-receptorer undertrycks inflammatoriska vägar. Detta innefattar också ett minskat uttryck och/eller aktivering av membranens TLR4-receptor (vänster), dvs. det minskade uttrycket av ACE2 kan betraktas som problematiskt (35). GA hämmar dock direkt TLR4 oberoende av ACE2-aktivering (pil 3). (ϕ och avbrutna linjer symboliserar hämning; röda kontinuerliga linjer symboliserar aktivering).
Diskussion
Många frågor förblir öppna. Vilken roll spelar lösligt respektive membranbundet ACE2? Kan det finnas en roll för lösligt ACE2 att skydda membranbeläggning? Detta har nyligen föreslagits på grundval av fynd i cellodlingsexperiment (41). Detta kan dock till viss del motsäga observationen att personer med hjärtsvikt, som bör betraktas som högriskpersoner, uppvisar höga nivåer av lösligt ACE2 (42). Vad är skillnaden i olika organ med eller utan uttryck av 11bHSD2? Vilken roll spelar den samtidiga motreglerande minskningen av aldosteron i plasma vid administrering av en 11betaHSD2-hämmare? Dessa frågor kan besvaras i lämpliga kliniska prövningar. Bestämning av slutprodukten av ACE2-enzymet, dvs. angiotensin 1-7 samt potentiella kliniska konsekvenser på blodtrycket kan vara till hjälp för att klargöra några av dessa frågor.
Väsentligt är att glycyrrhizin har en övergripande väl tolererad. Det har ett FDA-utlåtande om GRAS (allmänt betraktas som säkert) (13). I synnerhet är en dos upp till 100 mg/dag som används kroniskt säker och leder inte till förändringar, vilket har observerats vid kronisk användning i högre doser. De förväntade oönskade effekterna av höga doser, inklusive hypertoni och hypokalemi, bör dock övervakas. I samband med SARS har en oral dos på upp till 300 mg rekommenderats för oral administrering och cirka 240 mg för intravenös administrering (19). Chen et al. anger dock att denna dos för intravenös administrering kan vara för låg, med hänsyn till EC50 för effekten på virusreplikation. Det måste sägas att denna direkta effekt endast är en av tre relevanta mekanismer för att rikta in sig på den COVID-19-relaterade sjukdomsprocessen. Två öppna kliniska prövningar är registrerade på WHO:s webbplats för registrering av kliniska prövningar, en randomiserad öppen prövning (ChiCTR2000029768) och en fallserie (ChiCTR2000030490). För studien används en dos på 300 mg glycyrrhizin oralt/dag, dosen för den andra undersökningen har inte rapporterats. När det gäller valet av administreringsväg är det viktigt att beakta att för en GA-inducerad verkan är den orala administreringen av GL avgörande, eftersom GL inte metaboliseras till GA systemiskt. För en lokaliserad effekt av GL kan dock en intravenös eller inhalerad administrering krävas, som bör kombineras med en oral administrering. För användning av en potentiell primärprevention kan ett pragmatiskt dosval på 150 mg/dag oralt övervägas för ytterligare studier, eftersom denna dos påverkar MR-aktiviteten.
Slutsats
Glycyrrhizin är en allmänt tillgänglig och överlag säker förening. Den kan eventuellt minska uttrycket av ACE2 i lungan och trots det minska lunginflammation. Det borde vara värt att överväga att studera denna förening för en typ av primärprevention, som inte nödvändigtvis minskar risken för att bli smittad, men potentiellt sjukdomens svårighetsgrad och i att minska redan existerande symtom. Detta skulle kunna bidra till att minska antalet kritiskt sjuka patienter, som för närvarande överväldigar sjukvårdssystemet.
Författarbidrag
HM har utarbetat manuskriptet och den slutliga versionen.
Intressekonflikter
HM innehar ett patent för användning av glycyrrhizin vid terapirefraktär depression.
Författaren förklarar att forskningen utfördes i avsaknad av kommersiella eller ekonomiska relationer som skulle kunna tolkas som en potentiell intressekonflikt.
Acknowledgments
HM vill tacka Laura Zumpano för hennes genomgång och hjälpsamma kommentarer till manuskriptet.
1. Sanders JM, Monogue ML, Jodlowski TZ, Cutrell JB. Farmakologiska behandlingar för coronavirus sjukdom 2019 (COVID-19): en översikt. JAMA. (2020). doi: 10.1001/jama.2020.6019. .
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Reddy Bonam S, Kaveri SV, Sakuntabhai A, Gilardin L, Bayry J. Adjungerade immunterapier för behandling av svårt sjuka COVID-19-patienter. Cell Rep Med. (2020) 7:22. doi: 10.1016/j.xcrm.2020.100016
CrossRef Full Text | Google Scholar
3. Maglakelidze N, Manto KM, Craig TJ. En översyn: Har komplement eller kontaktsystemet en roll i skydd eller patogenes av COVID-19? Pulm Ther. (2020) 1-8. doi: 10.1007/s41030-020-00118-5
CrossRef Full Text | Google Scholar
4. Mastaglio S, Ruggeri A, Risitano AM, Angelillo P, Yancopoulou D, Mastellos DC, et al. Det första fallet av COVID-19 som behandlats med komplement C3-hämmaren AMY-101. Clin Immunol. (2020) 215:108450. doi: 10.1016/j.clim.2020.108450
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Risitano AM, Mastellos DC, Huber-Lang M, Yancopoulou D, Garlanda C, Ciceri F, et al. Complement as a target in COVID-19? (2020) Nat. Rev. Immunol. 1-2. doi: 10.1038/s41577-020-0320-7
CrossRef Full Text | Google Scholar
6. Lagunas-Rangel FA, Chavez-Valencia V. High IL-6/IFN-gamma ratio could be associated with severe disease in COVID-19 patients. J. Med. Virol. (2020). doi: 10.1002/jmv.25900. .
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Esler M, Esler D. Kan angiotensinreceptorblockerande läkemedel vara skadliga vid COVID-19-pandemin? J. Hypertens. (2020) 38:781-2. doi: 10.1097/HJH.0000000000002450
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Fedson DS, Opal SM, Rordam OM. Hiding in plain sight: ett tillvägagångssätt för behandling av patienter med allvarlig COVID-19-infektion. MBio. (2020) 11:e00398-20. doi: 10.1128/mBio.00398-20
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Sommerstein R, Kochen MM, Messerli FH, Grani C. Coronavirus disease 2019 (COVID-19): Har angiotensinkonverterande enzymhämmare/angiotensinreceptorblockerare en bifasisk effekt? J Am Heart Assoc. (2020) 9:e016509. doi: 10.1161/JAHA.120.016509
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Vaduganathan M, Vardeny O, Michel T, Mcmurray JJ, Pfeffer MA, Solomon SD. Hämmare av renin-angiotensin-aldosteronsystemet hos patienter med Covid-19. N Engl J Med. (2020) 382:1653-9. doi: 10.1056/NEJMsr2005760
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Ziegler CG. SARS-CoV-2-receptorn ACE2 är en interferonstimulerad gen i mänskliga luftvägsepitelceller och upptäcks i specifika cellundergrupper i olika vävnader. Cell. (2020) S0092-8674:30500-6. doi: 10.1016/j.cell.2020.04.035
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Luo H, Tang QL, Shang YX, Liang SB, Yang M, Robinson N, et al. Kan kinesisk medicin användas för att förebygga Corona virus disease 2019 (COVID-19)? En genomgång av historiska klassiker, forskningsbevis och nuvarande förebyggande program. Chin J Integr Med. (2020) 26:243-50. doi: 10.1007/s11655-020-3192-6
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Expertgrupp för granskning av kosmetiska ingredienser. Slutrapport om säkerhetsbedömning av glycyrrhetinsyra, kaliumglycyrrhetinat, disodiumsuccinoylglycyrrhetinat, glycerylglycyrrhetinat och glycyrrhetinylstearat, Stearylglycyrrhetinat, glycyrrhizinsyra, ammoniumglycyrrhizat, dikaliumglycyrrhizat, dikaliumglycyrrhizat, dinatriumglycyrrhizat, trinatriumglycyrrhizat, metylglycyrrhizat och kaliumglycyrrhizinat. Int J Toxicol. (2007) 26 (Suppl. 2):79-112. doi: 10.1080/10915810701351228
CrossRef Full Text | Google Scholar
14. Fukuda S, Horimai C, Harada K, Wakamatsu T, Fukasawa H, Muto S, et al. Aldosteroninducerad njurskada medieras av NFkappaB-aktivering. Clin Exp Nephrol. (2011) 15:41-9. doi: 10.1007/s10157-010-0373-1
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Keidar S, Gamliel-Lazarovich A, Kaplan M, Pavlotzky E, Hamoud S, Hayek T, et al. Mineralokortikoidreceptorblockerare ökar aktiviteten hos angiotensinkonverterande enzym 2 hos patienter med kongestiv hjärtsvikt. Circ Res. (2005) 97:946-53. doi: 10.1161/01.RES.0000187500.24964.7A
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Hu XS, Xie XD, Wang XX, Zeng CL, Ni YM, Yu GW, et al. Effekter av angiotensinkonverterande enzymhämmare på uttrycket av angiotensinkonverterande enzym 2 i förmaket hos patienter med förmaksflimmer. Zhonghua Xin Xue Guan Guan Bing Za Zhi. (2007) 35:625-8.
PubMed Abstract | Google Scholar
17. Malfitano C, De Angelis K, Fernandes T, Wichi RB, Rosa K, Pazzine M, et al. Lågdos enalapril minskar angiotensin II och dämpar diabetesinducerade hjärt- och autonoma dysfunktioner. J Cardiovasc Pharmacol. (2012) 59:58-65. doi: 10.1097/FJC.0b013e3182354776
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Cinatl J, Morgenstern B, Bauer G, Chandra P, Rabenau H, Doerr HW. Glycyrrhizin, en aktiv komponent i lakritsrötter, och replikation av SARS-associerat coronavirus. Lancet. (2003) 361:2045-6. doi: 10.1016/S0140-6736(03)13615-X
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Chen F, Chan KH, Jiang Y, Kao RY, Lu HT, Fan KW, et al. In vitro känslighet hos 10 kliniska isolat av SARS coronavirus för utvalda antivirala föreningar. J Clin Virol. (2004) 31:69-75. doi: 10.1016/j.jcv.2004.03.003
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Feng Yeh C, Wang KC, Chiang LC, Shieh DE, Yen MH, San Chang J. Vattenextrakt av lakrits hade antiviral aktivitet mot humant respiratoriskt syncytialvirus i cellinjer för mänskliga luftvägar. J Ethnopharmacol. (2013) 148:466-73. doi: 10.1016/j.jep.2013.04.040
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Hoffmann M, Kleine-Weber H, Schroeder S, Kruger N, Herrler T, Erichsen S, et al. SARS-CoV-2-cellinträde beror på ACE2 och TMPRSS2 och blockeras av en kliniskt beprövad proteashämmare. Cell. (2020) 181:271-80 e278. doi: 10.1016/j.cell.2020.02.052
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Shen LW, Mao HJ, Wu YL, Tanaka Y, Zhang W. TMPRSS2: ett potentiellt mål för behandling av infektioner med influensavirus och coronavirus. Biochimie. (2017) 142:1-10. doi: 10.1016/j.biochi.2017.07.016
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Sun Y, Jiang M, Park PH, Song K. Transkriptionellt undertryckande av androgenreceptorn av 18beta-glycyrrhetinsyra i mänskliga prostatacancerceller LNCaP. Arch Pharm Res. (2020) 43:433-48. doi: 10.1007/s12272-020-01228-z
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Hoever G, Baltina L, Michaelis M, Kondratenko R, Baltina L, Tolstikov GA, et al. Antiviral aktivitet hos glycyrrhizasyraderivat mot SARS-coronavirus. J Med Chem. (2005) 48:1256-9. doi: 10.1021/jm0493008
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Gurwitz D. Angiotensinreceptorblockerare som försök till terapi för SARS-CoV-2. Drug Dev. Res. (2020). doi: 10.1002/ddr.21656. .
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Kaparianos A, Argyropoulou E. Lokala renin-angiotensin II-system, angiotensinkonverterande enzym och dess homolog ACE2: deras potentiella roll i patogenesen för kroniska obstruktiva lungsjukdomar, pulmonell hypertoni och akut andningsnödsyndrom. Curr Med Chem. (2011) 18:3506-15. doi: 10.2174/092986711796642562
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Ye R, Liu Z. ACE2 uppvisar skyddseffekter mot LPS-inducerad akut lungskada hos möss genom att hämma LPS-TLR4-vägen. Exp Mol Pathol. (2020) 113:104350. doi: 10.1016/j.yexmp.2019.104350
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Yu Z, Ohtaki Y, Kai K, Sasano T, Shimauchi H, Yokochi T, et al. Trombocyternas kritiska roll i lipopolysackaridinducerad dödlighet: effekter av glycyrrhizin och möjlig strategi för akut andningsnödsyndrom. Int Immunopharmacol. (2005) 5:571-80. doi: 10.1016/j.intimp.2004.11.004
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Seo EH, Song GY, Kwak BO, Oh CS, Lee SH, Kim SH. Effekter av glycyrrhizin på differentieringen av myeloida celler i hjärta och lungor hos lipopolysackaridinducerade septiska möss. Chock. (2017) 48:371-6. doi: 10.1097/SHK.0000000000000850
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Yao L, Sun T. Glycyrrhizinadministration förbättrar Streptococcus aureus-inducerad akut lungskada. Int Immunopharmacol. (2019) 70:504-11. doi: 10.1016/j.intimp.2019.02.046
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Vitali R, Palone F, Pierdomenico M, Negroni A, Cucchiara S, Aloi M, et al. Dikaliumglycyrrhizat via HMGB1- eller AMPK-signalering undertrycker oxidativ stress under tarminflammation. Biochem Pharmacol. (2015) 97:292-9. doi: 10.1016/j.bcp.2015.07.039
CrossRef Full Text | Google Scholar
32. Wu CX, He LX, Guo H, Tian XX, Liu Q, Sun H. Inhibitionseffekt av glycyrrhizin i lipopolysackaridinducerad frisättning och uttryck av high-mobility group box 1 från RAW264.7-celler. Chock. (2015) 43:412-21. doi: 10.1097/SHK.0000000000000309
PubMed Abstract | CrossRef Full Text | Google Scholar
33. Thakur V, Nargis S, Gonzalez M, Pradhan S, Terreros D, Chattopadhyay M. Glycyrrhizins roll i minskningen av inflammation vid diabetisk njursjukdom. Nephron. (2017) 137:137-47. doi: 10.1159/000477820
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Wang XR, Hao HG, Chu L. Glycyrrhizin hämmar LPS-inducerad produktion av inflammatoriska mediatorer i endometriala epitelceller. Microb Pathog. (2017) 109:110-3. doi: 10.1016/j.micpath.2017.05.032
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Ingraham NE, Lotfi-Emran S, Thielen BK, Techar K, Morris RS, Holtan SG, et al. Immunmodulering i COVID-19. Lancet Respir Med. (2020) S2213-2600:30226-5. doi: 10.1016/S2213-2600(20)30226-5
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Kroes BH, Beukelman CJ, Van Den Berg AJ, Wolbink GJ, Van Dijk H, Labadie RP. Hämning av humant komplement med betaglycyrrhetinsyra. Immunologi. (1997) 90:115-20. doi: 10.1046/j.1365-2567.1997.00131.x
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Abe N, Ebina T, Ishida N. Interferoninduktion av glycyrrhizin och glycyrrhetinsyra hos möss. Microbiol Immunol. (1982) 26:535-9. doi: 10.1111/j.1348-0421.1982.tb00207.x
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Utsunomiya T, Kobayashi M, Pollard RB, Suzuki F. Glycyrrhizin, en aktiv komponent i lakritsrötter, minskar morbiditet och mortalitet hos möss som infekterats med letala doser av influensavirus. Antimicrob Agents Chemother. (1997) 41:551-6. doi: 10.1128/AAC.41.3.551
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Kong ZH, Chen X, Hua HP, Liang L, Liu LJ. Den orala förbehandlingen av glycyrrhizin förhindrar kirurgiskt inducerad kognitiv försämring hos åldrade möss genom att minska neuroinflammation och Alzheimersrelaterad patologi via HMGB1-hämning. J Mol Neurosci. (2017) 63:385-95. doi: 10.1007/s12031-017-0989-7
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Lai S, Wu G, Jiang Z. Glycyrrhizinbehandling underlättar utplåning av betingade rädsloreaktioner efter en enda långvarig stressexponering hos råttor. Cell Physiol Biochem. (2018) 45:2529-39. doi: 10.1159/000488271
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Monteil V, Kwon H, Prado P, Hagelkruys A, Wimmer RA, Stahl M, et al. Inhibering av SARS-CoV-2-infektioner i konstruerade mänskliga vävnader med hjälp av lösligt humant ACE2 av klinisk kvalitet. Cell. (2020) 181:905-913.e7. doi: 10.1016/j.cell.2020.04.004
PubMed Abstract | CrossRef Full Text | Google Scholar
42. Epelman S, Tang WH, Chen SY, Van Lente F, Francis GS, Sen S. Detection of soluble angiotensin-converting enzyme 2 in heart failure: insights into the endogenous counter-regulatory pathway of the renin-angiotensin-aldosterone system. J Am Coll Cardiol. (2008) 52:750-4. doi: 10.1016/j.jacc.2008.02.088
PubMed Abstract | CrossRef Full Text | Google Scholar
Leave a Reply