Cancer Cachexia
One Page Owner – Anthonia Abraham som en del av One Page Project
Definition
Cancer cachexia eller cancerassocierad trötthet definieras som ett multifaktoriellt syndrom som kännetecknas av en pågående förlust av skelettmuskelmassa (med eller utan förlust av fettmassa) som inte kan vändas helt och hållet med hjälp av konventionellt näringsstöd och som leder till progressivt funktionsbortfall.
Det karakteristiska draget är den negativa protein-energibalansen som uppstår på grund av minskat födointag och en onormal ämnesomsättning.
Klassificering
Det finns 3 stadier av klinisk relevans som bildar ett spektrum, men alla dessa personer genomkorsar inte hela spektrumet.
- Precachecia: De tidiga kliniska tecknen som anorexi och metabola tecken som försämrat glukostest föregår viktförlust (≤5 %). Progressionen varierar och beror på cancertyp och stadieindelning, lågt födointag, eventuell systemisk inflammation, dåligt svar på anti-cancerbehandling.
- Kachexi: En stabil viktminskning på mer än 5 % under 6 månader ELLER ett Body mass index (BMI) på mindre än 20 kg/m² ELLER sacrcopeni och pågående viktminskning på mer än 2 %, men som ännu inte gått in i det refraktära stadiet som klassificeras som kachexi.
- Refraktär kachexi: Mycket avancerad cancer ELLER snabbt progressiv cancer som inte svarar på cancerbehandling. Förknippad med aktiv katabolism och de faktorer som är förknippade med aktiv hantering av viktnedgång står här inte längre lämpligt. Låg prestationsstatus och en förväntad livslängd på mindre än 3 månader är karakteristiska.
Patofysiologi
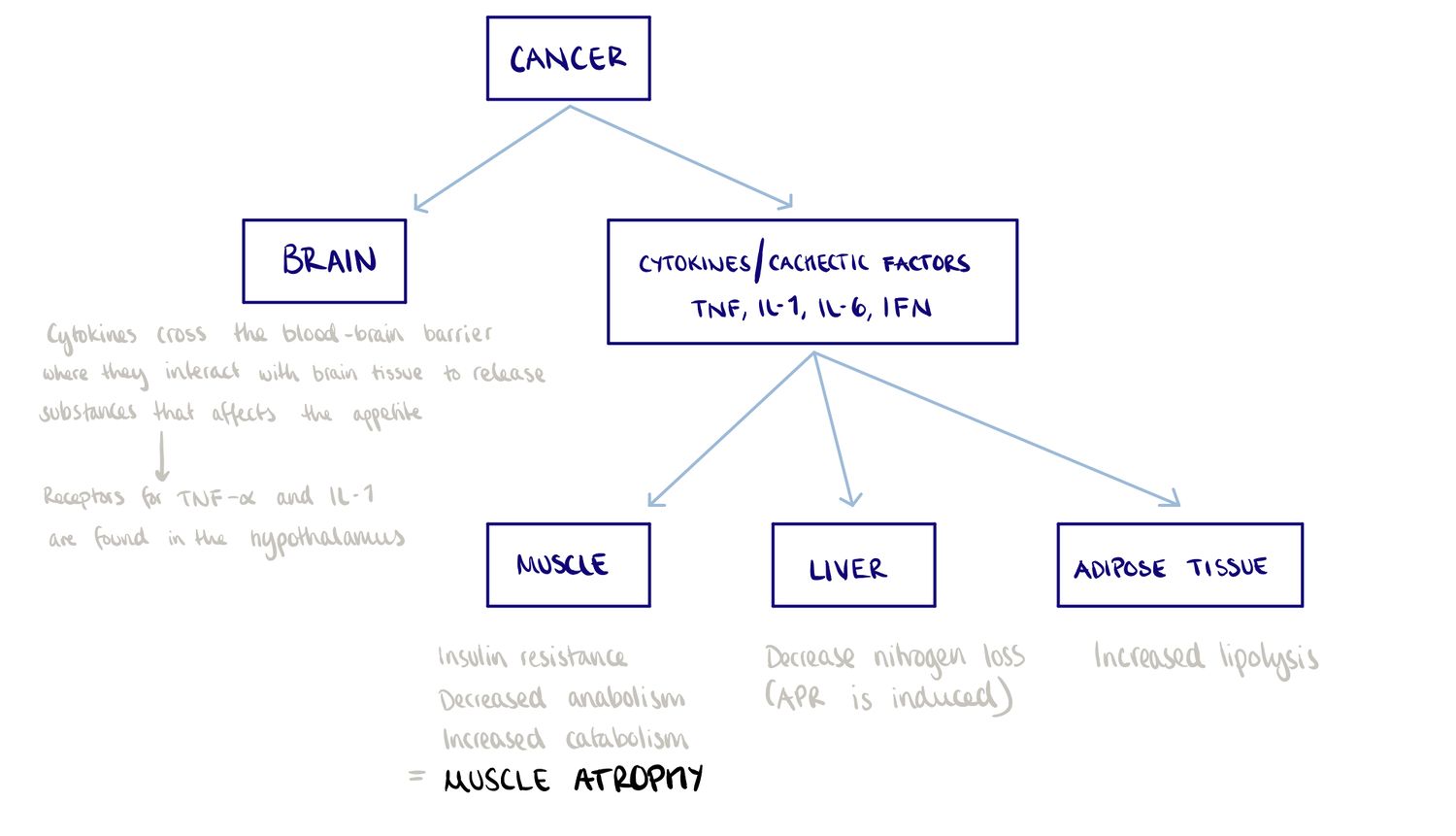
Diagnos av cancerkakexi
- BMI <20 och någon grad av viktnedgång >2%;
- Viktnedgång >5% under de senaste 6 månaderna (i avsaknad av enkel svält)
- Index för skelettmuskulatur i blindtarmen som är förenligt med sarkopeni (män <7-26 kg/m²; kvinnor <5-45 kg/m²) och varje grad av viktminskning >2%
Bedömning
Muskelmassa och muskelstyrka: Tvärsnittsbilder CT eller MRT, röntgenbilder med dubbla energier, bioimpedansanalys och antropometri som huvudsakligen omfattar omkrets i mitten av armen.
Anorexi och minskat födointag:
Anorexi och minskat födointag:
Anorexi och minskat födointag: Kvantifiering av protein kan vara relevant. Mekanismerna bakom detta kan vara kemosensoriska störningar, minskad rörlighet i övre mag-tarmkanalen, dysmobilitet i distala trakten. De sekundära orsakerna inkluderar stomatit, consti
Hantering
Det finns 4 grundläggande steg i behandlingsstrategier:
- Korrigera orsaken till det försämrade näringsintaget
- Att ge adekvat näringsstöd
- Multimodal intervention mot cancerkachexi:
- Upptäcka eventuella relaterade psykosociala besvär och behandla dessa
Multimodala anabola interventioner är bäst vid symtomhantering. Individualiserad kost och motion optimerar läkemedelseffekterna Rådgivning inklusive beteendeförändring, antikancer- eller antineoplastisk behandling, total parenteral nutrition, prokinetika, gestagener, cannabinoider, eikosapentaensyra, cyklooxygenashämmare, kortikosteroider och motionsinterventioner är behandlingarna.
Träningsinterventioner
Mekanismer
Träning kan öka muskelmassan, muskelfunktionen, styrkan, den kardiovaskulära konditionen och minska tröttheten vilket indirekt förbättrar livskvaliteten genom att minska trötthetsnivåerna. Det finns flera föreslagna mekanismer för samma sak. De omfattar:
Träning och inflammation
Akut träning framkallar ett immunsvar som ökar cytokinnivåerna i kroppen, men dessa cytokiner ger dock inte upphov till en proinflammatorisk effekt. IL-6 är den typiska cytokin som frigörs och förväntas i förhöjda nivåer, tillsammans med IL-10 och IL-1ra, Detta utlöser ett antiinflammatoriskt svar som spekuleras minska den systemiska inflammationen på grund av cancer, vilket dämpar kachexiprocessen. Från koncentriska övningar med måttlig intensitet till excentriska övningar med kraftig intensitet, dessa åtgärder ökar transkriptionen och uttrycker IL-6-proteinet, som är nödvändigt för att musklerna ska kunna kontrahera.
Inflammation och träning i fettvävnaden
Utomhusträning blockerar effekten av TNF-α, en inflammatorisk cytokin som stimulerar lipolys och stöder den inflammatoriska kaskaden.
Träning och oxidativ stress
Träning ökar de antioxidativa enzymerna såsom superoxiddismutas, glutationperoxidas i skelettmuskulaturen och mitokondriellt superoxiddismutas och katalas finns i lungor och diafragma. Även de icke-enzymatiska antioxidantnivåerna ökar i kroppen, vilket skyddar vävnaderna från skador.
Träning och insulinkänslighet
Det har spekulerats i att insulinresistens uppstår som svar på tumörtillväxt och som det normala inflammatoriska svaret. Motion minskar TNF-α-faktorn och förbättrar därmed kroppens känslighet för insulin. Även glukostransportproteiner som glukathion-4 ökar i skelettmuskulaturen vilket ökar glukostransporten till muskeln. Kreatininfosfat som förhindrar glutationens verkan minskar vid träning.
Träning
- Högintensiv intervallträning i åtta veckor har en effekt på icke-småcellig lungcancer i stadium III och IV hos patienter som får kemoterapi. Dessa patienter hade en hög risk för andningssvikt på grund av cancerkachexi och träning bidrog till att förbättra deras lungkapacitet.
- Progressiv motståndsträning (2-3 dagar i veckan i 12 veckor) förbättrade patienternas följsamhet och magra kroppsmassa med 1-2 kg. Dess effektivitet är dock ännu inte fastställd i gruppen med huvud- och halscancer som får strålbehandling.
- Aerobisk träning är fördelaktig i termer av att den ökar den mitokondriella biogenesen och minskar proteolysen genom att minska inflammationen.
- Pedometerbaserade övningar(7 veckor) bidrar till att förbättra skelettmassan, funktionsförmågan och livskvaliteten vid cancercachexi vid kemoterapi.
- Motståndsövningar hos patienter med prostatacancer som får androgen deprivationsbehandling och strålbehandling förebygger förlust av muskelmassa och styrka
- 1,0 1,1 Fearon K, Strasser F, Anker SD, Bosaeus I, Bruera E, Fainsinger RL, Jatoi A, Loprinzi C, MacDonald N, Mantovani G, Davis M. Definition och klassificering av cancerkakexi: en internationell konsensus. Lancet Oncol. 2011 May 1;12(5):489-95.
- Blum D, Omlin A, Fearon K, Baracos V, Radbruch L, Kaasa S, Strasser F, European Palliative Care Research Collaborative. Utvecklande klassificeringssystem för cancercachexia: redo för klinisk praxis? Support Care Cancer. 2010 Mar 1;18(3):273-9.
- Wallengren O, Lundholm K, Bosaeus I. Diagnostic criteria of cancer cachexia: relation to quality of life of life, exercise capacity and survival in unselected palliative care patients. Support Care Cancer. 2013 Jun 1;21(6):1569-77.
- 4.0 4.1 Blum D, Omlin A, Fearon K, Baracos V, Radbruch L, Kaasa S, Strasser F, European Palliative Care Research Collaborative. Utvecklande klassificeringssystem för cancercachexia: redo för klinisk praxis? Support Care Cancer. 2010 Mar 1;18(3):273-9.
- 5.0 5.1 Anderson LJ, Albrecht ED, Garcia JM. Uppdatering av hanteringen av cancerrelaterad cachexia. Curr Oncol Rep. 2017 Jan 1;19(1):3.
- 6,0 6,1 Gould DW, Lahart I, Carmichael AR, Koutedakis Y, Metsios GS. Förebyggande av cancercachexia via fysisk träning: molekylära mekanismer. J Cachexia Sarcopenia Muscle. 2013 Jun;4(2):111-24.
- Gandhi A, Samuel SR, Kumar KV, Saxena PU, Mithra P. Effect of a Pedometer-based Exercise Program on Cancer Related Fatigue and Quality of Life among Patients with Breast Cancer Receiving Chemotherapy. Asian Pac J Cancer Prev. 2020 Jun 1;21(6):1813-8.
Leave a Reply