Sintesi di Gabriel
Meccanismo
Partiamo con la ftalimmide, la trattiamo con una base come KOH o NaOH, aggiungiamo un alogenuro alchilico, e poi liberiamo l’ammina risultante. Analizziamo ogni passo del meccanismo:
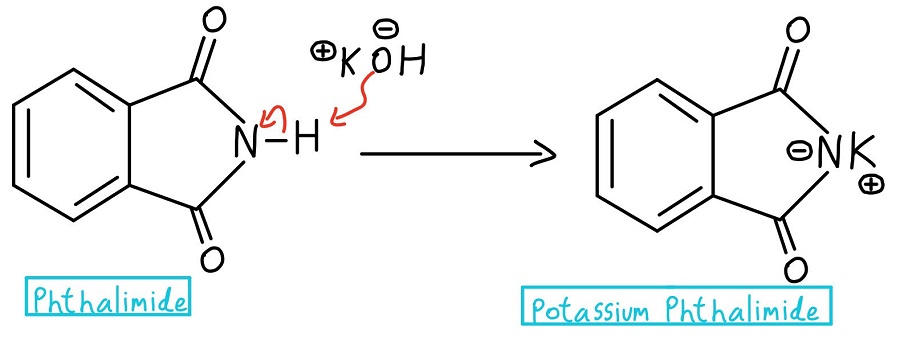
Deprotonazione dell’azoto
Nel primissimo passo, l’azoto della ftalimmide viene deprotonato per creare ftalimmide di potassio. Attenzione: alcuni professori potrebbero iniziare con la ftalimmide di potassio e saltare completamente il passo della deprotonazione.
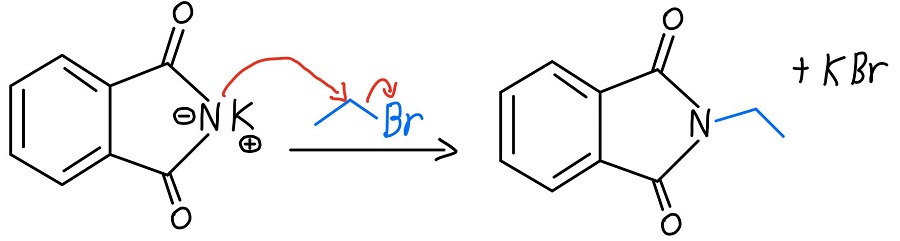
Alchilazione dell’azoto
Ora che l’azoto ha una carica negativa, può agire come nucleofilo ed eseguire una reazione SN2 su un alogenuro alchilico. Una volta che questo accade, abbiamo un’ammina primaria che aspetta solo di essere liberata.
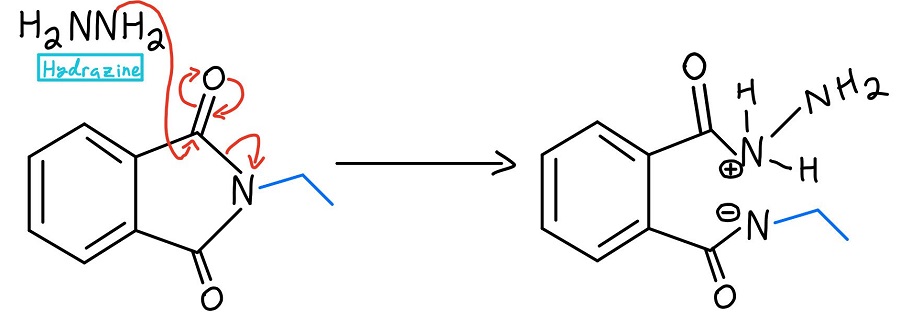
Sostituzione acilica nucleofila con idrazina
A questo punto, ci sono un paio di varianti. Di solito si usa l’idrazina (NH2NH2), ma a volte si usa l’idrolisi acida o l’idrolisi basica. Daremo un’occhiata a questi meccanismi più tardi. In ogni caso, il nucleofilo spinge via l’azoto attraverso un meccanismo di sostituzione acilica nucleofila.
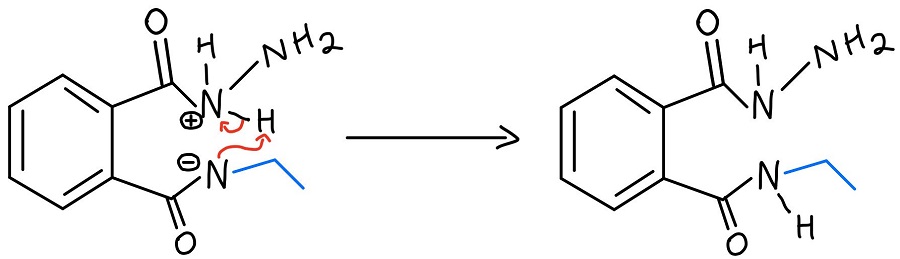
Trasferimento intramolecolare di protoni N-N
L’idrazina protonata è poi deprotonata dall’azoto che è stato appena spinto via da un carbonile. Abbiamo ancora bisogno di togliere l’ammina dal secondo carbonile, e l’NH2 dell’idrazina ripete il processo per toglierla.
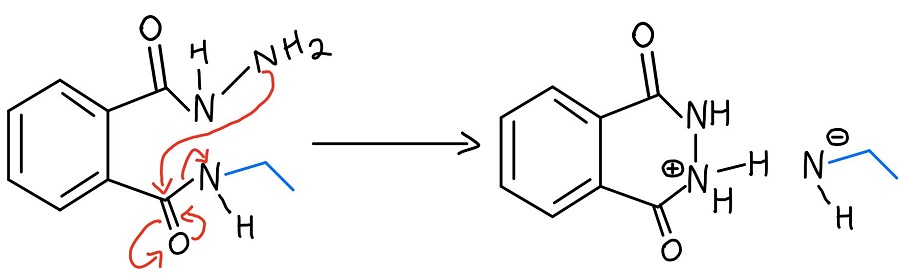
Secondo NAS
L’NH2 non reagito dell’idrazina attacca poi l’altro carbonile attraverso un altro meccanismo NAS per far uscire finalmente l’ammina. Ora c’è una carica negativa e una carica positiva, e bisogna occuparsene.
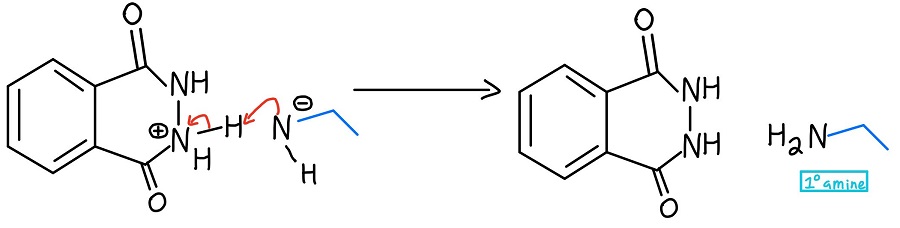
Formazione dell’ammina primaria
L’azoto negativo deprotonare l’azoto positivo, e rullo di tamburi per favore… abbiamo la nostra ammina primaria (così come il prodotto ciclico ftalidrazide)! Nel caso tu voglia vedere tutto il meccanismo in una volta, eccolo qui:
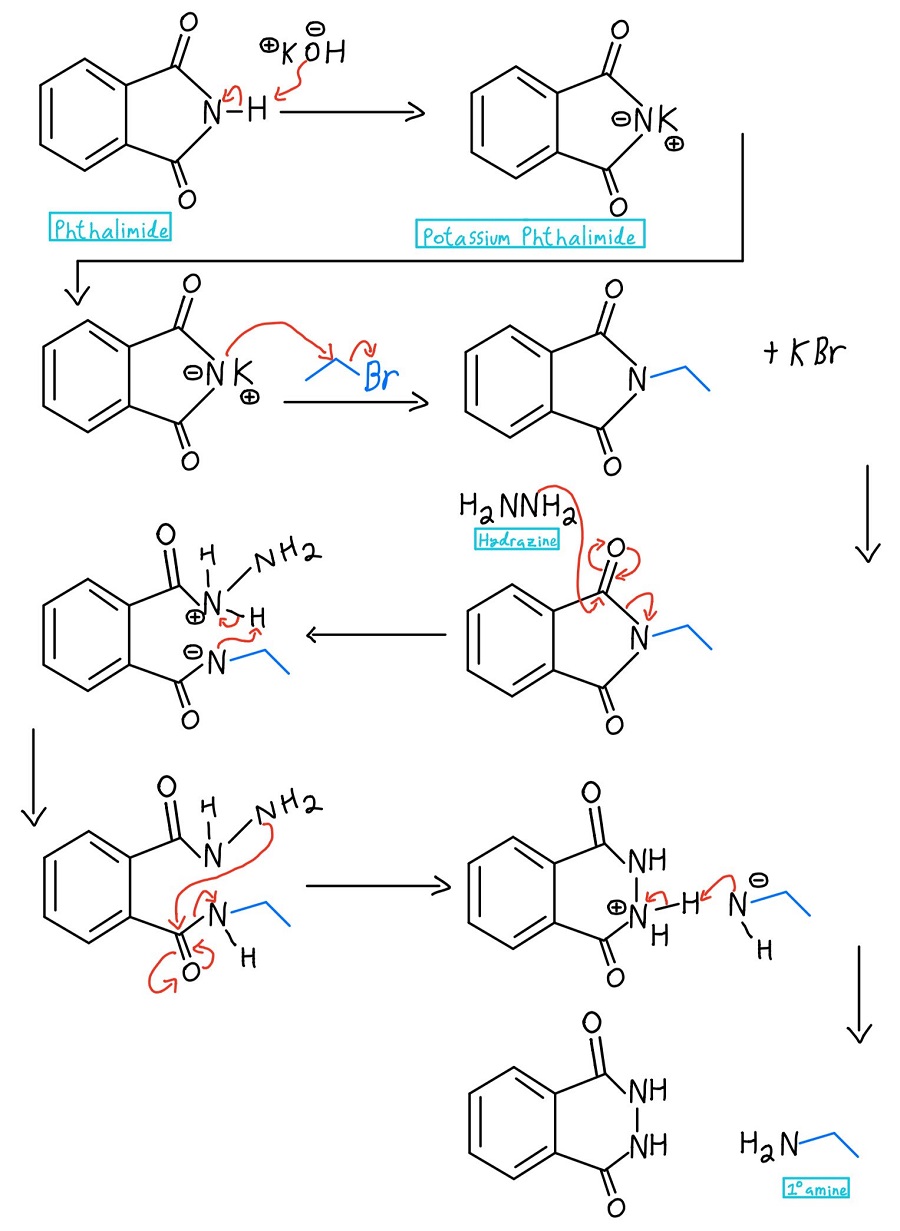
Meccanismo completo dell’idrazina
Leave a Reply