Gabrielin synteesi
Mekanismi
Aloitamme ftalimidillä, käsittelemme sitä emäksellä, kuten KOH:lla tai NaOH:lla, lisäämme alkyylihalogenidin ja vapautamme tuloksena olevan amiinin. Puretaanpa mekanismin jokainen vaihe:
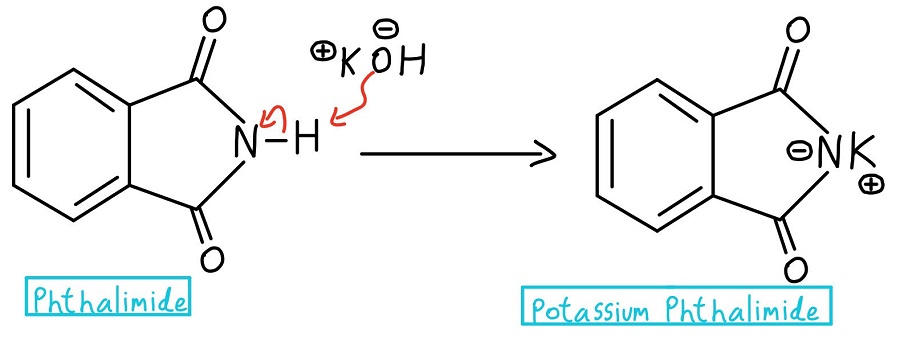
Typen deprotonointi
Heti ensimmäisessä vaiheessa ftalimidin typpi deprotonoidaan, jolloin syntyy kaliumftalimidi. Heads up: jotkut professorit saattavat aloittaa vain kaliumftalimidilla ja jättää deprotonointivaiheen kokonaan väliin.
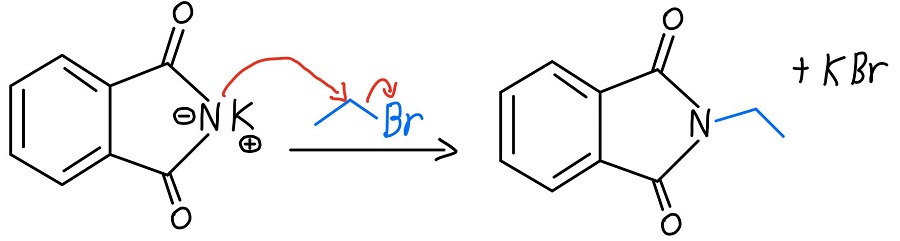
Typen alkylointi
Kun typellä on negatiivinen varaus, se voi toimia nukleofiilinä ja suorittaa SN2-reaktion alkyylihalogenidille. Kun tämä tapahtuu, meillä on primaarinen amiini vain odottamassa vapautumista.
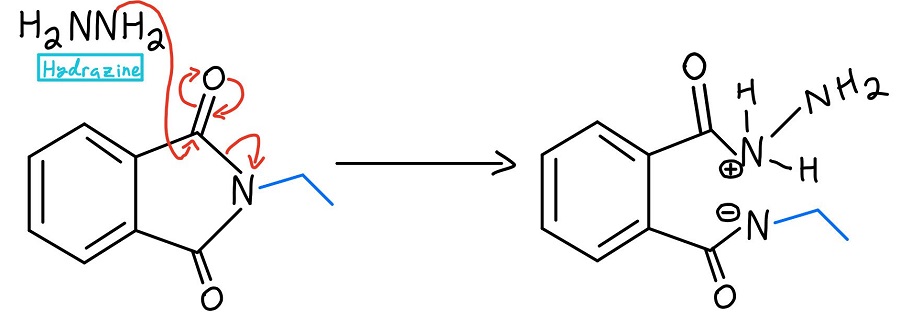
Hydratsiinin nukleofiilinen asyylisubstituutio
Tässä vaiheessa on pari variaatiota. Yleensä käytetään hydratsiinia (NH2NH2), mutta joskus käytetään hapanta tai emäksistä hydrolyysiä. Tarkastelemme näitä mekanismeja myöhemmin. Joka tapauksessa nukleofiili potkaisee typen irti nukleofiilisen asyylisubstituutiomekanismin kautta.
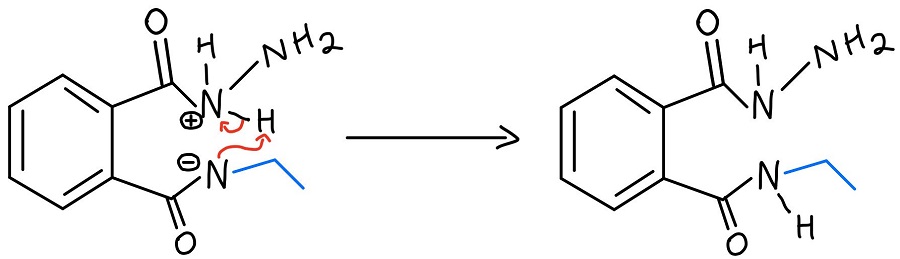
Intramolekulaarinen N-N-protoninsiirto
Protonoitunut hydratsiini deprotonoituu sitten typestä, joka juuri potkaistiin irti yhdestä karbonyylistä. Meidän on vielä saatava amiini irti toisesta karbonyylistä, ja hydratsiinin NH2 toistaa prosessin potkaistakseen sen irti.
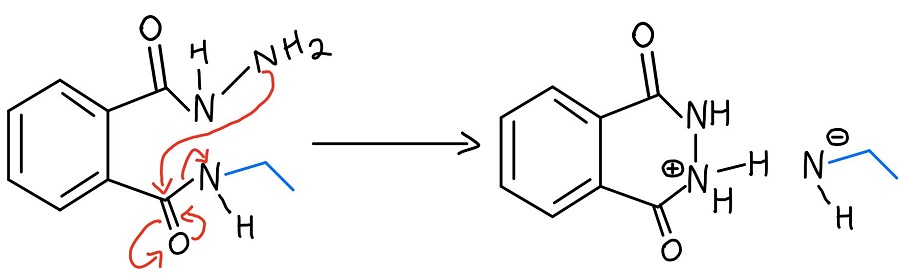
Toinen NAS
Hydratsiinin reagoimaton NH2 hyökkää sitten toisen NAS-mekanismin kautta toisen karbonyylin kimppuun potkaistakseen lopulta amiinin pois. Nyt on olemassa negatiivinen ja positiivinen varaus, ja niistä on huolehdittava.
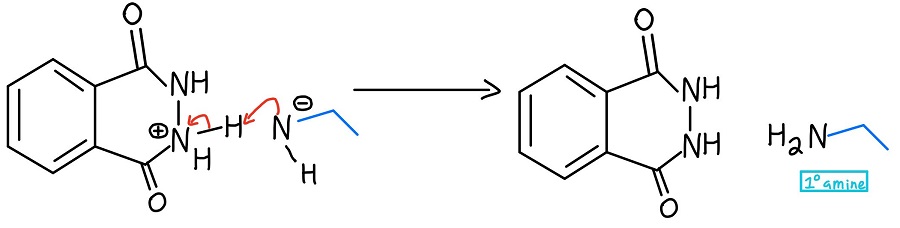
Primäärisen amiinin muodostuminen
Negatiivinen typpi deprotonoi positiivisen typen, ja rummunpyöritys… saamme primäärisen amiinin (sekä syklisen tuotteen ftalihydratsidin)! Jos haluatte nähdä koko mekanismin kerralla, tässä se on:
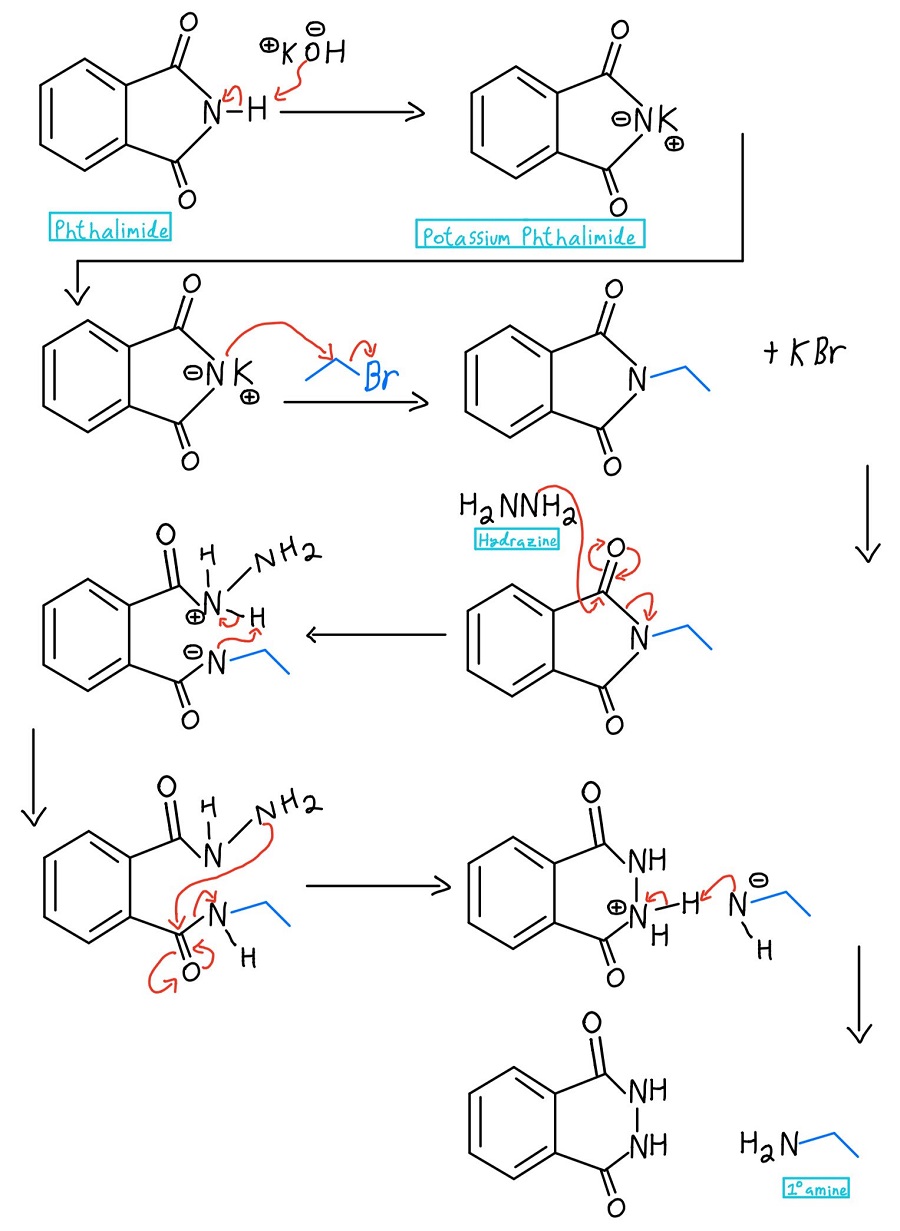
Hydratsiinin koko mekanismi
Leave a Reply