Farmakologi för ofraktionerat heparin
Detta läkemedel är en viktig del av antikoagulationen på intensivvårdsavdelningen och man gör klokt i att bli väl förtrogen med dess egenskaper.
Kemiska egenskaper och molekylstruktur
Heparin är en heterogen blandning av mukopolysackarider, så kallade glykosaminoglykaner.
Det är i huvudsak en polymeriserad disackarid, en stärkelse.
Varje upprepad disackarid är varierande sulfaterad. Här är en bild som jag slet av från Wikipedia:
Eftersom disackaridpolymererna är olika långa har heparin en genomsnittlig molekylvikt på 3 till 30 kDa. Såvida det inte fraktioneras, i vilket fall man kan kontrollera att man bara har den lågmolekylära versionen.
Dess polymerlängd är egentligen mycket mycket slumpmässig, främst på grund av att heparinet på ditt sjukhus härstammar från lungor från nötkreatur eller tarmar från svin, och dessa djur är i stort sett ointresserade av kvalitetskontrollen av industriell kemi. Det första heparinet framställdes faktiskt från leverceller från hundar 1916, av en läkarstudent på andra året.
Vad i helvete är en ”enhet” heparin?
En enhet heparin är den mängd som krävs för att hålla 1 ml kattblod flytande i 24 timmar vid 0 grader Celsius. Denna ovanligt djurfientliga definition kommer från en viss WH Howell, som lämnade lite kattblod över natten i kylskåpet. Det koagulerade inte – det koagulerade halvt – men förblev ändå flytande. Numera använder den internationella heparinstandarden fårplasma, förmodligen för att får är lättare att fånga och avbloda.
Kemiska släktingar
Jag antar att det skulle vara de fraktionerade heparinerna (t.ex. Enoxaparin).
Funktionella släktingar är alla andra indirekta trombinhämmare bland vilka finns Fondaparinux
Administrering och absorption
Den ges vanligen intravenöst, eller subkutant (varifrån den gradvis dissocieras).
-
- Den subkutana administreringsvägen tar 1-2 timmar för att nå maximal effekt.
Därefter är dess distributionsvolym 40-70 ml/kg, i huvudsak begränsad till den intravaskulära volymen.
Det tränger inte igenom placenta, vilket gör det särskilt användbart under graviditet.
Hur blir det om jag dricker det?
Oralt heparin har mycket dålig biotillgänglighet. Det är en för stor molekyl och dess laddning är för negativ för att absorberas lätt. Av denna anledning distribueras det nästan uteslutande i den cirkulerande volymen. Modiga män har försökt laga mat med heparin för att göra det mer oralt biotillgängligt. Dessutom har 45 modiga personer druckit 20 000 enheter heparin och sedan låtit testa sin APTT – det visade sig att den ökar med 2,3 sekunder i genomsnitt, vilket inte är mycket, men som visar att det finns en viss absorption. Studien är inte tillgänglig för mig, men jag skulle gärna höra från en frivillig om hur heparinet smakade.
Metabolism och clearance
Det finns 2 mekanismer: snabb mättbar clearance och långsam clearance av första ordningen.
Halveringstiden beror på dosen.
Halveringstid för 25 enheter per Kg = 30 minuter
Halveringstid för 100 enheter per Kg = 60 minuter
Halveringstid för 400 enheter per Kg = 150 minuter
Vid lägre doser, är halveringstiden mycket kort (eftersom det mesta av det heparin som ges som infusion binds direkt till makrofager och endotelceller, där det depolymeriseras). Denna mekanism blir mättad vid högre doser och elimineringen blir långsammare, med en hastighet som är relaterad till dosen.
Rapid Saturable Zero-Order Clearance:
- På grund av bindning till heparinbindande proteiner, makrofager och endotelceller.
- Som bundet blir heparin oanvändbart och depolymeriseras så småningom.
- Detta är den linjära eliminering av nollordning som ses vid låga doser.
Långsam clearance av första ordningen:
- Renal utsöndring… kanske? Om jag ska vara ärlig är det förmodligen inte renalt. Efter stora doser utsöndras en liten mängd i urinen.
- För närvarande medger MIMS att ”heparins metaboliska öde är dåligt förstått”, men nämner att det retikuloendoteliala systemet kan spela en roll i att sekretessbelägga och förstöra heparin.
Aktionsmekanism
Heparin finns i kroppen i mastcellernas sekretoriska granula. Det finns också i många djur, inklusive olika ryggradslösa djur som inte har något som ens tillnärmelsevis liknar människans koagulationskaskad. Vilket är konstigt.
Så ingen vet egentligen exakt vad dess syfte är.
Men hos människor…
Heparin ökar aktiviteten hos antitrombin-III med en faktor 1000.
Det gör det genom att det binder sig till antitrombin-III och får den aktiva platsen att genomgå en konformationell förändring.
I mitt barnsliga diagram representerar bortflippandet av antitrombin-III:s molekylära svans den ökade tillgängligheten till den aktiva platsen.
Sådär aktiverat inaktiverar antitrombin-III flera faktorer – men framför allt Xa och IIa (trombin).
Nu kommer vi till en viktig punkt.
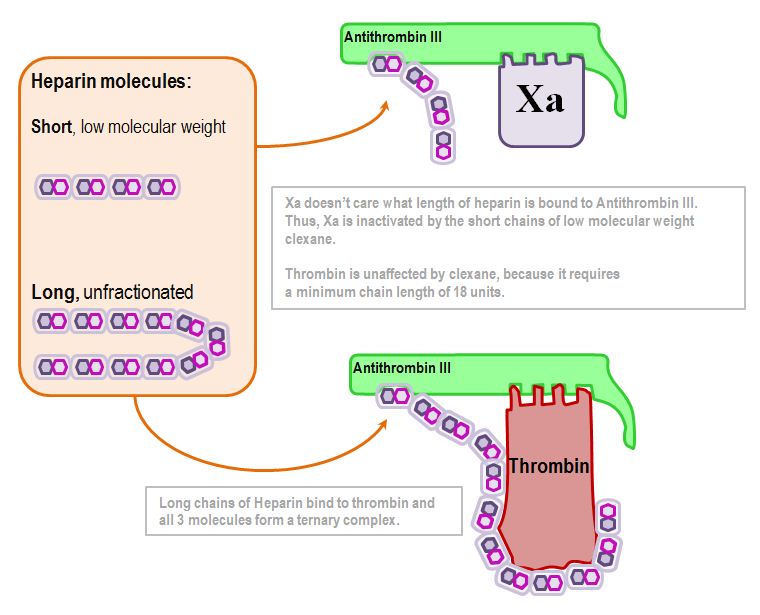
Inaktiveringen av trombin beror på heparinmolekylens längd:
18 disackaridenheter är nyckeltalet (ca 5kDa)
Inaktiveringen av Xa är oberoende av längden: så länge någon form av heparin är bundet till den kommer Antitrombin-III att inaktivera Xa.
Detta ligger till grund för skillnaden i farmakokinetik mellan heparin med låg molekylvikt och ofraktionerat heparin.
Därmed kan man sammanfattningsvis säga att ofraktionerat heparin påverkar trombin, medan lågmolekylärt heparin endast påverkar Xa.
Detta förklarar också varför mätning av APTT inte kommer att berätta om din clexandos är terapeutisk.
Det ofraktionerade heparinet påverkar också aktiviteten hos faktor 9, men inte aktiviteten hos faktor 7. Således påverkas de intrinsika och gemensamma vägarna, vilket ökar APTT. Den extrinsiska vägen är opåverkad och PT stiger inte särskilt mycket. Eftersom trombin inte påverkas av lågmolekylärt heparin förblir APTT i stort sett oförändrad.
Användningsindikationer
- Ja, dess antikoagulation, som är ett mycket större ämne. APTT-övervakning är den viktigaste frågan.
- Kort sagt, heparin används vid DVT-profylax, behandling av trombos och tromboembolism, vid akuta kranskärlssyndrom och vid upprätthållande av långsamt flödande dialyskretsar.
- Den farmakologiska hanteringen av DVT under graviditet har tidigare vilat på ofraktionerat heparin. PROTECT-studien, som jämförde ofraktionerat med LMWH, fann ingen större skillnad i DVT-frekvensen (fortfarande omkring 5,6 %), men LMWH-gruppen hade färre PE och det fanns en tendens till färre HITS.
Kontraindikationer
- Om det orsakar blödning får det en att tänka om när det gäller heparin. Detta sammanfattar i stort sett kontraindikationerna ur praktisk synvinkel. Överhängande hot om invasiva ingrepp är den viktigaste kontraindikationen.
- Den enda absoluta kontraindikationen är en tidigare historia av HIT eller HITT.
Interaktioner
Bortsett från den dumt uppenbara tendensen att öka blödningsrisken hos personer som också är antikoagulerade med någon annan typ av antikoagulerande läkemedel har heparin få verkliga farmakologiska interaktioner:
| Effekter av heparin förstärks av | Effekter av heparin motverkas av |
| Hydroxycholoroquine | Antihistaminer |
| Probenecid | Digoxin |
| Natriumvalproat | Tetracykliner |
| Vitamin C | |
| Nikotin |
Kroniska komplikationer
Heparin-Induced Thrombocytopenia Syndrome (HITS) plus Heparin-Induced Thrombocytopenia and Thrombosis Syndrome (HITTS)
-
- Immunmedierad trombocytopeni som diskuterades väl av Franchini 2005
-
-
-
- Frekventare förknippat med ofraktionerat heparin
- Högre frekvens hos äldre; Ovanligt hos barn
- Hjärtkirurgiska och ortopediska patienter löper större risk
- Typiskt inträffar 5-10 dagar efter start av heparin
-
-
-
- Immunmedierad trombocytopeni som diskuterades väl av Franchini 2005
-
- Finns i två smaker: Typ 1 och typ 2.
HITTER typ 1:
- Mild övergående trombocytopeni, Trombocytantal över 100
- Totalt reverserat av heparinstopp
- Förekommer hos upp till 10 % av patenterna
- Inte förknippat med ökad risk för trombos
- Förmodligen är det inte ens immunt ursprung
HITS Typ 2: HITS typ 2:
- Svårt allvarlig trombocytopeni, trombocytantalet kan sjunka till noll
- Förekommer i ungefär 1 % av patenten
- Associerat med trombos i 30 % av fallen
- Skyller på bildandet av antikroppar mot komplexet som består av trombocytfaktor 4 (PF4) och heparin; detta komplex bildas på trombocyternas yta.
- När HIT-antikroppen binder till detta komplex orsakar den trombocytaktivering och aggregering, och därför finns det en tendens till koagulering (eftersom alla trombocyter aktiveras) samt en samtidig tendens till blödning (eftersom det sker en förstörelse av antikroppsbelagda trombocyter i det retikuloendoteliala systemet)
När patienten har HIT bör han eller hon fortfarande vara antikoagulerad.
Direkta trombinhämmare är den bästa behandlingen.
Andra effekter av kronisk heparinanvändning
- Osteopeni
- Heparin aktiverar av någon anledning osteoklaster och benresorptionen ökar.
- Mineralokortikoidbrist
- Heparin tycks motverka effekterna av ACTH
- Konstiga biverkningar
- Alopeci- vem vet hur.
- Höjning av AST och ALT – vem vet varför.
Akut toxicitet och överdosering
- Den viktigaste akuta biverkningen är blödning. Mycket få personer är genuint allergiska mot heparin.
- Hudnekros kan uppstå vid de subkutana injektionsställena på grund av trombos i små kärl.
Hantering av akut toxicitet
Om man har överdoserat hepariniseringen kommer th APTT att stiga dramatiskt, och man mya få någon form av blödningskomplikationer. Man kan komma att tänka: ”Jag önskar att jag kunde sätta ihop koagulationskaskaden igen”. Detta kan åstadkommas med protamin.
RÖVERGÅNG AV HEPARINISERING med protaminsulfat
- 1 mg reverserar 100 enheter
- Inte mer än 50 mg vid ett och samma tillfälle
- Det ges LÅGT som intravenös infusion
Faranterna med protaminsulfat
Protaminsulfat är långt ifrån godartat. Det är en främmande, ovanlig substans – en starkt alkalisk polypeptid som binder irreversibelt till starkt surt heparin och därigenom minskar dess antikoagulerande effekt på antitrombin-3. I löjliga doser fungerar dock protamin i sig självt som antikoagulant.
Av dess många negativa effekter kan nämnas följande:
- Katastrofal hypotension på grund av vasodilatationen, som tack och lov är kortvarig (endast ca 3-4 min) – detta verkar vara resultatet av en systemisk histaminfrisättning, som utlöses på något slags direktkompletterande sätt av de cirkulerande heparin-protamin-komplexen
- Lunghypertension på grund av den lokaliserade vasokonstriktoriska aktiviteten hos tromboxan, aktiveras av en anafylaktoid reaktion på protamin
- Anafylaxi (det är trots allt en fiskprodukt)
Resistens mot heparinbehandling
Det finns situationer där stora mängder intravenöst heparin inte lyckas öka APTT trots alla ansträngningar. Man kan kalla detta för ”heparinresistens” eller ”heparininkänslighet”.
Det finns flera anledningar till att man kan vara resistent mot heparin:
- Ökade heparinbindande proteinnivåer (alla är akutfasreaktanter)
- Låga halter av antitrombin-III (i.Dvs. inget för heparin att binda)
- Ökat heparinclearance (t.ex. vid leversjukdom)
- Höga faktor VIII-nivåer
UpToDate erbjuder en bra artikel om Antitrombin III-brist. Antingen är man ärftligt misslyckad med att syntetisera tillräckligt mycket av det, eller så är levern så skadad att den inte kan producera tillräckligt mycket. Eller så har det förbrukats på något sätt, t.ex. i samband med DIC, MAHA eller i en bypass-krets. Slutligen är det möjligt att du förlorar det tillsammans med andra proteiner via dina läckande nefrotiska njurar.
Hanteringen av AT-III-brist är, vilket är förutsägbart, tillskott av AT-III.
Om den dyra renade faktorn inte finns tillgänglig räcker det med FFP.
Effektiv koagulation av den heparinresistenta patienten
Det finns flera strategier som man kan använda. Det specifika valet beror på exakt vad som orsakar heparinresistensen.
Det finns några bra artiklar om detta. De flesta av dem berör inte den rutinmässiga antikoagulationen av någon slumpmässig patient som råkar få eskalerande doser av heparin; jag antar att man i allmänhet utgår från att man kommer att fortsätta att trappa upp dosen tills de terapeutiska målen är uppnådda. Det finns dock situationer där antikoagulation är av avgörande betydelse, och ett sådant scenario är den kardiopulmonella bypass-kretsen.
– Byt till lågmolekylärt heparin i stället för ofraktionerat heparin
– Ge kryoprecipitat och/eller färsk fryst plasma (om det finns bekräftad ATIII-brist )
– Ge antitrombin III-koncentrat
Och man kan överväga att använda något annat, t.ex. en direkt trombinhämmare (hirudin eller argobatran)
.




Leave a Reply