Enolază
este o enzimă care catalizează o reacție de glicoliză. Glicoliza transformă glucoza în două molecule cu 3 atomi de carbon numite piruvat. Energia eliberată în timpul glicolizei este utilizată pentru a produce ATP. Enolază este utilizată pentru a transforma 2-fosfogliceratul (2PG) în fosfoenolpiruvat (PEP) în cea de-a 9-a reacție a glicolizei: este o reacție reversibilă de deshidratare… Enolază este exprimată abundent în majoritatea celulelor și s-a dovedit a fi utilă ca model pentru a studia mecanismele de acțiune enzimatică și analiza structurală . Ca și în cazul reacției de mai jos, Enolază trebuie să aibă un cation metalic divalent prezent pentru a activa sau dezactiva enzima. Cel mai bun cofactor ar fi Mg2+, dar pot fi utilizați mulți, inclusiv Zn2+, Mn2+ și Co2+. Ionul metalic acționează prin legarea la enzima din situsul activ și producerea unei modificări de conformație. Acest lucru face posibil ca substratul (2-PGA) să se lege la situsul activ al enolazei. Odată ce acest lucru se întâmplă, un al doilea ion metalic intervine și se leagă de enzimă pentru a activa capacitatea catalitică a enolazei. A se vedea Enzimele glicolizei. Pentru alinierea secvențelor, a se vedea Alinierea secvențelor multiple pentru Enolază.
Contenit
- 1 Structură
- 2 Mecanism
- 3 Cinetică
- 4 Reglementare
- 5 Altele informații interesante
- 6 Structuri 3D ale enolazei
Structura
Structura enolazei conține atât elice alfa cât și foițe beta. Foițele beta sunt în principal paralele. După cum se arată în figură, enolaza are aproximativ 36 de elice alfa și 22 de foițe beta (18 elice alfa și 11 foițe beta pe domeniu). Enolază este formată din două domenii.
Clasificarea structurală a proteinelor (SCOP)
Enolază face parte din clasa proteinelor alfa și beta și are un pliu de tip TIM beta/alfa-baril. Ea provine din Superfamilia pe Enolase C-terminal domain-like și face parte din familia enolazei.
Mecanism
Mecanismul enolazei, așa cum este prezentat, implică Lys 345, Lys 396, Glu 168, Glu 211 și His 159. Enolază formează un complex cu două la nivelul situsului său activ. Substratul, 2PG, se leagă de cele două . Mg 2+ formează apoi o legătură la acidul carboxilic deprotonat de pe 1’C pentru a-l lega de enolază. De asemenea, se leagă de Glu 211 și Lys 345. Glu 211 realizează o legătură de hidrogen cu grupul alcoolic de pe 3’C. Lys 345 deprotonează 2’C și apoi 2’C formează o alchenă cu 1’C care apoi mută electronii care formează cetona pe oxigen, ceea ce face ca acesta să aibă o sarcină negativă. Celălalt oxigen, care are deja o sarcină negativă, își mută apoi electronul pentru a forma o cetonă cu 1’C. Electronii care au format alchenul dintre 1’C și 2’C se deplasează apoi pentru a forma un alchen între 2’C și 3’C. Acest lucru rupe legătura cu alcoolul de pe 3’C care deprotonează Glu 211 de pe enolază pentru a forma H2O. Apoi, noua moleculă este eliberată din enolază sub formă de PEP. PEP trece apoi printr-o altă etapă a glicolizei pentru a crea piruvat.
Ionii de fluorură inhibă glicoliza prin formarea unei legături cu Mg 2+ și astfel blochează legarea substratului (2PG) la situsul activ al enolazei.
Cinetică

Din moment ce Mg2+ este esențial pentru legarea substratului, 2-PG, acesta este, de asemenea, necesar la o anumită calitate pentru a avea o rată, sau viteză bună. Graficul prezintă V vs. , în care PGA este 2-PG, cu două concentrații diferite de Mg2+. Curba superioară, care are, de asemenea, un Vmax mai mare, are o concentrație de Mg2+ de 10^-3 M, în timp ce curba inferioară, care are un Vmax mai mic, are o concentrație de Mg2+ de 10^-2 M. Km este, de asemenea, mai mare în cazul curbei superioare, ceea ce face ca cea mai mare să fie mai de dorit.
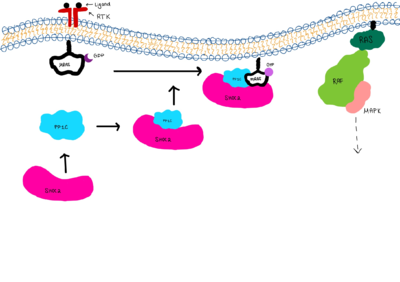
Reglementare
Enolază se găsește pe suprafața unei varietăți de celule eucariote ca un receptor puternic de legare a plamingoenului și pe suprafața celulelor hematopietice, cum ar fi monocitele, celulele T și celulele B, celulele neuronale și celulele endoteliale. Enoliza din mușchi poate lega cu mare afinitate alte enzime glicolitice, cum ar fi fosfoglicerat-mutaza, creatin-kinaza musculară, piruvat-kinaza și troponina musculară. Acest lucru sugerează că ele formează un segment glicolitic funcțional în mușchi, unde producția de ATP este necesară pentru ca mușchiul să se contracte. Proteina de legare a Myc (MBP-1) este similară cu structura a-enolazei și se găsește în nucleu ca proteină de legare a ADN. enolază este reglată de concentrația de Mg2+ și de etapele anterioare ale glicolizei.
Alte informații interesante
Enolază este prezentă în toate țesuturile și organismele cu capacitatea de a face glicoliză sau fermentare. Studii recente au probe de concentrație a Enolazei pentru a determina anumite condiții și gravitatea lor. De exemplu, concentrațiile ridicate de Enolază în lichidul cefalorahidian (LCR) sunt mai puternic asociate cu astrocitomul decât alte enzime, cum ar fi aldolază, piruvat kinaza și creatin-kinaza. Concentrațiile ridicate de Enolază în LCR sunt, de asemenea, legate de cea mai rapidă rată de creștere a tumorii și de creșterea șanselor de atac de cord sau de accident vascular cerebral.Enolază poate fi inhibată în mod competitiv de fluorură pentru substratul 2-PGA. În apa potabilă cu adaos de fluor, activitatea Enolazei bacteriilor orale este inhibată fără ca oamenii să fie afectați. Acest lucru funcționează pentru a preveni cariile.
Structuri 3D ale enolazei
Structuri 3D ale enolazei
.
Leave a Reply