Calor
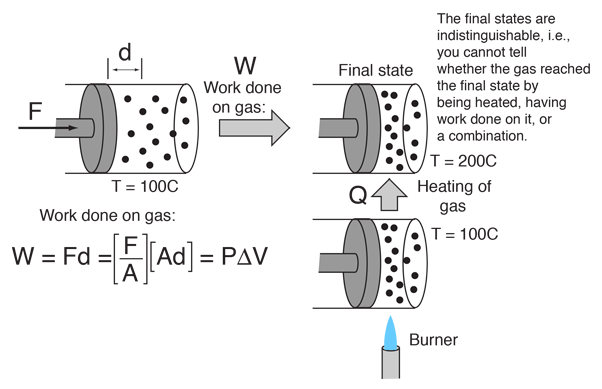
Este exemplo da intercambialidade de calor e do trabalho como agentes de adição de energia a um sistema pode ajudar a dissipar alguns equívocos sobre o calor. Encontrei a ideia num pequeno artigo de Mark Zemansky intitulado “The Use and Misuseuse of the Word ‘Heat’ in Physics Teaching” (O Uso e Mau Uso da Palavra ‘Calor’ no Ensino da Física). Uma idéia chave deste exemplo é que se você é apresentado com um gás de alta temperatura, você não pode dizer se ele atingiu essa alta temperatura por ser aquecido, ou por ter trabalhado nele, ou por uma combinação dos dois.
Para descrever a energia que um objeto de alta temperatura tem, não é um uso correto da palavra calor dizer que o objeto “possui calor” – é melhor dizer que ele possui energia interna como resultado de seu movimento molecular. A palavra calor é melhor reservada para descrever o processo de transferência de energia de um objeto de alta temperatura para um de temperatura mais baixa. Com certeza você pode pegar um objeto com baixa energia interna e elevá-lo a uma energia interna mais alta aquecendo-o. Mas você também pode aumentar sua energia interna fazendo trabalho nele, e como a energia interna de um objeto de alta temperatura reside no movimento aleatório das moléculas, você não pode dizer qual mecanismo foi usado para lhe dar essa energia.
No aviso tanto aos professores como aos alunos sobre as armadilhas do mau uso da palavra “calor”, Mark Zemansky aconselha a reflectir sobre o jingle:
“Ensinar física térmica |
Não se refira ao “calor num corpo”, ou diga “este objecto tem o dobro do calor daquele corpo”. Ele também se opõe ao uso do termo vago “energia térmica” e ao uso da palavra “calor” como verbo, pois eles alimentam os conceitos errados, mas é difícil evitar esses termos. Ele aconselharia a introdução e uso do conceito de energia interna o mais rápido possível. |
Zemansky aponta a Primeira Lei da Termodinâmica como uma relação esclarecedora. A Primeira Lei identifica tanto o calor como o trabalho como métodos de transferência de energia que podem trazer uma mudança na energia interna de um sistema. Depois disso, nem as palavras trabalho ou calor têm qualquer utilidade na descrição do estado final do sistema – podemos falar apenas da energia interna do sistema.
| Equivalente mecânico do calor | Primeira Lei da Termodinâmica | Cálculo |
Leave a Reply