Acetato de eslicarbazepina para dor neuropática, dor de cabeça e neuralgia craniana: evidências e experiência | Neurología (Portuguese Edition)
Introduction
Acetato de eslicarbazepina (ESL) é um medicamento antiepiléptico de terceira geração aprovado em 2009 pela Agência Europeia de Medicamentos e em 2013 pela US Food and Drug Administration. Está disponível no mercado espanhol desde Fevereiro de 2011. O medicamento está atualmente indicado como terapia adjuvante para pacientes adultos com convulsões parciais com ou sem generalização secundária. A dose inicial recomendada é de 400mg uma vez por dia, aumentando para 800mg uma vez por dia após 1 a 2 semanas. A dose pode ser aumentada para 1200mg, dependendo da resposta do paciente.1
ESL pertence à família das dibenzazepinas, assim como a carbamazepina (CBZ) e a oxcarbazepina (OXC). Estes medicamentos são estruturalmente diferentes um do outro na posição 10,11. Eles também diferem em termos de metabolismo: A CBZ é metabolizada em CBZ-10,11-epóxido, ao contrário da OXC, que é metabolizada no metabolito ativo S-licarbazepina (78,1%), e ESL, que é metabolizada no mesmo metabolito, mas em uma proporção maior (93,9%) (Fig. 1).2,3 O número de doses diárias também é diferente: doses únicas no caso de ESL e OXC de liberação prolongada (não disponível na Espanha), 2 doses de OXC de liberação imediata e CBZ de liberação prolongada (não disponível na Espanha), e 2 a 3 doses de CBZ de liberação imediata. De acordo com um estudo recente de Soares-da-Silva et al.,4 o mecanismo de ação da ESL tem algumas características distintivas em relação a outros medicamentos da mesma família: 1) a seletividade da interação com o estado inativo do canal de sódio em tensão (VGSC), 2) redução da disponibilidade da VGSC através do aumento da inativação lenta, ao invés da alteração da inativação rápida da VGSC, e 3) inibição do hCaV3 de alta e baixa afinidade.2 correntes internas com maior afinidade que CBZ.
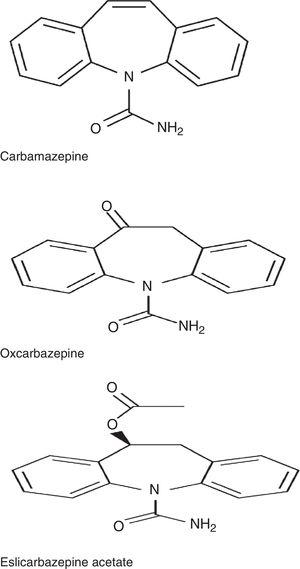
Estrutura química da carbamazepina, oxcarbazepina e acetato de eslicarbazepina.
>
Semelhantemente ao OXC, a ESL é moderadamente tóxica, com os efeitos adversos mais comuns sendo tonturas, náuseas, vómitos, sonolência e diplopia. Tem uma meia-vida de eliminação de 13-24 horas, e pode portanto ser administrada como uma dose única diária. A ESL é um leve indutor da UDP-glucuronosiltransferase (UGT1A1) e da isoforma CYP3A4 do citocromo P450. Esta atividade pode causar algumas interações clinicamente relevantes com fenitoína, warfarina e contraceptivos contendo estrogênio.1
CBZ está indicado não apenas para epilepsia, mas também para episódios maníacos e para profilaxia de distúrbio afetivo bipolar, neuralgia essencial do trigêmeo, neuralgia glosofaríngea essencial e síndrome de abstinência de álcool,5 enquanto a OXC está indicada para o tratamento de convulsões parciais com ou sem generalização secundária com convulsões tônico-clônicas.6
As últimas diretrizes clínicas concordam que os antidepressivos tricíclicos e de dupla ação (venlafaxina, duloxetina) e os antiepilépticos gabapentina e pregabalina constituem o tratamento de escolha para a dor neuropática. Tramadol, lidocaína 5% e capsaicina 8% são tratamentos de segunda linha, enquanto os opióides fortes constituem a terceira linha de tratamento.7
Não são indicados nem ESL nem OXC para dor neuropática, dor de cabeça ou neuralgias cranianas. Entretanto, outros medicamentos antiepilépticos não indicados para esses cenários clínicos, como lamotrigina e lacosamida, são freqüentemente utilizados fora do rótulo na prática clínica.8-Neste estudo, revisamos as evidências disponíveis sobre o uso de ESL para dor neuropática, dor de cabeça e neuralgias cranianas, para determinar se a droga pode ser uma opção válida em pacientes com má resposta ou intolerância aos tratamentos tradicionais.
Desenvolvimento
Realizamos uma pesquisa bibliográfica no PubMed e no Google Scholar usando a seguinte estratégia de pesquisa: “acetate eslicarbazepine AND neuropathic pain” e “acetate eslicarbazepine AND headaches”. Consideramos apenas artigos de revistas científicas indexadas e artigos originais selecionados e relatos de casos publicados em inglês ou em espanhol. Como esta estratégia não produziu praticamente nenhum resultado, decidimos ampliar nossa pesquisa incluindo cartazes e comunicações orais sobre o mesmo tema (“eslicarbazepina de acetato e dor neuropática” e “eslicarbazepina de acetato e dores de cabeça”) apresentados nas Reuniões Anuais da Sociedade Espanhola de Neurologia (SEN) entre 2011 e 2015 e em outros congressos internacionais. Para maior clareza, estruturamos o artigo com várias seções diferentes.
Estudos experimentais de acetato de eslicarbazepina para dor neuropática
Em estudos experimentais com ratos, o efeito analgésico da ESL tem sido estudado extensivamente em uma ampla gama de estados de dor induzida, incluindo neuralgia do trigêmeo, neuropatia diabética e dor visceral; os resultados sugerem que a droga pode ser útil para o tratamento da dor inflamatória e neuropática.13
Acetato de esclicarbazepina para neuropatia diabética dolorosa
Encontramos um poster sobre neuropatia diabética dolorosa (PDN) apresentado no congresso EFIC 2013 da Federação Europeia da Dor. O poster apresentou os resultados de um estudo multicêntrico, randomizado, duplo-cego, controlado por placebo, em grupo paralelo, fase II de dose-finding. O estudo compreendeu um período de duas semanas de washout, durante o qual os tratamentos anteriores para dor neuropática foram interrompidos, seguido por um período de titulação de uma semana, um período de manutenção de 12 semanas e um período de seguimento de duas semanas. Um total de 557 pacientes foram designados aleatoriamente para receber placebo, 400mg ESL duas vezes por dia (BID), 800mg ESL uma vez por dia (QD), 600mg ESL BID, 1200mg ESL QD, ou 800mg ESL BID. Após 12 semanas de tratamento, não foram observadas diferenças estatisticamente significativas entre os indivíduos que receberam placebo e aqueles que receberam ESL para o controle da dor (análise de eficácia primária) de acordo com a Escala Numérica de Classificação da Dor (NPRS). Entretanto, a porcentagem de indivíduos que experimentaram uma diminuição de 30% na intensidade da dor em ≥ foi maior no grupo que recebeu 400mg de ESL BID do que no grupo placebo (62,5% vs 44,8%; P=.0230). A incidência de reações adversas foi de 38,0% no grupo placebo e 51,8% no grupo tratado com 1200mg de ESL QD. As reacções adversas mais frequentes foram vómitos, tonturas e náuseas.14
A nossa pesquisa bibliográfica também encontrou um estudo multicêntrico, aleatório, duplo-cego, controlado por placebo, fase III do grupo paralelo da PDN; o estudo durou 15 semanas (3 semanas de ajuste da dose+12 semanas de seguimento). A variável de eficácia primária foi a mudança na intensidade da dor desde o início (linha de base) até a conclusão do estudo (15 semanas), e foi medida usando o NPRS. Um total de 332 pacientes com PDN foram designados aleatoriamente para receber placebo, 1600mg ESL QD, 1200mg ESL QD, ou 800mg ESL QD. Após 15 semanas de tratamento, não foram observadas diferenças estatisticamente significativas no tratamento da dor entre os participantes que receberam placebo e os que receberam ESL. A incidência de reações adversas variou de 12,20% no grupo placebo a 63,10% no grupo que recebeu 1600mg de ESL QD. As reações adversas mais frequentes foram vertigem, náusea e hiponatraemia (esta última foi dose-dependente). Os resultados deste estudo não foram publicados.15
García Escrivá et al.16 compartilharam sua experiência com ESL como tratamento de segunda linha para PDN refratário a drogas tradicionais. Durante 2013, os autores identificaram oito pacientes com PDN cujos tratamentos anteriores não haviam conseguido administrar a dor de forma satisfatória. Em uma visita inicial, eles substituíram o tratamento anterior da dor por ESL, coletaram dados demográficos e administraram os questionários a seguir: Escala DN4, Escala de Ansiedade e Depressão Hospitalar, Escala Visual Analógica (VAS) para dor, Escala de Impressão Global de Melhoria do Paciente e Escala de Impressão Clínica Global de Melhoria. Em uma consulta de acompanhamento realizada 12 semanas após o tratamento, os pacientes completaram os mesmos questionários e foram questionados sobre quaisquer reações adversas. Os dados coletados foram usados para análise estatística. Em relação ao tratamento anterior, 75% dos pacientes tinham recebido pré-gabalina, 25% amitriptilina, 12,5% clonazepam e 12,5% fentanil, tanto em monoterapia como em terapia combinada. No início do tratamento de ESL, os pacientes estavam tomando uma média de 4,6 medicamentos simultaneamente (variação, 1-11; mediana: 4,5). Não foram feitas alterações no tratamento concomitante durante o período de acompanhamento. A dor neuropática, avaliada com a escala DN4, diminuiu significativamente aos 3 meses (P=,026, teste de Wilcoxon). O estudo não encontrou alterações significativas em nenhuma das características da dor medidas pela escala. Os autores observaram uma diminuição significativa na dor neuropática medida com a EVA (P=.018, teste de Wilcoxon). Os resultados dos pacientes melhoraram tanto na escala de ansiedade (P=.102, teste de Wilcoxon) quanto na escala de depressão (P=.276, teste de Wilcoxon), embora as alterações não tenham sido estatisticamente significativas. Subjetivamente, 65,5% dos pacientes relataram sentir-se “muito melhor” ou “melhor” e 87,5% dos médicos indicaram que os pacientes estavam “melhores” ou “muito melhores”. O ESL foi retirado em um paciente devido a reações adversas (tonturas). Aos 3 meses, 7 pacientes (87,5%) continuaram a tomar ESL, 2 a 400mg/dia e 5 a 800mg/dia. Apesar do pequeno tamanho da amostra, a ESL foi encontrada como uma alternativa eficaz para o tratamento da dor neuropática em pacientes com NDP refratária ao tratamento convencional e mostrou boa tolerabilidade e aderência.16,17
Acetato de Eslicarbazepina para neuralgia pós-terpética
Nossa pesquisa na literatura encontrou um poster sobre neuralgia pós-terpética (PHN) apresentado no congresso EFIC 2013 da European Pain Federation. O poster apresentou os resultados de um estudo multicêntrico, randomizado, duplo-cego, controlado por placebo, grupo paralelo, fase II de dose-finding. O estudo compreendeu um período de duas semanas de washout, durante o qual os tratamentos anteriores para NPP foram interrompidos, seguido por um período de titulação de uma semana, um período de manutenção de oito semanas e um período de seguimento de duas semanas. Um total de 567 pacientes foram designados aleatoriamente para receber placebo, 400mg ESL BID, 800mg ESL QD, 600mg ESL BID, 1200mg ESL QD, ou 800mg ESL BID. A análise de intenção de tratamento não mostrou diferenças estatisticamente significativas entre os grupos de placebo e ESL em termos de intensidade da dor medida com a NPRS (análise de eficácia primária). De acordo com a análise por protocolo, entretanto, a intensidade da dor diminuiu significativamente mais no grupo que recebeu 800mg de ESL BID do que no grupo placebo (P=.0277). A incidência de reações adversas variou de 31,2% no grupo placebo a 54,4% no grupo que recebeu 800mg de BID de ESL. As reacções adversas mais frequentes foram tonturas, sonolência, dores de cabeça, náuseas e vertigens.18
A nossa pesquisa na literatura também encontrou um estudo multicêntrico, randomizado, duplo-cego, controlado por placebo, fase III do grupo paralelo de PHN com duração de 15 semanas. A variável de eficácia primária foi a mudança na intensidade da dor desde o início do estudo até a conclusão do estudo (15 semanas), e foi medida usando o NPRS. Um total de 240 pacientes com PHN foram designados aleatoriamente para receber placebo, 1600mg ESL QD, 1200mg ESL QD, ou 800mg ESL QD. Não foram observadas diferenças significativas na intensidade da dor entre os grupos placebo e ESL após 15 semanas de tratamento. A incidência de reações adversas variou de 10% no grupo placebo a 76,67% no grupo tratado com 1600mg de ESL QD. As reacções adversas mais frequentes foram náuseas, tonturas e dores de cabeça. Os resultados deste estudo não foram publicados.19
Eslicarbazepine acetate for cranial neuralgias
Gaber et al.20 publicaram o caso de uma mulher de 62 anos com neuralgia do trigêmeo associada a esclerose múltipla adequadamente controlada com CBZ. Entretanto, o tratamento teve que ser interrompido devido à hiponatremia sintomática recorrente. Diversas drogas, incluindo topiramato, gabapentina e amitriptilina, não conseguiram melhorar a neuralgia do trigêmeo. ESL em baixas doses (400mg diários) conseguiram excelente controle da dor sem alterar a concentração plasmática de sódio.
Cuadrado et al.21 publicaram o caso de um homem de 32 anos com epicrania fugax que era refratário a inúmeros tratamentos (bloqueio nervoso occipital com triamcinolona e bupivacaína, gabapentina, lamotrigina, pregabalina, topiramato, zonisamida, valproato de sódio, lacosamida, indometacina). A CBZ dosada a 1200mg/dia reduziu a intensidade da dor, mas teve que ser descontinuada devido a sonolência. A ESL dosada a 800mg/dia reduziu significativamente a frequência e intensidade da dor. A dose foi aumentada para 1600mg/dia; o paciente mostrou boa tolerância e permaneceu assintomático. Os sintomas reapareceram quando a dose foi reduzida.
Cação et al.22 estudaram uma coorte de 15 pacientes com dor de cabeça neuralgiforme unilateral de curta duração com injeção conjuntival e laceração (SUNCT), dos quais a maioria respondeu à lamotrigina, um respondeu ao topiramato e um à ESL.
O caso clínico apresentado por Aledo Serrano et al.23 na 66ª Reunião Anual do SEN descreveram o caso de um homem de 38 anos com diagnóstico de epicrania fugax refratária à lamotrigina, pré-gabalina, gabapentina, topiramato, zonisamida, indometacina, valproato, lacosamida, levetiracetam, bloqueio anestésico do nervo occipital maior e injeção de toxina botulínica no local da dor. O paciente reagiu parcialmente à CBZ, mas experimentou reacções adversas graves. O paciente permaneceu assintomático com ESL dosada a 1200mg diários.
Sánchez Larsen et al.24 apresentaram um estudo observacional e retrospectivo na 66ª Reunião Anual do SEN, analisando um grupo de pacientes com neuralgia do trigêmeo tratados com ESL tanto em monoterapia quanto em terapia combinada. As principais variáveis foram intensidade da dor antes e depois do tratamento (SAV), freqüência de crises de dor antes e depois do tratamento e reações adversas. O estudo incluiu 10 pacientes (4 em monoterapia); 7 eram mulheres, e a idade média foi de 67,9 anos (variação, 28-92). O tempo médio de seguimento foi de 24,7 meses, com exceção de 2 desistências devido a reações adversas leves (tonturas). Nenhum paciente apresentou reações adversas graves; um apresentou hiponatraemia. A intensidade e frequência da dor diminuiu em 9 dos 10 pacientes. Nestes pacientes, a intensidade da dor diminuiu de 8,7 pontos para 2,6 e a frequência da dor diminuiu de 12,13 para 2,28 ataques por dia (4 pacientes estavam assintomáticos, 3 tiveram 1-2 ataques por semana, 2 tiveram ligeiras melhorias, mas a frequência dos ataques ainda era elevada). Nesta série, a ESL foi considerada eficaz e segura para o tratamento da neuralgia do trigêmeo, e superior à CBZ do ponto de vista da segurança e farmacocinética, embora os autores recomendem um estreito monitoramento dos níveis de sódio.
Em um estudo apresentado na 67ª Reunião Anual do SEN (2015), Abril-Jaramillo et al.25 analisaram a resposta ao tratamento com ESL em pacientes com neuralgias cranianas (56% tinham neuralgias do trigêmeo) que haviam respondido bem à CBZ ou OXC, mas experimentaram reações adversas a essas drogas. A resposta à AEP foi avaliada em 15 pacientes durante um período de 6 meses; a avaliação inicial incluiu os dados da história clínica, exame físico, testes complementares, informações sobre tratamentos anteriores e as reações adversas que motivaram a descontinuação do fármaco. Os pacientes foram posteriormente avaliados aos 3 e 6 meses para avaliar a eficácia do tratamento e quaisquer reações adversas. A resposta foi favorável em 13 dos 15 pacientes; a ESL foi melhor tolerada que CBZ e OXC.
Acetato de Eslicarbazepina em séries de casos de diferentes etiologias
Na 63ª Reunião Anual do SEN (2011, Barcelona), Tena Mora26 apresentou em formato de pôster os resultados de um estudo prospectivo e descritivo da eficácia e segurança da ESL em monoterapia em 6 pacientes com diferentes tipos de dor neuropática. As análises (hemograma completo, teste de coagulação, níveis de sódio e potássio, função renal e hepática) foram realizadas 1 e 3 meses após o início do tratamento; a EVA foi concluída durante a primeira consulta (EVA 1), 1 mês (EVA 2), e 3 meses de seguimento (EVA 3). O estudo incluiu 4 pacientes com neuralgia do trigêmeo primário (100% mulheres; VAS 1: 8-10, VAS 2: 0-3, VAS 3: 0-3), um dos quais com sonolência que se resolveu quando a dose de manutenção foi dividida em 2 doses diárias; um paciente com dor pós-operatória (homem de 80 anos, VAS 1: 9; o tratamento foi interrompido aos 4 dias devido a sonolência; a CBZ foi gradualmente interrompida em paralelo); e uma paciente com dor facial idiopática persistente (mulher de 70 anos; VAS 1: 9, VAS 2: 8, VAS 3: 8). Nenhum dos pacientes apresentou alterações nos resultados das análises sanguíneas durante o período do estudo (3 meses). O autor enfatiza os efeitos analgésicos da ESL para neuralgia primária do trigêmeo.
Na 66ª Reunião Anual do SEN, García Arguedas et al.27 apresentaram os resultados de um estudo retrospectivo e descritivo de 10 pacientes com dor neuropática tratados com ESL em monoterapia. Analisaram as causas da dor, a dose utilizada, a eficácia do tratamento (utilizando escores basais e VAS de 3 meses) e a tolerabilidade ao tratamento. As causas da dor foram neuralgia do trigêmeo em 5 pacientes, PDN em 3 e PHN em 2. A dose mais freqüentemente utilizada foi de 800mg (dose máxima de 1200mg em um paciente). O escore médio de VAS foi de 8,2 na consulta de linha de base e 2,4 na consulta de seguimento de 3 meses, com uma diminuição global de mais de 50% na intensidade da dor. Quanto à tolerabilidade, a reação adversa mais freqüente foi tonturas; um paciente desenvolveu hiponatraemia leve, mas não suspendeu o tratamento.
Durante a 67ª Reunião Anual do SEN, Pagola Lorz et al.28 apresentaram sua experiência com ESL como tratamento de segunda linha para dor neuropática refratária às drogas tradicionais. Este estudo descritivo e retrospectivo analisou a resposta à ESL em 10 pacientes com dor neuropática mal controlada. As principais variáveis foram causa da dor, dose de AEP, melhora da dor (classificada como “muito melhor”, “melhor”, “sem alteração” ou “pior”), tratamento concomitante para dor neuropática e reações adversas. As causas da dor foram neuralgia do trigêmeo em 6 pacientes, neuralgia glosofaríngea em um, PHN em 2 e dor talâmica em um. Os pacientes receberam uma dose média de 800mg de ESL; 400mg foi suficiente para 3 pacientes, enquanto 2 necessitaram de 1200mg. Sete dos 10 pacientes relataram sentir-se “muito melhor”, 2 sentiram “melhor”, e o restante relatou “sem alterações”. Em relação ao tratamento concomitante, 3 pacientes receberam gabapentina, um recebeu pré-gabalina e outro recebeu amitriptilina. Reações adversas (apatia, tonturas, visão embaçada) foram leves e transitórias, não necessitando, em nenhum caso, de interrupção do tratamento.
Na 67ª Reunião Anual do SEN, Bermejo Velasco et al.29 apresentaram os resultados de um estudo retrospectivo das histórias clínicas de 10 pacientes com dor neuropática e que receberam ESL. Os autores avaliaram a eficácia da ESL utilizando a EVA, o percentual de respondedores (> 50% de diminuição da intensidade da dor), o percentual de pacientes sem dor, diminuição do tratamento concomitante, reações adversas, dose utilizada, programação de titulação e etiologia da dor neuropática. Os pacientes foram acompanhados por uma média de 6,1 meses. O estudo incluiu um total de 32 pacientes. A dose média de ESL foi de 920±220mg/dia. A intensidade da dor diminuiu em média 4,4±1,6 pontos, com 46% dos pacientes identificados como respondedores e 13% livres de dor. Cerca de 78% dos pacientes continuaram com o tratamento. As principais razões para a interrupção do tratamento foram ineficácia, sonolência e tontura.
As tabelas 1 e 2 resumem os resultados dos ensaios clínicos, estudos observacionais e relatos de casos incluídos nesta revisão.
Resumo dos estudos clínicos incluídos nesta revisão.
| Tipo de estudo | Referência | Tamanho da amostra | Dose | ESL dose | Duração | Resultados principais | Segurança |
|---|---|---|---|---|---|---|---|
| Teste Fase II | Kress et al.14 | 557 | PDN | Placebo, ESL 400mg BID, ESL 800mg QD, ESL 600mg BID, ESL 1200mg QD, e ESL 800mg BID | 15 semanas | Não foram observadas diferenças estatisticamente significativas entre os indivíduos que receberam placebo e aqueles que receberam ESL para o controle da dor (análise de eficácia primária), de acordo com os escores da NPRS.O percentual de indivíduos que apresentaram redução de 1% na intensidade de dor em a≥30 foi maior no grupo que recebeu 400mg de ESL BID (62,5%) do que no grupo placebo (44,8%) (P = .0230). | A incidência de reações adversas variou de 38,0% no grupo placebo a 51,8% no grupo tratado com 1200mg de ESL QD. As reacções adversas mais frequentes foram vómitos, tonturas e náuseas. |
| Teste Fase III | https://clinicaltrials.gov/ct2/show/study/NCT01129960?term=eslicarbazepine&rank=1915 | 332 | PDN | Placebo, ESL 1600mg QD, ESL 1200mg QD, e ESL 800mg QD | 15 semanas | Não foram observadas diferenças estatisticamente significativas entre os indivíduos que receberam placebo e aqueles que receberam ESL para o controle da dor, de acordo com os escores da NPRS. | A incidência de reações adversas variou de 12,20% no grupo placebo a 63,10% no grupo tratado com 1600mg de ESL QD. As reações adversas mais frequentes foram vertigem, náusea e hiponatraemia (esta última foi dose-dependente). |
| Teste Fase II | Kress et al.18 | 567 | PHN | Placebo, ESL 400mg BID, ESL 800mg QD, ESL 600mg BID, ESL 1200mg QD, e ESL 800mg BID | 11 semanas | A análise de intenção de tratamento não mostrou diferenças estatisticamente significativas entre os grupos placebo e ESL em termos de intensidade de dor medida com o NPRS (análise de eficácia primária).De acordo com a análise por protocolo, a intensidade da dor diminuiu significativamente mais no grupo que recebeu 800mg de ESL BID do que no grupo placebo (P = .0277). | A incidência de reacções adversas variou de 31,2% no grupo placebo a 54,4% no grupo que recebeu 800mg de BID de ESL. As reacções adversas mais frequentes foram tonturas, sonolência, dores de cabeça, náuseas e vertigens. |
| Teste Fase III | https://clinicaltrials.gov/ct2/show/study/NCT01124097?term=eslicarbazepine&rank=18§=X7015619 | 240 | PHN | Placebo, ESL 1600mg QD, ESL 1200mg QD, e ESL 800mg QD | 15 semanas | Não foram observadas diferenças estatisticamente significativas entre os indivíduos que receberam placebo e aqueles que receberam ESL para o controle da dor, de acordo com os escores da NPRS. | A incidência de reações adversas variou de 10% no grupo placebo a 76,67% no grupo tratado com 1600mg de ESL QD. As reacções adversas mais frequentes foram náuseas, tonturas e dores de cabeça. |
BID: duas vezes ao dia; ESL: acetato de eslicarbazepina; NPRS: Numeric Pain Rating Scale; PDN: neuropatia diabética dolorosa; PHN: neuralgia pós-terpética; QD: uma vez ao dia.
Resumo dos estudos observacionais e ensaios clínicos incluídos na revisão.
| Tipo de estudo | Referência | Tamanho da amostra | Dose | Dose de LES | Duração | Resultados principais | Segurança |
|---|---|---|---|---|---|---|---|
| Prospectiva, estudo descritivo, observacional | García Escrivá et al.16 | 8 | PDN com falha no tratamento anterior | ESL 400mg/dia (2 pacientes) e ESL 800mg/dia (5 pacientes) | 12 semanas | Aprimoramento nas pontuações da escala DN4, HADS, VAS, PGI-I e CGI-I. | 1 desistência devido a tontura |
| Caso clínico | Gaber et al.20 | 1 | TN associado à esclerose múltipla foi bem administrado com CBZ, mas a droga foi descontinuada devido à hiponatraemia sintomática recorrente. | 400mg/dia | – | Controle de dor excelente | Tolerância boa sem alterações nos níveis de sódio plasmático |
| Caso clínico | Cuadrado et al.21 | >1 | Epicrania fugax refratária com baixa tolerância de CBZ | 1600mg/dia | – | Significativo melhoria na frequência e intensidade da dor | Tolerância à boa |
| Série de casos | Cação et al.22 | 1 | SUNCT | 800mg/dia | – | Gestão da dor e diminuição do número de ataques por dia | O paciente morreu devido a causas não relacionadas com a ESL um ano depois. |
| Caso clínico | Aledo Serrano et al.23 | >1 | Epicrania fugax refratária com baixa tolerância de CBZ | 1200mg/dia | – | Asintomático | Bom tolerância |
| Retroactivo, estudo descritivo, observacional | Sánchez Larsen et al.24 | 10 | TN (4 pacientes em monoterapia e 6 em politerapia) | NA | Tempo de seguimento: 24,7 meses | Intensidade de crescimento e frequência de ataque diminuíram em 9 dos 10 pacientes. | Dois pacientes desistiram devido a reacções adversas leves (tonturas). Não foram relatados efeitos adversos graves. Um paciente apresentou hiponatraemia. |
| Estudo retrospectivo, descritivo, observacional | Abril-Jaramillo et al.25 | 15 | Nevralgia craniana (TN em 56% dos pacientes), com boa resposta à CBZ ou OXC mas associada a reacções adversas aos medicamentos | NA | 6 meses | Resposta favorável em 13 dos 15 pacientes | Tolerabilidade de aproximadamente 90% |
| Prospectiva, descritiva, estudo observacional | Tena Mora26 | 6 | 4 TN, 1 dor pós-choque, 1 dor facial persistente idiopática (tudo em monoterapia) | NA | 3 meses | Efeitos analgésicos significativos para TN | Um paciente com TN apresentou sonolência, que se resolveu quando a dose de manutenção foi dividida em 2 doses. O paciente com dor pós-costalgia suspendeu o tratamento aos 4 dias devido a sonolência. Nenhum paciente apresentou alterações nos resultados das análises durante o período do estudo. |
| Estudo retrospectivo, descritivo e observacional | García Arguedas et al.27 | 10 | 5 TN, 3 PDN, e 2 PHN (monoterapia) | Dose média: 800mg/dia (dose máxima de 1200mg/dia em um paciente) | 3 meses | Diminuição de 50% na intensidade da dor (SAV) | Tonturas, hiponatraemia leve em um paciente, sem drop-outs |
| Estudo retrospectivo, descritivo, observacional | Pagola Lorz et al.28 | 10 | 6 TN, 1 neuralgia glosofaríngea, 2 PHN, e 1 dor talâmica (sem resposta a drogas tradicionais) | Dose média: 800mg/dia; 3 pacientes requereram tão pouco quanto 400mg/dia enquanto 2 requereram 1200mg/dia. | NA | Sete pacientes relataram sentir-se “muito melhor”, 2 sentiram “melhor”, e os restantes relataram “sem alterações”. | Reacções adversas leves e transitórias (apatia, tonturas, visão turva) que não resultaram em descontinuação da droga |
| Estudo retrospectivo, descritivo, observacional | Bermejo Velasco et al.29 | 32 | Diferentes etiologias da dor neuropática refratária às drogas tradicionais. | Dose média: 920±220mg/dia | Tempo de seguimento médio: 6,1 meses | Diminuição da intensidade da dor de 4,4±1,6 pontos na EVA; 46% dos pacientes que responderam (> diminuição de 50% na intensidade da dor) e 13% dos pacientes sem dor | 78% dos pacientes continuaram o tratamento. As principais razões para a interrupção do tratamento foram ineficácia, sonolência e vertigem. |
CBZ: carbamazepina; CGI-I: Clinical Global Impression of Improvement scale; ESL: acetato de eslicarbazepina; HADS: Escala de Ansiedade e Depressão Hospitalar; NA: não disponível; OXC: oxcarbazepina; PDN: neuropatia diabética dolorosa; PGI-I: Patient Global Impression of Improvement scale; PHN: neuralgia pós-terpética; SUNCT: dor de cabeça neuralgiforme unilateral de curta duração com injeção conjuntival e laceração; TN: neuralgia do trigêmeo; VAS: Visual Analogue Scale.
Discussão
Drogas da família das dibenzazepinas podem causar hiponatraemia (nível de sódio
135mmol/L); esta é uma reação adversa comum à CBZ e OXC. A incidência de hiponatraemia secundária ao tratamento com CBZ varia entre 4,8% e 40%,30,31 Há evidências crescentes dos efeitos deletérios da hiponatraemia, mesmo em casos leves, especialmente em pacientes idosos, entre os quais a dor neuropática é relativamente freqüente.32,33 A hiponatraemia induzida por drogas deve ser considerada como um motivo para mudar o tratamento.
Os médicos normalmente enfrentam um dilema quando a CBZ é a única droga capaz de controlar um problema clínico específico, como a neuralgia do trigémeo. A ESL pode constituir uma alternativa em pacientes com reações adversas à CBZ. A hiponatraemia tem sido raramente relatada em ensaios clínicos e estudos observacionais de ESL em pacientes com epilepsia34-36; a mudança de CBZ ou OXC para ESL em pacientes que desenvolveram hiponatraemia parece, portanto, ser uma opção eficaz e bem tolerada. Os níveis de sódio ainda devem ser monitorados, entretanto, já que alguns pacientes continuam a apresentar hiponatraemia após a troca de drogas.37
Essas diferenças nos perfis dos antiepiléticos da família das dibenzazepinas podem resultar em diferentes níveis de eficácia, tolerabilidade e aderência,38 o que pode levar os médicos a considerar a troca de uma droga para outra na mesma família para adaptar o tratamento às características de cada paciente. O projeto EPICON, no qual um painel de especialistas em epilepsia adotou o método Delphi, avaliou situações específicas e a metodologia de mudança de CBZ ou OXC para ESL. O objetivo do estudo foi emitir recomendações consensuais para mudar de CBZ ou OXC para ESL em determinados pacientes. As principais recomendações são as seguintes: 1) A transição de CBZ para ESL deve ser realizada progressivamente durante 1 a 3 semanas, empregando uma relação CBZ:ESL de 1:1.3. 2) A mudança de CBZ para ESL é recomendada para pacientes que frequentemente esquecem de tomar sua medicação, aqueles que trabalham em turnos rotativos, pacientes polimedicados, pacientes com problemas cognitivos, pacientes com osteopenia/osteoporose grave, pacientes com dislipidemia ou doença hepática que não seja insuficiência hepática aguda e homens com disfunção erétil causada pela CBZ. 3) OXC pode ser mudado para ESL durante a noite a uma relação de dose de 1:1; isto é recomendado para pacientes que frequentemente esquecem de tomar sua medicação, aqueles que trabalham em turnos rotativos, pacientes polimedicados, ou pacientes com problemas cognitivos. 4) A troca de medicamentos não é recomendada para pacientes que apresentam erupção cutânea secundária ao tratamento com CBZ ou OXC.39 Embora essas recomendações se apliquem a pacientes com epilepsia, podem ser úteis em outras situações clínicas (diferentes tipos de dor neuropática, neuralgia do trigêmeo e outros tipos de dor de cabeça) associadas à má aderência ou tolerabilidade da CBZ ou OXC.
Conclusões
Dado o mecanismo de ação da ESL (interação seletiva com o estado inativo da VGSC através da inativação lenta, em contraste com a inativação rápida da CBZ e OXC, e a inibição do hCaV3.2 correntes com maior afinidade do que a CBZ), inicialmente parece ser uma boa opção para o tratamento da dor neuropática, dor de cabeça e neuralgia craniana.
No entanto, as evidências são muito escassas para recomendar a ESL para essas indicações. A maioria das evidências disponíveis vem de estudos abertos, observacionais com amostras pequenas e sem grupo controle. Além disso, alguns dos estudos incluídos nesta revisão tratam de diferentes entidades clínicas26-29 com diferentes mecanismos fisiopatológicos. Portanto, a heterogeneidade dos dados nos impede de estabelecer qualquer conclusão geral sobre a eficácia do ESL. Curiosamente, os estudos clínicos sobre a SLEE como tratamento da dor neuropática (NDP e NPP) não encontraram reduções estatisticamente significativas na intensidade da dor.
A escassez de estudos publicados sobre o assunto pode sugerir um viés de publicação. De fato, os estudos clínicos fase III incluídos em nossa revisão não foram publicados.
Em conclusão, a ESL pode constituir uma alternativa válida para o tratamento da dor neuropática, cefaléia e nevralgias cranianas em pacientes com má resposta ou intolerância às drogas tradicionais, especialmente no caso da neuralgia do trigêmeo; estudos mais randomizados com amostras maiores são necessários para confirmar esta hipótese. A utilidade da ESL para neuralgia do trigêmeo pode estar associada à excelente resposta da doença à CBZ e às semelhanças bioquímicas entre as duas drogas.
Conflitos de interesse
O estudo está de acordo com os padrões éticos e critérios de autoria da revista. Os autores não têm conflitos de interesse a declarar.
Leave a Reply