To co-ox or not to co-ox
Geschiedenis
De studie van de zuurstofverzadiging in het bloed vindt haar oorsprong in de vroege hetelucht- en waterstofballonvluchten die in de jaren 1800 in Frankrijk werden gemaakt. De ballonbemanningen merkten nadelige effecten op wanneer hun ballonnen boven de 7.000 meter stegen.
Op 15 april 1875 steeg de ballon Zenith op tot een hoogte van 8.600 meter met een bemanning van drie. Zonder waarschuwing raakten hun armen en benen verlamd en twee van hen kwamen om. De tragedie werd beschouwd als een nationale catastrofe en zij werden herdacht als “martelaren van de wetenschap op zoek naar de waarheid”.
De oorzaak van de catastrofe werd onthuld in 1878 na de publicatie van La Pression Barometrique door de Franse wetenschapper Paul Bert. In dit boek werden de fysiologische symptomen besproken van dieren en mensen die aan een lage barometerdruk werden blootgesteld.
Het was Bert die als eerste eenvoudige krommen publiceerde die het verband weergeven tussen de partiële druk van zuurstof in de lucht en het zuurstofgehalte in het bloed. Dit was de eerste in vivo dissociatiecurve. Bert was ook de eerste die aantoonde dat bloed meer zuurstof opnam als de temperatuur daalde.
In 1885 publiceerde Christian Bohr uit Kopenhagen een meer verfijnde dissociatiecurve voor een hemoglobine-oplossing (niet volbloed) die eruitzag als een hyperbool. In 1903 ontdekte Bohr de s-vormige dissociatiecurve voor volbloed (fig. 1).
In het volgende jaar toonden Bohr en collega’s aan dat de positie van de dissociatiecurve werd beïnvloed door de hoeveelheid kooldioxide in het bloed.
In 1910 deed Joseph Barcroft van Cambridge de ontdekking dat de dissociatie van oxyhemoglobine werd beïnvloed door pH, ionensterkte en temperatuur (Barcroft’s groep ontdekte ook de verhoogde zuurstofaffiniteit van foetaal hemoglobine veel later, in de jaren 1930). Deze ontdekkingen werden van cruciaal belang voor de studie van de ademhalingsfysiologie.
Een wiskundige beschrijving van de dissociatiecurve van oxyhemoglobine werd voor het eerst voorgesteld door Archibald Hill in 1910. In die tijd was het moleculaire gewicht van hemoglobine echter nog niet bekend en waren er verschillende meningen over hoe de vergelijking moest worden geïnterpreteerd. Pas in 1979 stelde John Severinghaus een gewijzigde vergelijking voor die beter bij de experimentele gegevens past:
sO2 = ( +1)-1
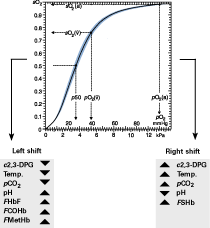
FIG. 1. Zuurstof-hemoglobine dissociatiecurve en factoren die de curve naar rechts of links verschuiven. 2,3-DPG is 2,3-difosfoglyceraat, een organische verbinding die normaal aanwezig is in erytrocyten en die zich bindt aan hemoglobine en de neiging heeft de affiniteit van hemoglobine voor zuurstof te verminderen.
Hoe de zuurstofverzadiging te meten
Er zijn twee basismanieren om de zuurstofverzadiging van hemoglobine in bloed te meten: (1) gasometrisch en (2) spectrofotometrisch.
Gasometrische methoden berusten op het vrijkomen, de reactie en de geselecteerde reabsorptie van gassen in een gesloten systeem. Standaard gaswetten worden gebruikt om de gasdruk te relateren aan de zuurstoffractie. De klassieke gasometrische procedure wordt de Van Slyke-methode genoemd. De ontwikkeling van spectrofotometrische methoden gaat terug tot Isaac Newton’s studies van licht in de jaren 1600.
Werk van Lambert (1760) en Beer (1852) resulteerde in de Beer-Lambert wet die de transmissie/absorptie van licht beschrijft als een logaritmische functie van de concentratie van de absorberende moleculen in oplossingen .
De eerste spectrofotometrische metingen van bloed werden verricht in de jaren 1930. In de jaren 1950 werd een spectrofotometer gebruikt voor het meten van hemoglobine en zijn derivaten. Specifieke instrumenten voor het meten van de zuurstofverzadiging werden in de jaren 1960 ontwikkeld. Het gebruik van ooroximeters voor continue schattingen van de arteriële saturatie kwam voort uit luchtvaartstudies in zowel Duitsland als Amerika tijdens de Tweede Wereldoorlog. Wijdverbreid gebruik van pulsoximeters ontwikkelde zich in de jaren 1980.
Een oximeter (vaak een CO-Oximeter genoemd, de naam van het eerste commercieel populaire apparaat gemaakt door Instrumentation Laboratories) bestaat uit een hemolyzer-eenheid, een fotolamp, een lenssysteem en detecterende fotodiodes.
Het bloedmonster wordt verwarmd tot 37 °C en door hemolyse met hoogfrequente trillingen ontstaat een doorschijnende oplossing. Onvolledig gehemolyseerde rode bloedcellen kunnen licht verstrooien en meetfouten introduceren (er zijn hemoximeters op de markt die het monster niet hemolyseert).
Het licht van de lamp wordt gefilterd en gefocusseerd om door het bloedmonster te gaan. Het doorgelaten licht wordt dan gefocusseerd door een diffractierooster dat het licht scheidt in een continu spectrum.
Een masker selecteert vervolgens de specifieke golflengten die voor de meting worden gebruikt. Deze afzonderlijke golflengten worden op fotodiodes gericht die elektrische stromen produceren evenredig aan de lichtintensiteiten.
De lichtintensiteiten zijn afhankelijk van de hoeveelheid licht die door de verschillende concentraties en typen hemoglobine wordt geabsorbeerd. Wanneer de concentraties van de verschillende soorten hemoglobine bekend zijn, kan de verzadiging worden berekend met behulp van de onderstaande vergelijkingen.
Concentratie van totaal hemoglobine
ctHb is de concentratie (c) van totaal hemoglobine (tHb) in het bloed. Totaal hemoglobine omvat in principe alle soorten hemoglobine:
- Hemoglobine (HbA) – normaal hemoglobine van een volwassene is een complex eiwit dat ijzer bevat en in staat is zuurstof in het bloed te transporteren.
- Deoxyhemoglobine (HHb) – niet-zuurstofhoudend (vroeger “gereduceerd” genoemd) hemoglobine.
- Oxyhemoglobine (O2Hb) – zuurstofhoudend hemoglobine, dat vier moleculen zuurstof per hemoglobinemolecule bevat.
- Carboxyhemoglobine (COHb) – hemoglobine gebonden aan koolmonoxide, een binding die ongeveer 210 keer sterker is dan de affiniteit zuurstof-hemoglobine; verhindert de normale overdracht van zuurstof en kooldioxide in het bloed.
- Methemoglobine (MetHb) – hemoglobinemolecule waarvan het ijzer zich in de geoxideerde, ferrische toestand bevindt; nutteloos voor de ademhaling; in het bloed aangetroffen na vergiftiging met acetanilide, kaliumchloraat en andere stoffen.
- Sulfhemoglobine – hemoglobine in combinatie met zwavel. Het zeer zeldzame en niet-zuurstofdragende sulfhemoglobine is niet opgenomen in het gerapporteerde ctHb.
- Foetaal hemoglobine (HbF) – het belangrijkste type hemoglobine in de zich ontwikkelende foetus. De zuurstofdissociatiecurve voor foetaal hemoglobine is naar links verschoven in vergelijking met hemoglobine van volwassenen.
De concentratie van totaal hemoglobine kan worden uitgedrukt als:
ctHb = cO2Hb + cHHb + cCOHb + cMetHb
Het systematische symbool voor arterieel bloed is ctHb(a). Het symbool voor de analysator kan tHb of ctHb zijn.
Referentiebereiken
ctHb(a) referentiebereik (volwassene):
- Mannelijk: 8,4-10,9 mmol/L (13,5-17,5 g/dL)
- Vrouwelijk: 7,4-9,9 mmol/L (12,0-16.0 g/dL)
Zuurstofverzadiging
Definitie
sO2 is de zuurstofverzadiging (soms functionele verzadiging genoemd) en wordt gedefinieerd als de verhouding tussen de concentraties van O2Hb en HHb + O2Hb:
![]()
sO2, zoals hierboven gedefinieerd, geeft onmiddellijk aan of meer zuurstof door hemoglobine kan worden getransporteerd – of dat een verhoging van pO2 alleen de fysisch opgeloste zuurstof zal verhogen.
Het systematische symbool voor arterieel bloed is sO2(a). Het symbool voor de analysator kan sO2 zijn.
Referentiebereiken
sO2(a) normaal bereik (volwassene): 95-99 %
Hemoglobine fractie van totaal hemoglobine (fractioneel oxyhemoglobine)
Definitie
FO2Hb wordt gedefinieerd als de verhouding tussen de concentraties van O2Hb en tHb (cO2Hb/ctHb). Zij wordt als volgt berekend:
![]()
Het systematische symbool voor arterieel bloed is FO2Hb(a).
Het symbool voor de analysator kan O2Hb of FO2Hb zijn.
Referentiebereiken
FO2Hb(a) referentiebereik (volwassene): 94-98 %
Zuurstofspanning bij 50 % verzadiging van bloed
Definitie
p50 is de zuurstofspanning bij halve verzadiging (50 %) van bloed en wordt berekend uit de gemeten zuurstofspanning en zuurstofsaturatie door extrapolatie langs de zuurstofdissociatiecurve naar 50 % verzadiging. Het systematische symbool voor p50 bepaald uit arterieel bloed is p50(a). Het symbool van de analysator kan p50(act) of p50 zijn.
Referentiebereiken
p50(a) referentiebereik (volwassene): 24-28 mmHg (3,2-3,8 kPa)
Gemeten verzadiging
Een oxymeter is een spectrofotometer die is ontworpen om de zuurstofverzadiging in het bloed te meten. Elk type hemoglobinemolecule (d.w.z., HHb, O2Hb, COHb en MetHb) heeft zijn eigen lichtabsorptiespectrum.
Oximeters bevatten lichtbronnen bij geselecteerde golflengten die overeenkomen met de absorptiespectra van de te meten hemoglobinemoleculen. Aldus moet een basisoxymeter die sO2 kan meten, de absorptie bij slechts twee golflengten bepalen, één voor HHb en één voor O2Hb.
Pulsoximeters gebruiken twee golflengten die door de huid kunnen worden doorgegeven (bijv, een vinger of teen), waardoor niet-invasieve controle van de saturatie mogelijk is.
Oxymeters met twee golflengten kunnen echter misleidende schattingen geven van het zuurstofgehalte van bloed in aanwezigheid van verhoogde niveaus van COHb en MetHb.
Om FO2Hb te verkrijgen, moet een oximeter ten minste vier golflengten gebruiken (één elk voor HHb, O2Hb, COHb en MetHb). Momenteel zijn voor dergelijke oximeters (die soms hemoximeters worden genoemd om ze te onderscheiden van pulsoximeters) bloedmonsters van de patiënt nodig.
De relatie tussen FO2Hb en sO2 is:
FO2Hb = sO2 × (1 – FCOHb – FMetHb)
Het is belangrijk te weten dat de “zuurstofverzadiging” zoals die door pulsoximeters wordt gemeten, niet FO2Hb is, maar sO2. De vergelijking hierboven drukt de relatie uit tussen FO2Hb en sO2.
Dus, als er geen abnormale hemoglobines (dyshemoglobines) aanwezig zijn, is de fractie van zuurstofhoudende hemoglobines gelijk aan de zuurstofverzadiging, uitgedrukt als een fractie. Het verschil tussen beide is te zien in het onderstaande voorbeeld. Merk op dat dit in de eerste plaats nuttig is wanneer het wordt gebruikt in relatie tot ctHb.
- ctHb = 10 mmol/L
- cHHb = 0,2 mmol/L
- cCOHb = 3 mmol/L ~ 30 %
- cO2Hb = 6,8 mmol/L
![]()
![]()
Gecalculeerde saturatie
De meeste bloedgasanalysatoren zonder CO-oximeter bieden een uitlezing voor de saturatie.
De waarde wordt dan echter berekend in plaats van gemeten. De berekening is complex en houdt rekening met de verschillende factoren die de vorm van de oxyhemoglobine-dissociatiecurve kunnen beïnvloeden. De wiskundige beschrijving en de variabelen hierin variëren voor verschillende merken analyzers.
Klinisch belangrijke fouten kunnen het gevolg zijn van het gebruik van geschatte sO2 in andere berekeningen, zoals die voor shuntfractie en zuurstofgehalte .
Het wordt ontraden om een schatting van sO2 te maken uit een meting van pO2 en omgekeerd met behulp van een standaard ODC. De gevolgen hiervan blijken uit fig. 2, die gebaseerd is op de meting van 10.179 bloedmonsters .
Daaruit blijkt dat bij een sO2 van 90 % de corresponderende pO2 ligt tussen 29-137 mmHg (4-18 kPa) en een pO2 van 60 mmHg (8 kPa) correspondeert met een sO2 van 70 tot 99 %.
Al met al is de sO2 het meest betrouwbaar door de meting met een CO-oximeter. Dit geeft tevens het voordeel dat ook FO2Hb, FCOHb en FMetHb kunnen worden gerapporteerd.
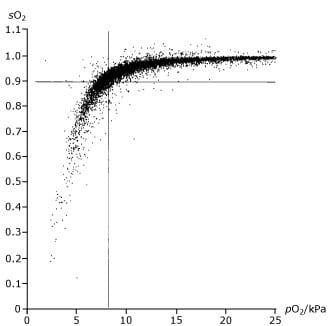
FIG. 2. Grafiek van bloedverzadigingsmetingen die een slechte correlatie vertoont met de partiële druk van zuurstof in het bloed.
Clinische toepassing
Zuurstofgehalte is een belangrijke indicator van het zuurstoftransport in het lichaam. Het zuurstoftransport van arterieel bloed wordt gebruikt om het vermogen van zuurstoftransport van de longen naar het weefsel te beoordelen. Zuurstoftransport, gedefinieerd als de hoeveelheid zuurstof die per liter arterieel bloed wordt vervoerd, hangt voornamelijk af van:
- Het totale gehalte aan zuurstof in het arteriële bloed, ctO2 – de belangrijkste parameter voor de evaluatie van het zuurstoftransport
- De concentratie van hemoglobine in het bloed (ctHb)
- De concentratie van dyshemoglobines (cCOHb en cMetHb)
- De arteriële zuurstofspanning (pO2)
- De arteriële zuurstofverzadiging (sO2), die weer wordt bepaald door pO2 en p50
Zuurstofverzadiging is dus niet de enige indicator van zuurstoftransport. De aanwezigheid van dyshemoglobines en/of een lage concentratie hemoglobine kunnen ernstige verminderingen van de zuurstoftransportcapaciteit van het arteriële bloed veroorzaken.
Conclusie
Voor vele doeleinden is sO2 (gemeten door een pulsoxymeter of berekend door een bloedgasanalysator) voldoende om klinische beslissingen te nemen. Bij juiste toepassing kan pulsoximetrie voordelen opleveren, zoals continue bewaking, lagere kosten en minder bloedverlies (belangrijk bij de verzorging van pasgeborenen).
Wanneer echter vergiftiging door koolmonoxide of andere stoffen die hemoglobine kunnen beïnvloeden wordt vermoed, is FO2Hb, zoals gemeten met een bench hemoximeter, vereist.
Clinische richtlijnen voor het gebruik van pulsoximeters en hemoximeters zijn beschikbaar bij de American Association for Respiratory Care . Aanverwante aanbevelingen zijn gepubliceerd door het National Committee for Laboratory Standards.
Leave a Reply