右肝拡大術の新しい手術手技:臍帯裂孔止血術と右門脈閉塞術(ALTPS). 臨床例|Cirugía Española(英語版)
はじめに
広範囲切除や2段階肝切除(TSLR)で、残存肝機能量(RLV)が不十分な場合、経皮的門脈塞栓術(PPVE)3,4や術中門脈結紮術(IPVL)が行われる5。-7 どちらの術式でも門脈閉塞に伴う問題がいくつかあり、肝内側副血行路の形成による肥大化の遅れ(3~8週間)、あるいは肥大化なし3-7(肝大切開後の肝不全8,9(PLF)、腫瘍の進行10,11による手術不能の危険性がある)などがあります。 2011年、Baumgartら12は、左側区域にRLVを有する3名の患者に対し、TSLRを実施し右三等分切除を得るために、右門脈結紮と臍裂レベルのin situ二分割を行い、9日間でII-IIIセグメントのRLV肥大を達成したと報告している。 この結果は、他の著者13,14によっても、同じ手技でCantlie線に切開することにより再現された。 この新しい手技は、associating liver partition and portal ligation for staged hepatectomy (ALPPS) 15 と呼ばれ、迅速な肥大を達成し、肥大不全や腫瘍の進行といった従来の閉塞法の問題を防ぐことができるので、大きな前進といえる。 2011 年 9 月、我々は二分割の代わりに Cantlie ラインに止血帯を挿入し、肝止血と門脈閉塞を組み合わせた段階的肝切除術を行い、7 日間で RLV 肥大を達成した22) 。
本論文の目的は、右葉に大きな肝腫瘤があり右三等分切除を必要とする患者に対し、Cantlie lineの代わりに臍裂に止血帯を挿入する我々の手技を行い、II-IIIセグメントの肥大を得た臨床例を紹介することである。
臨床例と手術手技
2002年10月、51歳男性に6cmの右腎高血圧症に対する手術が行われたが、腺病変や血管侵襲はなかった。 右腎摘出術とリンパ節郭清が行われ,9年間無症状が続いた。 2011年11月、トランスアミナーゼの上昇が認められ、超音波検査が依頼された。 その結果、右肝葉、第Ⅰ分節、下大静脈を包含する大きな腫瘤が検出された。 ビリルビン、トランスアミナーゼ、凝固、腫瘍マーカーは正常であった。 コンピュータ断層撮影(CT)により,右葉の大部分,右および中央の上肝静脈,セグメントI,周囲の下大静脈を70%以上侵襲する20cmの腫瘤を検出した(左腎臓分岐部上3cmから左上肝静脈下2cmまでの侵襲)(図1)。 肝臓の容積分析では、RLVは3870ml(総肝容積20%)、肝容積/体重商は0.5と検出された。 肝外病変はPETでは検出されなかった。 我々の基準23ではFLVは不十分と判断し、ALTPS法による2段階肝切除を指示した
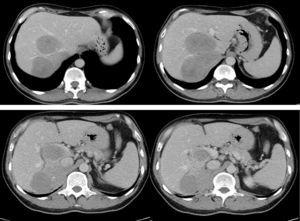
解剖学的右葉、セグメントI、下大静脈に浸潤した大きな腫瘍を示す術前CT(4画像)、セグメントII-IIIのみが遊離している(20%の残存量)。
最初の外科的介入
腫瘍の播種を否定するために、肋骨下両側切開で肝臓と腹腔を診察しました。 胆嚢摘出術と胆管造影による経膀胱的ドレナージが行われた。 前述の右肝動脈の解離は血管ループを使用して行った。 右門脈を切離した。 IVCは左腎静脈の上、左肝上静脈の下をVessel-loopを用いて切離した。 腫瘍の転移がなく、2期でR0切除が可能であることが確認されると、Vicryl 3mm V152 Ethicon®製止血帯を臍裂部に挿入した。 止血帯は中静脈と左肝上静脈の間を通り、左葉の基部を回ってRex凹部を通り左門脈ペディクルまで継続した。 ここでは、止血帯を閉じたときにペディクルが閉塞しないように、グリソン外法で通過させた。 その後、鎌状靭帯の右側(臍裂)に溝を作り、これを結んで実質と肝内側副血行路のみを閉塞させた。 超音波検査ではⅡ-Ⅲ節とⅣ節間の循環が完全に停止していることが確認された。 手術時間は180分で、出血は最小限であった。 術後Quick値は70%低下し、GPT値は240U/lに上昇した。 術後4日目に合併症なく退院した。 術後7日目にCTスキャンによる体積測定が行われた。
術後体積測定と二次介入
RLVは953ml(全肝容積の31%)に上昇し、150%(573ml上昇)の増加を示した。 CT検査では,止血帯を介した側副血行がないこと,腫瘍の進行がないこと,腫瘍の切除性があることが確認された(図2)。 第二期手術は第一期手術後10日目に行われ、VCIクランプテストが行われ、完全寛容で静脈バイパスの必要なしとされた。 右胆管、右肝動脈、第IVセグメントの動脈枝を結紮し、左門脈を完全に分離・隔離した。 臍裂開脈による分割(Fig. 3)を行い、閉塞した第IV分枝の門脈を中上肝静脈と左上肝静脈の接合部まで結紮し、中上肝静脈を結紮(分割はin situ)して、解剖学的に右葉の残りの部分からII-III分枝を完全に切り離すことができるようにした。 ICVは左腎分岐部上と左肝上静脈下でクランプし、左腎上と右肝上静脈のオスティウムのレベルでVCIを切離した。 最後に、直径2cm、長さ8cmのリング状のゴアテックスグラフトを挿入した。 VCI閉塞時間は70分、手術時間は210分、出血量は600mlであった。 閉塞前にコントロール胆管造影を行い、残存胆管を正しく表示することができた。 術後Quick値57%低下、赤血球数2mg/dl増加、GPT値267IU増加のため2IUの輸血を必要とした。 術後48時間より抗凝集療法を行い,5日目に38℃の発熱があり,CTにて肝周囲に貯留物が認められた. CTで肝周囲に貯留物が認められ,放射線ドレーンで貯留物を除去し,術後12日目に退院となった. その後,定期的に検査を行い,2013年7月に最後のCT検査を行った(図4)。 2回目の手術から20ヶ月経過しても再発はなかった。
側副血行路のない止血帯マーカー、対応する血管および得られた肥大(150%体積増加)を示す7日目の対照的なコンピュータ断層撮影。
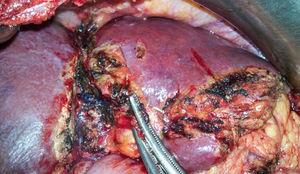
臍裂の右側に止血溝が認められる第2期インターベンションの術中画像.
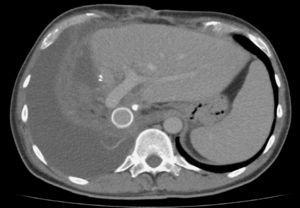
術後20ヶ月のコントロールCTでは、肥大した左外側セクター、透過性のあるゴアテックスグラフト、腫瘍の再発がないことが観察された。
Discussion
今回ご紹介するのは、右三等分切除を伴う後肝IVG完全切除で、リング状ゴアテックス2cmグラフトに置き換え、ALPPSまたはALTPSによる肥大術を行った文献上初めての症例です。 ALTPSはALPPSと同じ土台の上に成り立っており、両葉間の側副血行路を閉塞させ24、より早く肥大させることを意図している。 我々の手術手技の利点は、分割を行わず、二分割線(この場合は臍の裂け目)に止血帯を挿入するだけなので、両手術の攻撃性が変わることである。 「これらは同じ生理学的病理学的基盤を持つ2つのTSLR介入である」。 この症例は、ALTPSの場合、最初の介入がより少ないことを証明している:出血量は少なく、輸血は不要で、患者は術後4日で退院し、ALPPSの22%16と33%17と異なり、Pringle manoeuvreを使用する必要はない。 ALPPSの多施設共同研究16では、初回手術時の出血量は330ml、最大7500mlで、2名が15IUの大量輸血を必要とした。
ALPPSの合併症として多いのは初回手術時の側枝結紮による虚血でⅣ節が壊死し、感染や胆瘻、再手術遅延に至るものである11、16、19。
2回目の手術の後、患者は感染症を呈したが、X線ドレナージと抗生物質で治療し、IHPの兆候はなかった。 ALPPSの罹患率は53~64%であり、IHPの基準を満たす患者もいる。16~20 胆汁瘻や感染コレクションは頻繁に起こる合併症であり、一部の症例では死亡のリスクもある。
従来のEPPやLPIの欠点として、再生時間の延長に伴う腫瘍の進行10, 11が挙げられる7, 11, 25。 我々の症例では、10日後に再手術を行ったが、腫瘍の進行は見られなかった。R0切除が達成され、患者は2回目の手術後20ヶ月間無病だった。 1回目の手術では実質を切開せず、切開線と右門脈に止血を行うため、より侵襲的である。 ALPPSとALTPSの有効性を評価するため,また従来の門脈閉塞術(EPPとLPI)に対するこれらの新しい手技の有効性を評価するために,より大規模なシリーズが必要である。
Leave a Reply