Acetato de eslicarbazepina para el dolor neuropático, la cefalea y la neuralgia craneal: evidencia y experiencia | Neurología (English Edition)
Introducción
El acetato de eslicarbazepina (ESL) es un fármaco antiepiléptico de tercera generación aprobado en 2009 por la Agencia Europea del Medicamento y en 2013 por la Food and Drug Administration de Estados Unidos. Está disponible en el mercado español desde febrero de 2011. El fármaco está actualmente indicado como tratamiento complementario para pacientes adultos con crisis de inicio parcial con o sin generalización secundaria. La dosis inicial recomendada es de 400mg una vez al día, aumentando a 800mg una vez al día después de 1 a 2 semanas. La dosis puede aumentarse hasta 1200 mg, dependiendo de la respuesta del paciente.1
El ESL pertenece a la familia de las dibenzazepinas, al igual que la carbamazepina (CBZ) y la oxcarbazepina (OXC). Estos fármacos son estructuralmente diferentes entre sí en la posición 10,11. También difieren en cuanto a su metabolismo: La CBZ se metaboliza en CBZ-10,11-epóxido, a diferencia de la OXC, que se metaboliza en el metabolito activo S-licarbazepina (78,1%), y la ESL, que se metaboliza en el mismo metabolito pero en mayor proporción (93,9%) (Fig. 1).2,3 El número de dosis diarias también es diferente: dosis única en el caso de ESL y OXC de liberación prolongada (no disponible en España), 2 dosis de OXC de liberación inmediata y CBZ de liberación prolongada (no disponible en España), y de 2 a 3 dosis de CBZ de liberación inmediata. Según un estudio reciente de Soares-da-Silva et al.,4 el mecanismo de acción de la ESL tiene algunas características distintivas en comparación con las de otros fármacos de la misma familia: 1) la selectividad de la interacción con el estado inactivo del canal de sodio activado por voltaje (VGSC), 2) la reducción de la disponibilidad del VGSC a través de la mejora de la inactivación lenta, en lugar de la alteración de la inactivación rápida del VGSC, y 3) la inhibición de las corrientes entrantes de alta y baja afinidad del hCaV32 con mayor afinidad que la CBZ.
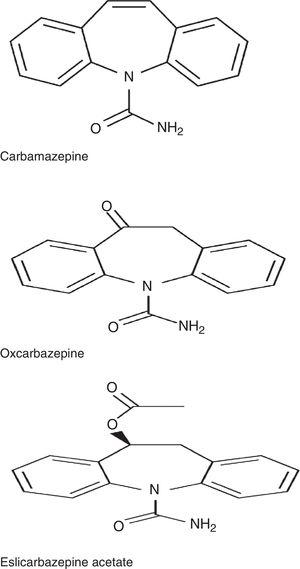
Estructura química de la carbamazepina, la oxcarbazepina y el acetato de eslicarbazepina.
De forma similar a OXC, ESL es moderadamente tóxico, siendo los efectos adversos más comunes mareos, náuseas, vómitos, somnolencia y diplopía. Tiene una semivida de eliminación de 13-24 horas, por lo que puede administrarse como una dosis única diaria. El ESL es un leve inductor de la UDP-glucuronosiltransferasa (UGT1A1) y de la isoforma CYP3A4 del citocromo P450. Esta actividad puede causar algunas interacciones clínicamente relevantes con la fenitoína, la warfarina y los anticonceptivos que contienen estrógenos.1
CBZ está indicada no sólo para la epilepsia, sino también para los episodios maníacos y para la profilaxis del trastorno afectivo bipolar, la neuralgia esencial del trigémino, la neuralgia esencial del glosofaríngeo y el síndrome de abstinencia del alcohol,5 mientras que OXC está indicado para el tratamiento de las crisis parciales con o sin generalización secundaria con crisis tónico-clónicas.6
Las últimas guías de práctica clínica coinciden en que los antidepresivos tricíclicos y de doble acción (venlafaxina, duloxetina) y los antiepilépticos gabapentina y pregabalina constituyen el tratamiento de elección para el dolor neuropático. El tramadol, los parches de lidocaína al 5% y los parches de capsaicina al 8% son tratamientos de segunda línea, mientras que los opioides fuertes constituyen la tercera línea de tratamiento.7
A diferencia de la CBZ, ni el ESL ni el OXC están indicados para el dolor neuropático, la cefalea o las neuralgias craneales. Sin embargo, otros fármacos antiepilépticos que no están indicados para estos escenarios clínicos, como la lamotrigina y lacosamida, se utilizan frecuentemente fuera de etiqueta en la práctica clínica.8-12
En este estudio, se revisa la evidencia disponible sobre el uso de ESL para el dolor neuropático, la cefalea y las neuralgias craneales para determinar si el fármaco puede ser una opción válida en pacientes con mala respuesta o intolerancia a los tratamientos tradicionales.
Desarrollo
Se realizó una búsqueda bibliográfica en PubMed y Google Scholar utilizando la siguiente estrategia de búsqueda: «acetato de eslicarbazepina AND dolor neuropático» y «acetato de eslicarbazepina AND cefaleas». Sólo se consideraron artículos de revistas científicas indexadas y se seleccionaron artículos originales e informes de casos publicados en inglés o en español. Como esta estrategia apenas arrojó resultados, decidimos ampliar la búsqueda incluyendo pósteres y comunicaciones orales sobre el mismo tema («acetato de eslicarbazepina y dolor neuropático» y «acetato de eslicarbazepina y cefaleas») presentados en las Reuniones Anuales de la Sociedad Española de Neurología (SEN) entre 2011 y 2015 y en otros congresos internacionales. Para mayor claridad, estructuramos el artículo con varias secciones diferentes.
Estudios experimentales del acetato de eslicarbazepina para el dolor neuropático
En estudios experimentales con ratones, se ha estudiado ampliamente el efecto analgésico del ESL en una amplia gama de estados de dolor inducido, incluyendo la neuralgia del trigémino, la neuropatía diabética y el dolor visceral; los resultados sugieren que el fármaco puede ser útil para el tratamiento del dolor inflamatorio y neuropático.13
Acetato de eslicarbazepina para la neuropatía diabética dolorosa
Encontramos un póster sobre la neuropatía diabética dolorosa (ND) presentado en el congreso de la Federación Europea del Dolor EFIC de 2013. El póster presentaba los resultados de un estudio de fase II multicéntrico, aleatorizado, doble ciego, controlado con placebo, de grupos paralelos y de búsqueda de dosis. El ensayo incluyó un período de lavado de 2 semanas, durante el cual se interrumpieron los tratamientos anteriores para el dolor neuropático, seguido de un período de titulación de una semana, un período de mantenimiento de 12 semanas y un período de seguimiento de 2 semanas. Un total de 557 pacientes fueron asignados aleatoriamente a recibir placebo, 400 mg de ESL dos veces al día (BID), 800 mg de ESL una vez al día (QD), 600 mg de ESL BID, 1200 mg de ESL QD o 800 mg de ESL BID. Tras 12 semanas de tratamiento, no se observaron diferencias estadísticamente significativas entre los individuos que recibieron placebo y los que recibieron ESL para el tratamiento del dolor (análisis de eficacia primario) según la Escala Numérica de Calificación del Dolor (NPRS). Sin embargo, el porcentaje de individuos que experimentaron una disminución de la intensidad del dolor ≥ 30% fue mayor en el grupo que recibió 400 mg de ESL BID que en el grupo de placebo (62,5% frente a 44,8%; P=0,0230). La incidencia de reacciones adversas fue del 38,0% en el grupo placebo y del 51,8% en el grupo tratado con 1200mg de ESL QD. Las reacciones adversas más frecuentes fueron vómitos, mareos y náuseas.14
Nuestra búsqueda bibliográfica también encontró un estudio de fase III multicéntrico, aleatorizado, doble ciego, controlado con placebo y con grupos paralelos de PDN; el estudio duró 15 semanas (3 semanas de ajuste de dosis + 12 semanas de seguimiento). La variable principal de eficacia fue el cambio en la intensidad del dolor desde el inicio del estudio (línea de base) hasta la finalización del mismo (15 semanas), y se midió mediante la NPRS. Un total de 332 pacientes con NDP fueron asignados aleatoriamente a recibir placebo, 1600 mg de ESL QD, 1200 mg de ESL QD o 800 mg de ESL QD. Tras 15 semanas de tratamiento, no se observaron diferencias estadísticamente significativas en el control del dolor entre los participantes que recibieron placebo y los que recibieron ESL. La incidencia de reacciones adversas osciló entre el 12,20% en el grupo de placebo y el 63,10% en el grupo que recibió 1600 mg de ESL QD. Las reacciones adversas más frecuentes fueron el vértigo, las náuseas y la hiponatremia (esta última dependiente de la dosis). Los resultados de este ensayo no fueron publicados.15
García Escrivá et al.16 compartieron su experiencia con ESL como tratamiento de segunda línea para la NDP refractaria a los fármacos tradicionales. Durante el año 2013, los autores identificaron a 8 pacientes con NDP cuyos tratamientos previos no habían logrado manejar el dolor de forma satisfactoria. En una primera visita, sustituyeron su tratamiento previo del dolor por el ESL, recogieron datos demográficos y administraron los siguientes cuestionarios: Escala DN4, Escala de Ansiedad y Depresión Hospitalaria, Escala Visual Analógica (EVA) para el dolor, Escala de Impresión Global del Paciente de Mejora y Escala de Impresión Global Clínica de Mejora. En una consulta de seguimiento realizada 12 semanas después del tratamiento, los pacientes completaron los mismos cuestionarios y se les preguntó sobre cualquier reacción adversa. Los datos recogidos se utilizaron para el análisis estadístico. En cuanto al tratamiento previo, el 75% de los pacientes había recibido pregabalina, 25% de amitriptilina, 12,5% de clonazepam y 12,5% de fentanilo, bien en monoterapia o en terapia combinada. Al inicio del tratamiento de ESL, los pacientes tomaban una media de 4,6 fármacos simultáneamente (rango, 1-11; mediana: 4,5). No se realizaron cambios en el tratamiento concomitante durante el periodo de seguimiento. El dolor neuropático, evaluado con la escala DN4, disminuyó significativamente a los 3 meses (P=.026, prueba de Wilcoxon). El estudio no encontró cambios significativos en ninguna de las características del dolor medidas por la escala. Los autores observaron una disminución significativa del dolor neuropático medido con la EVA (P=0,018, prueba de Wilcoxon). Las puntuaciones de los pacientes mejoraron tanto en la escala de ansiedad (P=0,102, prueba de Wilcoxon) como en la de depresión (P=0,276, prueba de Wilcoxon), aunque los cambios no fueron estadísticamente significativos. Subjetivamente, el 65,5% de los pacientes dijeron sentirse «mucho mejor» o «mejor» y el 87,5% de los médicos indicaron que los pacientes estaban «mejor» o «mucho mejor». El ESL se retiró en un paciente debido a reacciones adversas (mareos). A los 3 meses, 7 pacientes (87,5%) siguieron tomando ESL, 2 a 400 mg/día y 5 a 800 mg/día. A pesar del pequeño tamaño de la muestra, el ESL resultó ser una alternativa eficaz para el manejo del dolor neuropático en pacientes con NDP refractarios al tratamiento convencional, y mostró una buena tolerabilidad y adherencia.16,17
Acetato de eslicarbazepina para la neuralgia postherpética
Nuestra búsqueda bibliográfica encontró un póster sobre la neuralgia postherpética (NPH) presentado en el congreso de la Federación Europea del Dolor de 2013 EFIC. El póster presentaba los resultados de un estudio de fase II multicéntrico, aleatorizado, doble ciego, controlado con placebo, de grupos paralelos y de búsqueda de dosis. El estudio incluyó un periodo de lavado de 2 semanas, durante el cual se interrumpieron los tratamientos anteriores para la NPH, seguido de un periodo de titulación de una semana, un periodo de mantenimiento de 8 semanas y un periodo de seguimiento de 2 semanas. Un total de 567 pacientes fueron asignados aleatoriamente a recibir placebo, 400mg de ESL BID, 800mg de ESL QD, 600mg de ESL BID, 1200mg de ESL QD, o 800mg de ESL BID. El análisis por intención de tratar no mostró diferencias estadísticamente significativas entre los grupos de placebo y ESL en cuanto a la intensidad del dolor medida con la NPRS (análisis de eficacia primario). Sin embargo, según el análisis por protocolo, la intensidad del dolor disminuyó significativamente más en el grupo que recibió 800 mg de ESL BID que en el grupo de placebo (p=0,0277). La incidencia de reacciones adversas osciló entre el 31,2% en el grupo de placebo y el 54,4% en el grupo que recibió 800 mg de ESL BID. Las reacciones adversas más frecuentes fueron mareos, somnolencia, dolor de cabeza, náuseas y vértigo.18
Nuestra búsqueda bibliográfica también encontró un estudio de fase III multicéntrico, aleatorizado, doble ciego, controlado con placebo y con grupos paralelos en la NPH que duró 15 semanas. La variable principal de eficacia fue el cambio en la intensidad del dolor desde el inicio del estudio hasta su finalización (15 semanas), y se midió mediante la NPRS. Un total de 240 pacientes con NPH fueron asignados aleatoriamente a recibir placebo, 1600 mg de ESL QD, 1200 mg de ESL QD o 800 mg de ESL QD. No se observaron diferencias significativas en la intensidad del dolor entre los grupos de placebo y ESL tras 15 semanas de tratamiento. La incidencia de reacciones adversas osciló entre el 10% en el grupo de placebo y el 76,67% en el grupo tratado con 1600 mg de ESL QD. Las reacciones adversas más frecuentes fueron náuseas, mareos y dolor de cabeza. Los resultados de este estudio no se publicaron.19
Acetato de eslicarbazepina para las neuralgias craneales
Gaber et al.20 publicaron el caso de una mujer de 62 años con neuralgia del trigémino asociada a esclerosis múltiple adecuadamente controlada con CBZ. Sin embargo, el tratamiento tuvo que ser interrumpido debido a una hiponatremia sintomática recurrente. Varios fármacos, como el topiramato, la gabapentina y la amitriptilina, no lograron mejorar la neuralgia del trigémino. El ESL a dosis bajas (400mg diarios) consiguió un excelente control del dolor sin alterar la concentración plasmática de sodio.
Cuadrado et al.21 publicaron el caso de un hombre de 32 años con epicrania fugax refractaria a numerosos tratamientos (bloqueo del nervio occipital con triamcinolona y bupivacaína, gabapentina, lamotrigina, pregabalina, topiramato, zonisamida, valproato sódico, lacosamida, indometacina). La CBZ dosificada a 1200mg/día redujo la intensidad del dolor, pero tuvo que ser suspendida debido a la somnolencia. El ESL dosificado a 800mg/día redujo significativamente la frecuencia e intensidad del dolor. La dosis se aumentó a 1600 mg/día; el paciente mostró una buena tolerancia y permaneció asintomático. Los síntomas reaparecieron cuando se redujo la dosis.
Cação et al.22 estudiaron una cohorte de 15 pacientes con cefalea neuralgiforme unilateral de corta duración con inyección conjuntival y lagrimeo (SUNCT), de los cuales la mayoría respondió a lamotrigina, uno respondió a topiramato y uno a ESL.
El caso clínico presentado por Aledo Serrano et al.23 en la 66ª Reunión Anual de la SEN describió el caso de un hombre de 38 años con diagnóstico de epicrania fugax refractario a lamotrigina, pregabalina, gabapentina, topiramato, zonisamida, indometacina, valproato, lacosamida, levetiracetam, bloqueo anestésico del nervio occipital mayor e inyección de toxina botulínica en el lugar del dolor. La paciente respondió parcialmente a la CBZ, pero experimentó reacciones adversas graves. El paciente permaneció asintomático con ESL en dosis de 1200 mg diarios.
Sánchez Larsen et al.24 presentaron un estudio observacional y retrospectivo en la 66ª Reunión Anual de la SEN, analizando un grupo de pacientes con neuralgia del trigémino tratados con ESL en monoterapia o en terapia combinada. Las variables principales fueron la intensidad del dolor antes y después del tratamiento (VAS), la frecuencia de los ataques de dolor antes y después del tratamiento y las reacciones adversas. El estudio incluyó a 10 pacientes (4 en monoterapia); 7 eran mujeres, y la edad media era de 67,9 años (rango, 28-92). El tiempo medio de seguimiento fue de 24,7 meses, con la excepción de 2 abandonos debidos a reacciones adversas leves (mareos). Ningún paciente experimentó reacciones adversas graves; uno presentó hiponatremia. La intensidad y la frecuencia del dolor disminuyeron en 9 de los 10 pacientes. En estos pacientes, la intensidad del dolor disminuyó de 8,7 puntos a 2,6 y la frecuencia del dolor se redujo de 12,13 a 2,28 ataques al día (4 pacientes estaban asintomáticos, 3 experimentaron 1-2 ataques a la semana, 2 experimentaron leves mejoras pero la frecuencia de los ataques seguía siendo alta). En esta serie, el ESL resultó ser eficaz y seguro para el tratamiento de la neuralgia del trigémino, y superior a la CBZ desde el punto de vista de la seguridad y la farmacocinética, aunque los autores recomiendan una estrecha vigilancia de los niveles de sodio.
En un estudio presentado en la 67ª Reunión Anual de la SEN (2015), Abril-Jaramillo et al.25 analizaron la respuesta al tratamiento con ESL en pacientes con neuralgias craneales (el 56% tenía neuralgia del trigémino) que habían respondido bien a CBZ u OXC pero que experimentaron reacciones adversas a estos fármacos. La respuesta al ESL se evaluó en 15 pacientes durante un periodo de 6 meses; la evaluación inicial incluyó los datos de la historia clínica, la exploración física, las pruebas complementarias, la información sobre los tratamientos anteriores y las reacciones adversas que motivaron la interrupción del fármaco. Posteriormente, los pacientes fueron evaluados a los 3 y 6 meses para valorar la eficacia del tratamiento y las posibles reacciones adversas. La respuesta fue favorable en 13 de los 15 pacientes; ESL fue mejor tolerado que CBZ y OXC.
Acetato de eslicarbazepina en series de casos de diferentes etiologías
En la 63ª Reunión Anual de la SEN (2011, Barcelona), Tena Mora26 presentó en formato póster los resultados de un estudio prospectivo y descriptivo de la eficacia y seguridad de ESL en monoterapia en 6 pacientes con diferentes tipos de dolor neuropático. Los análisis (recuento sanguíneo completo, prueba de coagulación, niveles de sodio y potasio, función renal y hepática) se realizaron a los 1 y 3 meses del inicio del tratamiento; la EVA se completó durante la primera consulta (EVA 1), al mes (EVA 2) y a los 3 meses de seguimiento (EVA 3). El estudio incluyó a 4 pacientes con neuralgia primaria del trigémino (100% mujeres; EVA 1: 8-10, EVA 2: 0-3, EVA 3: 0-3), uno de los cuales presentó somnolencia que se resolvió cuando se dividió la dosis de mantenimiento en 2 dosis diarias; un paciente con dolor postinfarto (hombre de 80 años, EVA 1: 9; el tratamiento se suspendió a los 4 días debido a la somnolencia; la CBZ se suspendió gradualmente en paralelo); y un paciente con dolor facial idiopático persistente (mujer de 70 años; EVA 1: 9, EVA 2: 8, EVA 3: 8). Ninguno de los pacientes mostró alteraciones en los resultados de los análisis de sangre durante el periodo de estudio (3 meses). El autor destaca los efectos analgésicos de ESL para la neuralgia primaria del trigémino.
En la 66ª Reunión Anual de la SEN, García Arguedas et al.27 presentaron los resultados de un estudio retrospectivo y descriptivo de 10 pacientes con dolor neuropático tratados con ESL en monoterapia. Analizaron las causas del dolor, la dosis utilizada, la eficacia del tratamiento (utilizando las puntuaciones de la EVA al inicio y a los 3 meses) y la tolerabilidad del tratamiento. Las causas del dolor fueron la neuralgia del trigémino en 5 pacientes, la NDP en 3 y la NPH en 2. La dosis más utilizada fue de 800 mg (dosis máxima de 1200 mg en un paciente). La puntuación media de la EVA fue de 8,2 en la consulta inicial y de 2,4 en la consulta de seguimiento a los 3 meses, con una disminución global de más del 50% en la intensidad del dolor. En cuanto a la tolerabilidad, la reacción adversa más frecuente fue el mareo; un paciente desarrolló una hiponatremia leve, pero no interrumpió el tratamiento.
Durante la 67ª Reunión Anual de la SEN, Pagola Lorz et al.28 presentaron su experiencia con el ESL como tratamiento de segunda línea para el dolor neuropático refractario a los fármacos tradicionales. Este estudio descriptivo y retrospectivo analizó la respuesta al ESL en 10 pacientes con dolor neuropático mal controlado. Las variables principales fueron la causa del dolor, la dosis de ESL, las mejoras del dolor (calificadas como «mucho mejor», «mejor», «sin cambios» o «peor»), el tratamiento concomitante para el dolor neuropático y las reacciones adversas. Las causas del dolor fueron neuralgia del trigémino en 6 pacientes, neuralgia glosofaríngea en uno, NPH en 2 y dolor talámico en uno. Los pacientes recibieron una dosis media de 800 mg de ESL; 400 mg fueron suficientes para 3 pacientes, mientras que 2 necesitaron 1200 mg. Siete de los 10 pacientes informaron de que se sentían «mucho mejor», 2 se sentían «mejor» y el restante informó de que «no había cambios». En cuanto al tratamiento concomitante, 3 pacientes recibieron gabapentina, uno pregabalina y otro amitriptilina. Las reacciones adversas (apatía, mareos, visión borrosa) fueron leves y transitorias, y no requirieron la interrupción del fármaco en ningún caso.
En la 67ª Reunión Anual de la SEN, Bermejo Velasco et al.29 presentaron los resultados de un estudio retrospectivo de las historias clínicas de 10 pacientes con dolor neuropático y que recibían ESL. Los autores evaluaron la eficacia del ESL mediante la EAV, el porcentaje de respondedores (> 50% de disminución de la intensidad del dolor), el porcentaje de pacientes sin dolor, la disminución del tratamiento concomitante, las reacciones adversas, la dosis utilizada, el programa de titulación y la etiología del dolor neuropático. Los pacientes tuvieron un seguimiento medio de 6,1 meses. El estudio incluyó un total de 32 pacientes. La dosis media de ESL fue de 920±220mg/día. La intensidad del dolor disminuyó una media de 4,4±1,6 puntos, con un 46% de pacientes identificados como respondedores y un 13% sin dolor. Alrededor del 78% de los pacientes continuaron con el tratamiento. Las principales razones para la interrupción del tratamiento fueron la ineficacia, la somnolencia y los mareos.
Las tablas 1 y 2 resumen los resultados de los ensayos clínicos, los estudios observacionales y los informes de casos incluidos en esta revisión.
Resumen de los estudios clínicos incluidos en la revisión.
| Tipo de estudio | Referencia | Tamaño de la muestra | Enfermedad | ESL dosis | Duración | Resultados principales | Seguridad |
|---|---|---|---|---|---|---|---|
| Enayo de fase II | Kress et al.14 | 557 | PDN | Placebo, ESL 400mg BID, ESL 800mg QD, ESL 600mg BID, ESL 1200mg QD, y ESL 800mg BID | 15 semanas | No se observaron diferencias estadísticamente significativas entre los individuos que recibieron placebo y los que recibieron ESL para el tratamiento del dolor (análisis de eficacia primario), según las puntuaciones de la NPRS.El porcentaje de individuos que experimentaron una≥30% de disminución de la intensidad del dolor fue mayor en el grupo que recibió 400mg de ESL BID (62,5%) que en el grupo de placebo (44,8%) (P = .0230). | La incidencia de reacciones adversas osciló entre el 38,0% en el grupo de placebo y el 51,8% en el grupo tratado con 1200mg de ESL QD. Las reacciones adversas más frecuentes fueron vómitos, mareos y náuseas. |
| Ensayo de fase III | https://clinicaltrials.gov/ct2/show/study/NCT01129960?term=eslicarbazepine&rank=1915 | 332 | PDN | Placebo, ESL 1600mg QD, ESL 1200mg QD, y ESL 800mg QD | 15 semanas | No se observaron diferencias estadísticamente significativas entre los individuos que recibieron placebo y los que recibieron ESL para el tratamiento del dolor, según las puntuaciones de la NPRS. | La incidencia de reacciones adversas osciló entre el 12,20% en el grupo de placebo y el 63,10% en el grupo tratado con 1600 mg de ESL QD. Las reacciones adversas más frecuentes fueron vértigo, náuseas e hiponatremia (esta última fue dependiente de la dosis). |
| Ensayo de fase II | Kress et al.18 | 567 | PHN | Placebo, ESL 400mg BID, ESL 800mg QD, ESL 600mg BID, ESL 1200mg QD, y ESL 800mg BID | 11 semanas | El análisis por intención de tratar no mostró diferencias estadísticamente significativas entre los grupos de placebo y de ESL en cuanto a la intensidad del dolor medida con la NPRS (análisis de eficacia primario).Según el análisis por protocolo, la intensidad del dolor disminuyó significativamente más en el grupo que recibió 800 mg de ESL BID que en el grupo de placebo (P = 0,0277). | La incidencia de reacciones adversas osciló entre el 31,2% en el grupo de placebo y el 54,4% en el grupo que recibió 800mg de ESL BID. Las reacciones adversas más frecuentes fueron mareos, somnolencia, dolor de cabeza, náuseas y vértigo. |
| Ensayo de fase III | https://clinicaltrials.gov/ct2/show/study/NCT01124097?term=eslicarbazepine&rank=18§=X7015619 | 240 | PHN | Placebo, ESL 1600mg QD, ESL 1200mg QD, y ESL 800mg QD | 15 semanas | No se observaron diferencias estadísticamente significativas entre los individuos que recibieron placebo y los que recibieron ESL para el tratamiento del dolor, según las puntuaciones de la NPRS. | La incidencia de reacciones adversas osciló entre el 10% en el grupo de placebo y el 76,67% en el grupo tratado con 1600 mg de ESL QD. Las reacciones adversas más frecuentes fueron náuseas, mareos y dolor de cabeza. |
BID: dos veces al día; ESL: acetato de eslicarbazepina; NPRS: Numeric Pain Rating Scale; PDN: neuropatía diabética dolorosa; PHN: neuralgia postherpética; QD: una vez al día.
Resumen de los estudios observacionales y ensayos clínicos incluidos en la revisión.
| Tipo de estudio | Referencia | Tamaño de la muestra | Enfermedad | Dosis de ESL | Duración | Resultados principales | Seguridad |
|---|---|---|---|---|---|---|---|
| Prospectivo, descriptivo, estudio observacional | García Escrivá et al.16 | 8 | PDN con fracaso del tratamiento previo | ESL 400mg/día (2 pacientes) y ESL 800mg/día (5 pacientes) | 12 semanas | Mejora en las puntuaciones de las escalas DN4, HADS, VAS, PGI-I y CGI-I. | 1 abandono debido a mareos |
| Caso clínico | Gaber et al.20 | 1 | TN asociada a esclerosis múltiple fue bien manejada con CBZ, pero el fármaco se suspendió debido a hiponatremia sintomática recurrente. | 400mg/día | – | Excelente manejo del dolor | Buena tolerancia sin alteraciones en los niveles plasmáticos de sodio |
| Caso clínico | Cuadrado et al.21 | 1 | Epicrania fugax refractaria con mala tolerancia a la CBZ | 1600mg/día | – | Significativa mejora de la frecuencia e intensidad del dolor | Buena tolerancia |
| Serie de casos | Cação et al.22 | 1 | SUNCT | 800mg/día | – | Manejo del dolor y disminución del número de ataques al día | El paciente falleció por causas no relacionadas con el ESL un año después. |
| Caso clínico | Aledo Serrano et al.23 | 1 | Epicrania fugax refractaria con mala tolerancia a la CBZ | 1200mg/día | – | Asintomática | Buena tolerancia |
| Retrospectiva, descriptivo, estudio observacional | Sánchez Larsen et al.24 | 10 | TN (4 pacientes en monoterapia y 6 en politerapia) | NA | Tiempo medio de seguimiento: 24,7 meses | La intensidad del dolor y la frecuencia de los ataques disminuyeron en 9 de los 10 pacientes. | Dos pacientes abandonaron debido a reacciones adversas leves (mareos). No se notificaron efectos adversos graves. Un paciente presentó hiponatremia. |
| Estudio observacional, descriptivo y prospectivo | Abril-Jaramillo et al.25 | 15 | Neuralgia craneal (TN en el 56% de los pacientes), con buena respuesta a CBZ u OXC pero asociada a reacciones adversas al fármaco | NA | 6 meses | Respuesta favorable en 13 de los 15 pacientes | Tolerabilidad de aproximadamente el 90% |
| Prospectivo, descriptivo, estudio observacional | Tena Mora26 | 6 | 4 TN, 1 dolor post-apoplejía, 1 dolor facial idiopático persistente (todos en monoterapia) | NA | 3 meses | Efectos analgésicos significativos para la TN | Un paciente con TN mostró somnolencia, que se resolvió cuando se dividió la dosis de mantenimiento en 2 dosis. El paciente con dolor postinfarto interrumpió el tratamiento a los 4 días debido a la somnolencia. Ningún paciente mostró alteraciones en los resultados de los análisis durante el período de estudio. |
| Estudio retrospectivo, descriptivo y observacional | García Arguedas et al.27 | 10 | 5 TN, 3 PDN y 2 PHN (monoterapia) | Dosis media: 800mg/día (dosis máxima de 1200mg/día en un paciente) | 3 meses | Disminución de más del 50% en la intensidad del dolor (EVA) | Mareos, hiponatremia leve en un paciente, sin abandonos |
| Estudio retrospectivo, descriptivo, observacional | Pagola Lorz et al.28 | 10 | 6 NT, 1 neuralgia glosofaríngea, 2 NPH y 1 dolor talámico (sin respuesta a los fármacos tradicionales) | Dosis media: 800 mg/día; 3 pacientes necesitaron tan sólo 400 mg/día mientras que 2 necesitaron 1200 mg/día. | NA | Siete pacientes informaron de que se sentían «mucho mejor», 2 se sintieron «mejor» y el restante informó de que «no hubo cambios». | Reacciones adversas leves y transitorias (apatía, mareos, visión borrosa) que no dieron lugar a la interrupción del fármaco |
| Estudio retrospectivo, descriptivo y observacional | Bermejo Velasco et al.29 | 32 | Diferentes etiologías del dolor neuropático refractario a los fármacos tradicionales. | Dosis media: 920±220mg/día | Tiempo medio de seguimiento: 6,1 meses | Disminución media de la intensidad del dolor de 4,4±1,6 puntos en la EVA; 46% de respondedores (> 50% de disminución de la intensidad del dolor) y 13% de pacientes sin dolor | El 78% de los pacientes continuó el tratamiento. Los principales motivos de interrupción del tratamiento fueron la ineficacia, la somnolencia y los mareos. |
CBZ: carbamazepina; CGI-I: escala de Impresión Clínica Global de la Mejora; ESL: acetato de eslicarbazepina; HADS: Escala Hospitalaria de Ansiedad y Depresión; NA: no disponible; OXC: oxcarbazepina; NDP: neuropatía diabética dolorosa; IGP-I: escala de Impresión Global de la Mejoría del Paciente; NPH: neuralgia postherpética; SUNCT: cefalea neuralgiforme unilateral de corta duración con inyección conjuntival y lagrimeo; NT: neuralgia del trigémino; EVA: escala visual analógica.
Discusión
Los fármacos de la familia de las dibenzazepinas pueden causar hiponatremia (nivel de sodio
135mmol/L); ésta es una reacción adversa frecuente a la CBZ y al OXC. La incidencia de hiponatremia secundaria al tratamiento con CBZ oscila entre el 4,8% y el 40%.30,31 Cada vez hay más pruebas de los efectos nocivos de la hiponatremia, incluso en los casos leves, especialmente en los pacientes de edad avanzada, entre los que el dolor neuropático es relativamente frecuente.32,33 La hiponatremia inducida por el fármaco debe considerarse un motivo para cambiar el tratamiento.
Los médicos suelen enfrentarse a un dilema cuando la CBZ es el único fármaco capaz de controlar un problema clínico específico, como la neuralgia del trigémino. El ESL puede constituir una alternativa en los pacientes que experimentan reacciones adversas a la CBZ. En los ensayos clínicos y en los estudios de observación de la ESL en pacientes con epilepsia34-36 rara vez se ha notificado hiponatremia; por lo tanto, el cambio de CBZ u OXC a ESL en pacientes que han desarrollado hiponatremia parece ser una opción eficaz y bien tolerada. Sin embargo, los niveles de sodio deben seguir siendo controlados, ya que algunos pacientes siguen mostrando hiponatremia tras el cambio de fármaco.37
Estas diferencias en los perfiles de los fármacos antiepilépticos de la familia de las dibenzazepinas pueden dar lugar a diferentes niveles de eficacia, tolerabilidad y adherencia,38 lo que puede llevar a los médicos a considerar el cambio de un fármaco a otro de la misma familia para adaptar el tratamiento a las características de cada paciente. El proyecto EPICON, en el que un panel de especialistas en epilepsia adoptó el método Delphi, evaluó situaciones específicas y la metodología para cambiar de CBZ u OXC a ESL. El objetivo del estudio era emitir recomendaciones consensuadas para pasar de CBZ u OXC a ESL en determinados pacientes. Las principales recomendaciones son las siguientes 1) La transición de CBZ a ESL debe realizarse de forma progresiva a lo largo de 1 a 3 semanas, empleando una proporción CBZ:ESL de 1:1,3. 2) El cambio de CBZ a ESL se recomienda a los pacientes que olvidan con frecuencia tomar su medicación, a los que trabajan en turnos rotativos, a los pacientes polimedicados, a los pacientes con problemas cognitivos, a los pacientes con osteopenia/osteoporosis grave, a los pacientes con dislipidemia o enfermedad hepática distinta de la insuficiencia hepática aguda y a los hombres con disfunción eréctil causada por la CBZ. 3) El OXC puede cambiarse por el ESL durante la noche en una proporción de dosis de 1:1; esto se recomienda para los pacientes que olvidan frecuentemente tomar su medicación, los que trabajan en turnos rotativos, los pacientes polimedicados o los pacientes con problemas cognitivos. 4) No se recomienda el cambio de fármaco en los pacientes que presenten erupciones cutáneas secundarias al tratamiento con CBZ u OXC.39 Aunque estas recomendaciones se aplican a los pacientes con epilepsia, pueden ser útiles en otras situaciones clínicas (diferentes tipos de dolor neuropático, neuralgia del trigémino y otros tipos de cefalea) asociadas a una mala adherencia o tolerabilidad de CBZ u OXC.
Conclusiones
Dado el mecanismo de acción de ESL (interacción selectiva con el estado inactivo del VGSC mediante inactivación lenta, en contraste con la inactivación rápida de CBZ y OXC, e inhibición de las corrientes hCaV3.2 con mayor afinidad que la CBZ) parecería inicialmente una buena opción para el tratamiento del dolor neuropático, la cefalea y la neuralgia craneal.
Sin embargo, las pruebas son demasiado escasas para recomendar la ESL para estas indicaciones. La mayoría de las pruebas disponibles proceden de estudios observacionales abiertos con muestras pequeñas y sin grupo de control. Además, algunos de los estudios incluidos en esta revisión abordan diferentes entidades clínicas26-29 con diferentes mecanismos fisiopatológicos. Por lo tanto, la heterogeneidad de los datos impide establecer cualquier conclusión general sobre la eficacia del ESL. Curiosamente, los ensayos clínicos sobre el ESL como tratamiento del dolor neuropático (NDP y NPH) no han encontrado disminuciones estadísticamente significativas de la intensidad del dolor.
La escasez de estudios publicados sobre el tema puede sugerir un sesgo de publicación. De hecho, los ensayos clínicos de fase III incluidos en nuestra revisión no fueron publicados.
En conclusión, la ESL puede constituir una alternativa válida para el tratamiento del dolor neuropático, la cefalea y las neuralgias craneales en pacientes que muestran una mala respuesta o intolerancia a los fármacos tradicionales, especialmente en el caso de la neuralgia del trigémino; son necesarios más estudios aleatorios con muestras más amplias para confirmar esta hipótesis. La utilidad del ESL para la neuralgia del trigémino puede estar asociada a la excelente respuesta de la afección a la CBZ y a las similitudes bioquímicas entre ambos fármacos.
Conflictos de intereses
El estudio cumple con las normas éticas y los criterios de autoría de la revista. Los autores no tienen ningún conflicto de intereses que declarar.
Leave a Reply