Varme
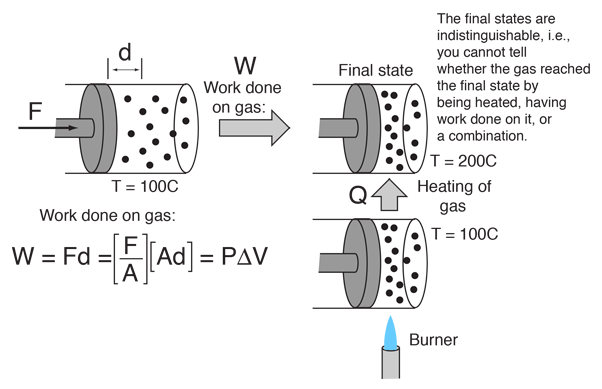
Dette eksempel på, at varme og arbejde kan udskiftes som midler til at tilføre energi til et system, kan bidrage til at fjerne nogle misforståelser om varme. Jeg fandt ideen i en lille artikel af Mark Zemansky med titlen “The Use and Misuse of the Word ‘Heat’ in Physics Teaching” (Brugen og misbruget af ordet ‘varme’ i fysikundervisningen). En nøgleidé fra dette eksempel er, at hvis man præsenteres for en gas med høj temperatur, kan man ikke sige, om den har nået den høje temperatur ved at blive opvarmet, ved at der er udført arbejde på den eller ved en kombination af de to.
For at beskrive den energi, som et objekt med høj temperatur har, er det ikke en korrekt brug af ordet varme at sige, at objektet “besidder varme” – det er bedre at sige, at det besidder intern energi som følge af dets molekylære bevægelse. Ordet varme er bedre reserveret til at beskrive processen med overførsel af energi fra et objekt med høj temperatur til et objekt med lavere temperatur. Man kan ganske vist tage en genstand med en lav intern energi og hæve den til en højere intern energi ved at opvarme den. Men man kan også øge dets indre energi ved at udføre arbejde på det, og da den indre energi i et objekt med høj temperatur ligger i molekylernes tilfældige bevægelse, kan man ikke sige, hvilken mekanisme der blev brugt til at give det denne energi.
I sin advarsel til både lærere og elever om faldgruberne ved at misbruge ordet “varme” råder Mark Zemansky til at reflektere over jinglen:
“Teaching thermal physics |
Lad være med at henvise til “varmen i et legeme” eller sige “denne genstand har dobbelt så meget varme som det legeme”. Han protesterer også mod brugen af den vage betegnelse “termisk energi” og mod brugen af ordet “varme” som verbum, fordi de giver næring til misforståelserne, men det er svært at undgå disse udtryk. Han vil råde til at indføre og bruge begrebet intern energi så hurtigt som muligt. |
Zemansky peger på termodynamikkens første lov som et afklarende forhold. Den første lov identificerer både varme og arbejde som metoder til energioverførsel, der kan medføre en ændring i et systems interne energi. Herefter har hverken ordene arbejde eller varme nogen nytteværdi til at beskrive systemets endelige tilstand – vi kan kun tale om systemets interne energi.
| Mekanisk ækvivalent til varme | Termodynamikkens første lov | Beregning |
Leave a Reply